Luonnollisesti johdettujen alkaloidien mahdollisuudet monikohdeterapeuttisina aineina neurodegeneratiivisiin sairauksiin
Mar 19, 2022
Ottaa yhteyttä:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Abstrakti:Alkaloiditovat luokka sekundaarisia metaboliitteja, jotka voivat olla peräisin kasveista, sienistä ja merisienistä. Ne tunnetaan laajalti jatkuvana lääkelähteenä kroonisten sairauksien, kuten syövän, diabeteksen ja hermostoa rappeuttavien sairauksien, hoitoon. Esimerkiksi galantamiini ja hupertsiini A ovatalkaloidijohdannaisia, joita tällä hetkellä käytetään neurodegeneratiivisten sairauksien oireenmukaiseen hoitoon. Neurodegeneratiivisten sairauksien etiologia on polygeeninen ja monitekijäinen, mukaan lukien, mutta ei rajoittuen, tulehdus, oksidatiivinen stressi ja proteiinien aggregaatio. Siksi luonnontuotteisiin perustuvat alkaloidit, joilla on polyfarmakologisia modulaatioominaisuuksia, ovat mahdollisesti käyttökelpoisia lääkkeiden jatkokehityksessä tai, vähemmässä määrin, ravintoaineina hermoston rappeuman hallinnassa. Tämän katsauksen tarkoituksena on keskustella ja tehdä yhteenveto viimeaikaisesta kehityksestä luonnosta peräisin olevissa alkaloideissa hermoston rappeutumissairauksissa.
Avainsanat:alkaloidit; multi-target agent; koliiniesteraasi; hermoja suojaava; hermoston tulehdus; neurogeneesi; amyloidi-beeta; tau-proteiini; huumeiden kaltaisuus

EstääAlzheimerin tautisairauden kanssacistanche
Yew Rong Kong 1,†, Kai Ching Tay 1,†, Yi Xiang Su 1, Choon Kwang Wong 1, Wen Nee Tan 2,* ja Kooi Yeong Khaw
1 Biofunctional Molecule Exploratory Research Group (BMEX), Farmasian koulu, Monash University Malesia, Jalan Lagoon Selatan, Bandar Sunway 47500, Malesia
2 Chemistry Section, School of Distance Education, Universiti Sains Malaysia, Penang 11800, Malesia
1. Esittely
Neurodegeneratiivinensairaudetluokitellaan kroonisten sairauksien ryhmään, jotka ovat enimmäkseen parantumattomia ja joille on ominaista etenevä muistin menetys ja/tai hermosolujen kuolema keskushermostossa. Joitakin esimerkkejä ovat Alzheimerin tauti (AD) ja Parkinsonin tauti (PD), ja näiden sairauksien hoitosuunnitelmat ovat vain oireenmukaisia hoitoja, jotka eivät estä taudin etenemistä [1,2]. Suurin osa näistä sairauksista liittyy läheisesti ikään. Jokaiseen neurodegeneratiiviseen sairauteen liittyy erilaisia kliinisiä ilmenemismuotoja, kuten kognitiivisia toimintahäiriöitä ja päivittäisen toiminnan heikkenemistä [3]. Vuonna 2016 noin 43,8 miljoonaa ihmistä kärsi dementiasta ja 6,1 miljoonaa ihmistä Parkinsonin taudista, ja määrät kasvavat edelleen vuosittain [4,5]. AD muodostaa noin 75 prosenttia kaikista dementiatapauksista, joten sitä pidetään yleisimpänä dementian muotona [6,7].
AD-oireita ovat muistin menetys, ja se voi edetä pitkälle edenneeseen vaiheeseen, joka ilmenee kiihtyneisyytenä, apatiana, aggressiona, hallusinaatioina, väärinä uskomuksina ja kognitiivisena toimintahäiriönä; lopulta vakavat AD-potilaat kuolevat fysiologisten perustoimintojen menettämiseen ja infektioiden aiheuttamiin komplikaatioihin [8–10]. AD:n hoitovaihtoehdot rajoittuvat koliiniesteraasin estäjiin, mukaan lukien donepetsiili, rivastigmiini ja galantamiini, sekä N-metyyli-D-aspartaattireseptorin (NMDA) antagonistiin nimeltä memantiini. Vaikka koliiniesteraasi-inhibiittorit estävät asetyylikoliinin hajoamista lisäämään kolinergistä hermosolujen aktiivisuutta keskushermostossa, memantiini estää ylimääräisen glutamaatin aiheuttamaa neurotoksisuutta [11]. PD:lle on tunnusomaista liikkeen hitaus ja vähintään yksi seuraavista oireista, mukaan lukien lepovapina, asennon epävakaus tai lihasten jäykkyys. PD:tä hoidetaan yleensä lääkkeillä, jotka lisäävät dopaminergistä hermotoimintaa, mukaan lukien levodopa ja dopamiiniagonistit, sekä lääkkeillä, jotka estävät dopamiinin aineenvaihduntaa, mukaan lukien katekoli-O-metyylitransferaasin (COMT) estäjät ja monoamiinioksidaasi B:n (MAO-B) estäjät [12]. Kummallakaan ei ole parannuskeinoa, joka joko pysäyttäisi taudin etenemisen tai kumoaa vaurioita. AD on monitekijäinen sairaus, koska sen etiologia liittyy amyloidi-beetan kertymiseen, tau-proteiinin hyperfosforylaatioon, eksitotoksisuuteen, oksidatiiviseen stressiin ja hermotulehdukseen [7,13]. Vaikka PD liittyy solunsisäisten aggregaattien sisältävien proteiinien, kuten ubikitiinin ja alfa-synukleiinin (-Syn), kerääntymiseen, jotka muodostavat Lewy-kappaleita, dopaminergiseen hermosolujen rappeutumiseen substantia nigra pars compactassa (SNpc) ja hermotulehdukseen [12,14].

Cistanche herba voi parantaa muistia
Toinen samankaltaisuus AD:n ja PD:n välillä on, että molemmat sairaudet liittyvät hermotulehdukseen. Amyloidi-beetaplakkien aiheuttama neurotulehdus AD:ssa ja alfa-synukleiiniaggregaattien indusoima PD:ssä pahentaa olennaisesti kolinergisten ja dopaminergisten neuronien menetystä, vastaavasti [11,14]. Koska nykyiset hoitovaihtoehdot tarjoavat yksinomaan oireenmukaista helpotusta, meneillään oleva tutkimus on keskittynyt hermoston rappeutumissairauksien monikohdeisten hoitovaihtoehtojen tunnistamiseen. Luonnontuotteet ovat tuottelias terapeuttisten johtolankojen lähde. Esimerkiksi luonnollisesti johdettualkaloiditmukaan lukien lääkekasveista peräisin oleva hupertsiini A ja galantamiini, on löydetty ja tutkittu niiden potentiaalin suhteen AD:n hoidossa [15]. Tähän mennessä paradigman muutos kohti monikohdennettua modulaatiolähestymistapaa hermostoa rappeutuvien sairauksien hoidossa on sopusoinnussa vallitsevien tunnusomaisten luonnontuotejohdannaisten kanssa, joilla on monia kohdentavia ominaisuuksia. Tämä katsaus tarjoaa päivityksen viimeaikaiseen kirjallisuuteen alkaloidipohjaisista koliiniesteraasi-inhibiittoreista ja niiden in vivo -tehokkuudesta eläinmalleissa, ja korostaa niiden mekanismeja hermoston rappeutumishäiriöihin liittyvissä kokeellisissa malleissa, mukaan lukien hermosolujen suojaus, hermotulehdus, neurogeneesi, tau-patologia ja amyloidi- beetan kertymistä. Yksi lääkekehityksen esteistä sisältää lääkkeen kaltaiset ominaisuudet. Siksi myös alkaloidipohjaisten yhdisteiden fysikaalis-kemiallisten ominaisuuksien analyysi suoritetaan.
2. Luonnontuotteista peräisin olevien alkaloidien koliiniesteraasin estopotentiaali
Acetylcholinesterase enzyme (AChE) is predominantly found in the cholinergic synapses while butyrylcholinesterase enzyme (BuChE) is a non-substrate-specific enzyme that can be found throughout the body including in glial cells. Low levels of AChE and high levels of BuChE have been reported as AD progress [16]. Acetylcholinesterase enzyme inhibitors (AChEi) including galanthamine (1) and donepezil are drugs that have been approved by the Food and Drug Agency (FDA) to manage AD. Archie is used to enhance acetylcholine (ACh), a neurotransmitter responsible for cognition at a homeostatic level in the brain [17–19]. Therefore, chemical compounds able to inhibit the AChE enzyme or both AChE and BuChE enzymes (dual inhibitor) are considered essential in the management of the progression of AD. In this review, all naturally occurring alkaloids are categorized by their inhibitory activities in IC50. By definition, IC50 is a measure of the potency that one chemical substance has to inhibit a specific biological or biochemical function [11]. The inhibition in three categories (IC50 ≤ 10 µM, 10–50 µM, and >50 µM) on esitetty kuvassa 1.
Indolialkaloidit ovat yksi suurimmista heterogeenisten sekundaaristen metaboliittien ryhmästä, joka sisältää kuusijäsenisen aromaattisen renkaan, joka on fuusioitu viisijäseniseen typpeä sisältävään pyrrolirenkaaseen [36]. Rauvolfifia-reflexin reskinnamiinin (3) raportoitiin käyttäytyvän kaksoiskoliiniesteraasi-inhibiittorina (IC50 AChE 11,01 µM; BuChE 8,06 µM) [20]. Monoterpeeni-indolialkaloidit tunnistetaan molekyyleiksi, jotka sisältävät monoterpenoidiyksikön fuusioituneena indoliosaan. Nauclea Officinalisista eristetyillä monoterpeeniindolialkaloideilla (4–6) on selektiivinen BuChE:tä estävä vaikutus. Augustiinin (4), nukleiinin (5) ja Augustiinin (6) osoitettiin inhiboivan BuChE:tä IC50-arvolla alueella 1,03 - 7,70 uM. Kineettinen tutkimus osoitti, että 4 oli sekamoodi-inhibiittori, jonka Ki-arvo oli 6,12 µM [21].

-karboliinialkaloidit muodostavat indoliosan, joka on fuusioitu pyridiinin C-3- ja C-4-osaan orto-asemassaan [37]. Kymmenen Peganum harmalan karboliinialkaloidilla (7–16) on raportoitu olevan koliiniesteraasia estäviä vaikutuksia IC50-arvoilla<10 µm.="" harmol="" (8),="" harmalol="" (13),="" deoxyvasicine="" (15),="" and="" vaccine="" (16)="" were="" potent="" inhibitors="" of="" buche="" with="" ic50="" values="" in="" the="" range="" of="" 0.04="" to="" 0.66="" µm.="" however,="" harmine="" was="" the="" most="" potent="" ache="" inhibitor="" with="" an="" ic50="" of="" 1.21="" µm="" among="" the="" indole="" alkaloids.="" a="" preliminary="" structure-activity="" relationship="" study="" showed="" that="" multiple="" substitutions="" at="" the="" indole="" ring="" and="" saturation="" of="" the="" pyridine="" ring="" were="" essential="" for="" the="" cholinesterase="" inhibition="" effects="" [22].="" 3-ethyl-12-methoxy-β-="" carboline="" (17)="" and="" 6,12-dimethoxy-3-ethyl-β-carboline="" (18)="" from="" picrasma="" quassinoids="" were="" reported="" as="" possessing="" ache="" inhibitory="" properties="">
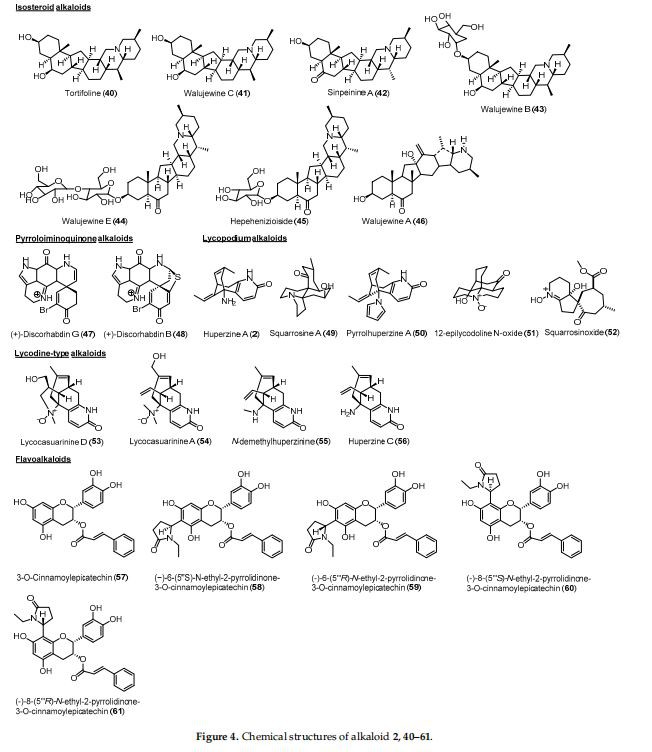
Kuva 2 paljastaa, että yhteensä 55 alkaloidia tunnistettiin AChEi:ksi, kun taas 24 alkaloidia tunnistettiin BuChEi:ksi. Pohjimmiltaan 16 alkaloidin osoitettiin inhiboivan molempia entsyymejä IC50-arvoilla, jotka ovat yhtä suuria tai pienempiä kuin 10 uM. Taulukossa 1 on lueteltu kasveista eristetyt bioaktiiviset alkaloidit sekä niiden koliiniesteraasia estävät vaikutukset, kun taas kuviot 3 ja 4 esittävät alkaloidien 1–61 kemiallisia rakenteita.

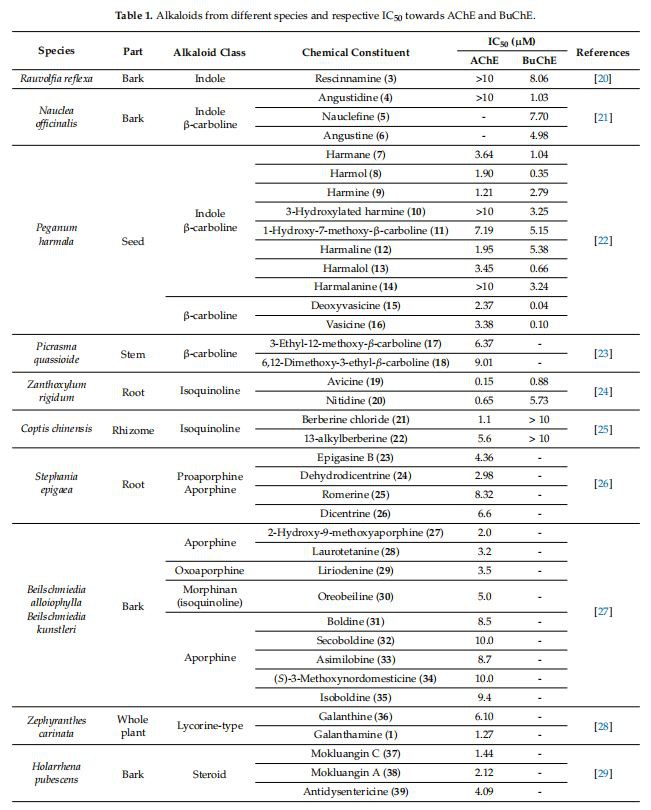

Isokinoliinialkaloidit kuuluvat useisiin luonnollisista lähteistä saatuihin alkaloidien luokkiin. Ne koostuvat isokinoliini- tai tetrahydroisokinoliinirenkaasta perusrungokseen [38]. Neuvo (19) oli tehokkain kaksoiskoliiniesteraasi-inhibiittori, jonka IC50-arvot olivat 0,15 ja 0,88 µM sekä AChE:lle että BuChE:lle. Ranitidiinilla (20) oli heikompi estävä aktiivisuus sekä AChE:tä että BuChE:tä kohtaan kuin 19:llä IC50-arvoilla 0,65 µM ja 5,73 µM [24]. Molekyylirakenteiden vertailussa tertiäärinen amiini on läsnä asemissa 7, 19 ja 20, ja se on vastuussa korkeasta sitoutumisaffiniteetista sekä AChE:tä että BuChE:tä kohtaan. Berberiinikloridi (21) ja 13-alkyyliberberiini (22) ovat kaksi isokinoliinialkaloidia, jotka ovat peräisin Coptis Chinensis -lajin juurakoista ja joilla on hieman erilaiset molekyylirakenteet kuin 19 ja 20. Vaikka molemmilla 21 ja 22 oli IC50 > 10 µM, kohti BuChE 21 osoitti voimakkaampaa inhiboivaa aktiivisuutta AChE:tä kohtaan IC50:llä 1,1 µM kuin 22:lla, jonka IC50 oli 5,6 µM [25]. Vertaamalla molempien alkaloidien molekyylirakenteita nähdään, että metyyliryhmän läsnäolo asemassa 13 rakenteen 22:ssa on vastuussa sekä AChE:n että BuChE:n alentuneesta inhiboivasta aktiivisuudesta.
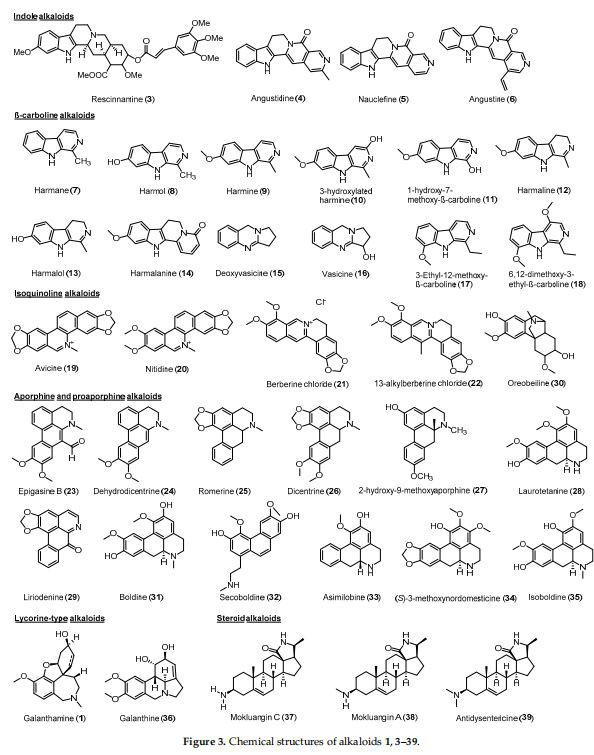
Aporfiini- ja proaporfiinialkaloidit ovat luonnollisesti peräisin isokinoliinista. Yleensä ne jakautuvat Annonaceae-, Lauraceae-, Magnoliaceae- ja Menispermaceae-heimoihin [39]. Stephania Epigaea [26], Illigera aromatic [40], Beilschmiedia sp. [27], Monimiaceae ja Magnoliaceae [41] johtivat sarjan aporfiini- ja proaporfiinityyppisiä alkaloideja eristämiseen. Niistä epinastiini B (23), dehydrodisentriini (24), romaine (25), oppi (26), 2-hydroksi-9-metoksiaporfiini (27), laurotetaniini (28), liriodeniini (29), oreobeliinillä (30), boldiinilla (31), sekoboldiinilla (32), asimilobiinilla (33), (S)-3-metoksinordomestiinilla (34) ja isoboldiinilla (35) on raportoitu olevan merkittäviä AChE:tä estäviä vaikutuksia [26,27] .
Lykoriinityyppiset alkaloidit, jotka tunnetaan myös nimellä Amaryllidaceae-alkaloidit, kuuluvat suureen isokinoliinialkaloidien ryhmään. Niitä löytyy Amaryllidaceae-heimon kasveista. Useita lykoriinityyppisiä alkaloideja on eristetty, enimmäkseen sipuliin ja lehtiin [42]. Lykoriinityyppiset alkaloidit, mukaan lukien galantiini (36) ja 1 Zephyranthes carinatasta, osoittivat AChE:tä estävää aktiivisuutta AChE:tä vastaan [28].
Steroidialkaloidit ovat yksi tärkeimmistä kasveista peräisin olevien alkaloidien luokista. Niillä on emäksinen steroidirunko, jonka renkaassa tai sivuketjussa on typpiatomi [43]. Kolmella uudella Holarrhena pubescensin steroidialkaloidilla Mokluangins A–C (37–39) ilmoitettiin olevan AChE:tä estävää aktiivisuutta alueella 1,44–4,09 µM, joissa substituutio C-3:ssa toimii avaimena AChE:n moduloinnissa inhiboiva vaikutus [29]. Isosteroidiset alkaloidit ovat yksi edustavista steroidaalisista alkaloideista, jotka kuuluvat C-27-runkotyyppiin [43]. Seitsemän Fritillaria walujewiin isosteroidialkaloidia (40–46) raportoitiin niiden mahdollisen koliiniesteraasia estävän vaikutuksen vuoksi. Tortifoliini (40), Walujewine C (41), Sinpeinine A (42), Walujewine A (46) ja Walujewine E (44) inhiboivat AChE:tä IC50-arvoilla 5,8-9,8 µM, kun taas kaikkien yhdisteiden osoitettiin estävän BuChE alle 10 uM paitsi 46. Voidaan päätellä, että kaikki yhdisteet ovat kaksoiskoliiniesteraasi-inhibiittoreita paitsi 43, 45 ja 46 [30].

vesisäiliö myytävänä
Pyrroloiminokinonialkaloidit eristetään pääasiassa meren eliöistä. Tärkeitä pyrroloiminokinonialkaloideja ovat diskorhabdiinit, ennuste, bazillionit, wakayiinit ja kamaronit [44]. Diskorhabdiinit G (47) ja B (48) Antarktiselta Latrunculia sp. sienet osoittivat AChE:tä estäviä aktiivisuuksia IC50-arvoilla 1,3 ja 5,7 µM, vastaavasti [31]. Lycopodium-alkaloidit ovat mielenkiintoinen alkaloidien luokka, jota esiintyy yleisesti Lycopodiaceae-kasveissa. Ne koostuvat kinolitsiini-, pyridiini- ja -pyridonityyppisistä alkaloideista [45]. Yleensä lykopodiumalkaloidit koostuvat C16-rungoista ja joskus niillä on C32-runkoja, kun ne esiintyvät dimeereinä [46]. Eristetyistä lykopodiumalkaloideista hupertsiini A (2) on esiintynyt tunnetuksi AChE-estäjänä AD:n hoidossa [45]. Squarroosi A (49) ja pyrrolhupertsiini A (50) eristettiin uusina Lycopodium-alkaloideina Huperzia squarrosasta yhdessä tunnetun 2- ja 12-epilykodoliini-N-oksidin (51) kanssa. Löydösten perusteella hupertsiini A oli tehokkain AChE:n esto, jota seurasivat 49, 50 ja 51 [32]. Samassa kasvissa tehdyssä jatkotutkimuksessa H. squarrosa tuotti 52 uutena lykopodiumalkaloidina, jolla oli AChE:n estopotentiaali [33].
Lykodiinityyppiset alkaloidit kuuluvat lykopodiumalkaloidien luokkaan. Yleensä ne koostuvat neljästä renkaasta, mukaan lukien yksi pyridiini- tai pyridiinirengas. Lykodiinityyppisten alkaloidien on tiedetty osoittavan AChE:tä estävää aktiivisuutta [46]. Lycopodiastrum casuarinoides -lajin lykodiinityyppisillä alkaloideilla, mukaan lukien Lycocasuarinine D (53), Lycocasuarinine A (54), N-demetyylihupertsiniini (55) ja hupertsiini C (56), tehdyssä tutkimuksessa niiden raportoitiin koliiniesteraasin estopotentiaalistaan. 50 ja 51 osoittivat AChE-inhibitiota IC50-arvoilla 0,22 ja 4,74 µM, kun taas 55 ja 56 olivat kaksoiskoliiniesteraasi-inhibiittoreita [34].
Flavoalkaloidit ovat ainutlaatuinen alkaloidien alaluokka, joka koostuu flavonoidien perusrungosta, jotka on fuusioitu typpeä sisältäviin renkaisiin, kuten pyrrolidinoni, pyrrolidiini, indoli, piperidiini, piperidiini ja aminoglykosidi [47]. Tähän mennessä on raportoitu alle 100 luonnossa esiintyvää makukeloidia, vaikka niillä on havaittu olevan laaja valikoima bioaktiivisuutta [35,47]. Äskettäisessä tutkimuksessa Camellia sinensiksestä eristettiin viisi uutta cinnamoyloitua makukeloidia. Yhdisteet tunnettiin nimellä 3-O-cinnamoyylilepikatekiini (57), (−)-6-(5"' S)
N-etyyli-2-pyrrolidinoni-3-O-cinnamoyylilepikatekiini (58), (−)-6-(5"'R)-N-etyyli-2-pyrrolidinoni{{1{{ 30}}}} O-kannamoyylilepikatekiini (59), (-)-8-(5"'S)-N-etyyli-2-pyrrolidinoni-3-O-kannamoyylilepikatekiini (60) ja (- )-8-(5"'R)-N-etyyli-2-pyrrolidinoni-3-O-cinnamoyylilepikatekiini (61). Kaikki makukeloidit osoittivat merkittävää AChE:tä estävää aktiivisuutta IC50-arvon ollessa 0,126-1,040 µM Tutkimus paljasti, että C-6-asema oli ratkaiseva AChE:tä inhiboivissa aktiivisuuksissa [35].
3. Alkaloidien monikohdemodulaatiopotentiaali neurodegeneratiivisissa sairauksissa
Vuosikymmenien ajan tutkijat ovat keskittyneet voimakkaasti sellaisten lääkkeiden löytämiseen, jotka voivat mahdollisesti muuttaa hermoston rappeutumissairauksien etenemistä, esimerkiksi Alzheimerin taudin amyloidihypoteesiin perustuvien sekretaasi-inhibiittorien löytämiseen. Valitettavasti yksikään ehdokkaista ei ole osoittanut lupaavia tuloksia, jotka parantaisivat taudin etenemistä kliinisten tutkimusten viimeisessä vaiheessa. Koliiniesteraasi-inhibiittorit ovat säilyneet lääkkeinä taudin hallinnassa, ja lisätutkimuksia kehotetaan tutkimaan alkaloidien potentiaalia neurodegeneratiivisten tilojen hoidossa niiden koliiniesteraasiaktiivisuuden lisäksi [48]. Huolimatta tehokkaista koliiniesteraasin vastaisista ominaisuuksista, jotka auttavat parantamaan kognitiivista toimintaa, olemme tehneet haun taulukon 1 alkaloideista, joilla on potentiaalista koliiniesteraasia estävää vaikutusta, ja koonnut useita tutkimuksia, jotka ovat raportoineet näiden alkaloidien potentiaalista vaikuttaa useisiin muihin kohteisiin. antaakseen yleiskuvan näiden yhdisteiden monikohdemodulaatiopotentiaalista. Ei kuitenkaan voida sulkea pois sitä, että yhdisteet, joilla on vähemmän koliiniesteraasia estäviä aktiivisuuksia, eivät ole mahdollisesti käyttökelpoisia joillekin muille hermosolujen rappeutumissairauksien kohteille. Tämä osio keskittyy pääasiassa Alzheimerin tautiin (AD) ja Parkinsonin tautiin (PD). Joukko mekanismeja, joihin nämä alkaloidit vaikuttavat, sisältää hermosolujen suojauksen, hermoston tulehduksen, neurogeneesin, amyloidi-beeta-aggregaation (A) ja tau-hyperfosforylaation.
3.1. Neurosuojaus
Neuroprotektio hidastaa hermosolujen häviämistä ja myöhempää hermostoa rappeutuvien sairauksien etenemistä useiden eri reittien kautta, mukaan lukien oksidatiivisen stressin, mitokondrioiden toimintahäiriön, proteiinien aggregaation, tulehduksen, eksitotoksisuuden ja soluapoptoosin vähenemisen [49].
Useat tutkimukset ovat osoittaneet, että harmane (7), harmol (8), harmiini (9), harmaliini (12) ja harmaloli (13) kuuluvat indoli-karboliinien luokkaan (taulukko 1), ja niillä on hermoja suojaava potentiaali hermosolujen vaurioita vastaan. In vitro -tutkimus osoitti, että 7 suojaa H2O2--indusoitua toksisuutta vastaan neuroblastoomasoluissa heikentämällä solujen elinkelpoisuutta [50]. Tämä malli liittyy neurodegeneratiivisten sairauksien kehittymiseen liittyvän oksidatiivisen stressin aiheuttamiin hermosoluvammoihin.
12:ta käytetään laajalti vapinaan jyrsijöillä, pelkästään dopaminergisiin PC12-soluihin ei havaittu negatiivista vaikutusta pitoisuudella 50 µM, samoin sen metaboliitilla harmalolilla 13 [51]. Tulos on sama kuin kaksi muuta tutkimusta, jotka osoittivat, ettei PC12-soluihin kohdistunut toksisuutta pelkästään 12:lla ja 13:lla [52,53]. MPP plus on neurotoksiini dopaminergisille hermosoluille, jotka ovat osallisia Parkinsonin taudissa (PD). 7:n rooli 1-Metyyli-4- fenyylipyridiniumin (MPP plus ) vaikutusten tukahduttamisessa saavutetaan estämällä mitokondrioiden transmembraanipotentiaalia (MMP), sytokromi c:n vapautumista, kaspaasin-3 aktivaatiota ja reaktiivisia happilajeja ( ROS) ja GSH-tasot In vitro [51–53]. Dopamiinin hapettuminen käynnistää erilaisia kaskadeja muodostaen endogeenisiä hermomyrkkyjä, jotka edistävät hermoston rappeutumista [54,55]. 12:n tapauksessa sen osoitettiin kompensoivan dopamiinin hapettumisen myrkyllisiä vaikutuksia aivojen mitokondrioihin ex vivo. Tämä johtuu 12:n antioksidanttisista ominaisuuksista, koska se ylläpitää tioredoksiinireduktaasiaktiivisuutta ja estää tiolin hapettumista ja siten dopamiinin hapettumistuotteiden muodostumista [56]. Lisäksi 9 ja 12 antioksidanttientsyymiä, kuten superoksididismutaasia [57] ja glutationiperoksidaasia (GPx) säädelivät in vitro, kun taas muissa tutkimuksissa ne vähensivät ROS:n nousua ja tiolin hapettumista, mikä johti tehostettuun antioksidanttipuolustusmekanismiin hermoja suojaavan vaikutuksen aikaansaamiseksi. [52,53,58,59].
Lisäksi 9:llä oli hermostoa suojaavia vaikutuksia säätelemällä glutamaatin kuljettaja-1 (GLT-1) proteiinitasoja sekä GLT-1- ja glutamaattiaspartaattikuljettaja (GLAST) -riippuvaista glutamaatin ottoa astrogliasoluissa ja SOD1G93A-hiirten kortikaalinen kudos, amyotrofisen lateraaliskleroosin siirtogeeninen hiirimalli [60]. Nämä glutamaattikuljettajat ylläpitävät glutamaatin, joka on eksitatorinen hermovälittäjäaine, alhaisen ekstrasellulaarisen pitoisuuden, jolloin sen kertyminen edistää eksitotoksisuutta [61]. Lisäksi äskettäinen systemaattinen katsaus osoitti, että 9 paransi muistia ja oppimista ja osoitti neuroprotektiivisia vaikutuksia hippokampukseen prekliinisissä kokeellisissa malleissa [62]. Sen väitetään osallistuneen GLT{11}}:n nousuun, ROS:n vähenemiseen, aivoperäisen neurotrofisen tekijän (BDNF) nousuun, ja sillä oli anti-inflammatorisia vaikutuksia. PD:n yhteydessä 9:ää tutkittiin äskettäin sen hajoamisvaikutuksen suhteen -synukleiiniin in vitro. Ubikitiini-proteasomijärjestelmä (UPS) on yksi järjestelmistä, joka poistaa synukleiinia proteasomin proteolyyttisen aktiivisuuden kautta, ja osoitettiin, että 9 lisäsi proteolyyttistä aktiivisuutta proteiinikinaasi A:n (PKA) fosforylaation kautta ja näin ollen tehosti UPS:ää synukleiinin puhdistumaan [63, 64].
13, 9:n metaboliitti, sisällytettiin aiemmin mainittujen tutkimusten tuloksiin kiinnostavana yhdisteenä, ja havaittiin, että 13 tarjosi hermosuojaa moduloimalla oksidatiivista stressiä, MMP:tä ja apoptoosia in vitro [51–53]. Nämä havainnot osoittivat ROS:n ja tiolin hapettumisen vähenemistä, GSH-tasojen nousua ja MMP-häviön heikkenemistä [51–53,65]. Myös 13:n vaikutusta kahteen solukuoleman välittämiseen liittyvään prosessiin, joka on sytokromi c:n vapautuminen ja kaspaasi-3 aktivaatio, tutkittiin, ja 13 vähensi molempia [51,66].
Berberiinikloridin (21), joka on isokinoliinialkaloidi (taulukko 1), suojaavista vaikutuksista hermoston rappeutumiseen liittyvä tutkimus on yleistynyt viime vuosina. In vivo -tutkimuksessa 21:n esikäsittely 6-hydroksididopamiinilla (6-OHDA) stimuloimalla neurotoksisuudesta, joka mallintaa PD:tä rotilla, vähensi merkittävästi apomorfiinin aiheuttamia rotaatioita ja Nissl-värjätyn substantia nigra pars compactan ( SNpc) hermosoluja, ja heikensi tyrosiinihydroksylaasi-immunoreaktiivisuuden vähenemistä SNpc-dopaminergisissä neuroneissa [67]. In vitro -tutkimus osoitti, että 21:llä oli hermostoa suojaavia ominaisuuksia oksidatiivisen stressin välittämää hermoston rappeutumista vastaan aktivoimalla Akt/GSK-, Akt/GSK3 /Nrf{12}}- ja PI3K/Akt/Nrf2-signalointikaskadeja, lisäämällä p-CREB:tä, stimuloimalla NGF:ää ja BDNF:n vapautuminen, NF-κB:n tuman translokaatio vähentäminen, TNF:n, COX-2, IL-1B, NF-κB:n suppressoiminen ja kaspaasin-1, kaspaasin-3, Baxin alentaminen, Bcl-2 nousu, sykliini D1 ja p53 [68]. Aiempien tutkimusten tulosten lisäksi Deng ja ryhmä raportoivat 21:stä vähentyneestä ROS-tuotannosta ja käänteisestä MMP-vähennyksestä in vitro, ja ehdottivat, että 21:llä oli neuroprotektiivisia vaikutuksia PI3K/Akt-reitin aktivaatiolla rotenonin aiheuttamassa neurotoksisuudessa [69]. 21:n osoitettiin myös suojaavan PC-12-soluja oksidatiivisilta vaurioilta PI3K/AKT/mTOR-välitteiseltä mitofagialta [70]. Wallerian kaltainen rappeuma (WLD) on aksonin rappeuma, joka ulottuu distaalisesta aksonista vauriokohtaan ja esiintyy hermoston rappeumasairauksissa [71]. Mielenkiintoista on, että 21:n havaittiin olevan ei-kilpaileva inhibiittori steriiliä alfaa ja toll-interleukiinireseptorimotiivia sisältävälle proteiinille 1 (SARM1), joka on keskeinen WLD:n välittäjä, ja tuottaa 70 prosentin eston ensisijaisesta seulonnasta [72]. . Samassa tutkimuksessa testattiin edelleen sen estoaktiivisuutta bakteeri- ja Expi293-solujen SAM1-2TIR-domeenilla löydösten vahvistamiseksi ja saatiin vastaavasti IC50-arvot 110 ± 10 µM ja 77 ± 5 µM. Lisäksi 21 lisäsi CYP2J2:ta, proteiinia, jonka havaittiin suojaavan PD-mallia vastaan, stimuloimalla peroksisomiproliferaattori-aktivoitua reseptoria alfaa (PPAR-) in vitro [73]. In vivo -tutkimus osoitti, että 21 esti aminolevuliinihappodehydrataasin (δ-ALA-D) eston ja purinergisen transmission vaurioitumisen heikentämällä NTPDaasi-, ADP-, 50 -nukleotidaasi- ja ADA-aktiivisuuden menetystä streptotsotosiinin aiheuttamassa dementiassa, jossa tämän lähetyksen säätelyllä on rooli muistin käsittelyssä [74,75]. Kuitenkin δ-ALA-D-aktiivisuus spesifisissä hermosoluissa vaatii lisätutkimuksia saatavilla olevien tutkimusten rajallisuuden vuoksi.

vesisäiliö myytävänä
Glian puolikanavan aktiivisuuden stimulaatio tehostaa ATP:n ja glutamaatin vapautumista, mikä myöhemmin aiheuttaa hermosolujen kuoleman, kun taas retikuloni-3 (RTN3) aggregoituu AD-aivoissa ja helpottaa dystrofisten neuriittien kehittymistä [76,77]. Boldiinin (31), aporfiinialkaloidin (taulukko 1), ilmoitettiin vähentävän astroglian hemikanavan aktiivisuutta vaikuttamatta aukon liitosviestintään, mikä vähentää ATP:n ja glutamaatin vapautumista. In vivo -tutkimus osoitti, että 31 oli suojattu hermosolujen oksidatiiviselta stressiltä ja amyloidi-beeta (A ) -plakkeja ympäröiviltä neuriittisilta dystrofioilla, joissa APP/PS1-hiirissä havaittiin pienempiä ja harvempia alueita RTN3-immunoreaktiivisia dystrofisia neuriitteja (RIDN:t) [78]. Toisessa tutkimuksessa 31 hajotti H2O2:ta, vähensi raudan ja EDTA:n välittämää deoksiriboosin hajoamista ja melaniinin muodostumista dopamiinihapetuksen vaikutuksesta, heikensi MMP:n menetystä, sytokromi C:n nousua, tioredoksiinireduktaasiaktiivisuuden menetystä, esti tiolin hapettumista ja {{15}dopamiinin aiheuttamaa }OHDA- ja PC-12-solujen elinkelpoisuuden menetys ja dopamiinin aiheuttama kaspaasin-3 aktivaatio [79].
In vivo -tutkimus osoitti, että deoksivasisiini (15), joka on -karboliinialkaloidi (taulukko 1), suojasi hermosoluja oksidatiivisen stressin aiheuttamilta vaurioilta annoksella 15 mg kg-1. Tutkimus osoitti, että glutationiperoksidaasin (GPx) määrä nousi merkittävästi 15 peroksidaasin antamisen jälkeen, mikä tehosti aivojen antioksidanttista puolustusmekanismia. Lisäksi 15 kykeni parantamaan hermojen selviytymistä nostamalla aivoperäistä neurotrofista tekijää (BDNF) 45 mg:aan kg-1 [80].
3.2. Hermoston tulehdus
Vuosien varrella on tehty tutkimuksia hermostoa rappeutuvien tilojen patologian selvittämiseksi, ja hermotulehduksen on havaittu olevan yksi taustalla olevista mekanismeista. Vika immuunisolujen toiminnassa voi käynnistää tulehduksen keskushermostossa (CNS) ja lopulta aiheuttaa hermovaurion. Erityisesti akuutti tulehdus voi olla hyödyllistä aivoille. Sitä vastoin krooninen tulehdus voi vahingoittaa aivoja edistämällä tau-proteiinin hyperfosforylaatiota ja amyloidi-beeta (A) -aggregaatiota. Näitä mekanismeja voivat aktivoida proinflammatoriset välittäjät, kuten interleukiini 1 (IL-1) ja interleukiini 6 (IL-6). Koska tulehdus liittyy läheisesti neurodegeneratiivisten tilojen, kuten AD:n ja PD:n, patologiaan, alkaloidit, jotka pystyvät estämään hermoston tulehduksen, saattavat pystyä lievittämään hermoston tulehdusta sekä auttamaan sairauksien hallinnassa [81–83].
9 ja 12 korostettiin kykeneviksi torjumaan hermotulehdusta. Ehdotettiin, että ne pystyivät vähentämään tulehduksellisten sytokiinien, kuten tuumorinekroositekijä-alfan (TNF-) ja myeloperoksidaasin (MPO) ja välittäjien, kuten typpioksidin (NO), tuotantoa. Erityisesti 7 ja 12 osoittivat IC50-arvoa 0,08 µM ja 0,26 µM MPO:ta kohtaan, mikä osoitti niiden potentiaalin sisällyttää hermotulehduksia ehkäisevänä aineena [58, 59]. Lisäksi in vivo -tutkimus ehdotti, että 9 paransi merkittävästi kognitiivisia puutteita kemiallisesti indusoiduilla diabeettisilla rotilla annoksella 20 mg kg-1. Tutkimuksessa ehdotettiin, että diabetes mellitus liittyi läheisesti kognitiiviseen toimintahäiriöön ja molemmat liittyivät tulehdukseen. Kun 9:ää annettiin diabeettisille rotille, NLRP3-tulehdusaktiivisuus vaimeni, mikä johti aivoperäisen neurotrofisen tekijän (BDNF) ilmentymisen lisääntymiseen ja myöhemmin kognitiivisten kykyjen paranemiseen [84]. Lisäksi in vivo -tutkimus raportoi, että 9 kykeni myös ylittämään veri-aivoesteen (BBB) pian suun kautta ottamisen jälkeen [85].
Toinen -karboliinialkaloidi 15 kykeni estämään hermotulehduksen useiden reittien kautta. In vivo -tutkimus oli osoittanut, että 15 kykeni lisäämään -GABA:n määrää ja vähentämään glutamaatin määrää aivoissa pitoisuuksilla 5 1, 15 ja 45 mg kg-1. -GABA on elintärkeä välittäjäaine, joka estää astrosyyttien ja mikroglian käynnistämää hermotulehdusta estämällä TNF-:n vapautumisen. Lisäksi TNF-:n, joka on tulehdusta edistävä sytokiini, tuotanto väheni myös merkittävästi pitoisuudesta riippuvaisessa mallissa, kun sitä käsiteltiin 15:llä pitoisuuksina 5–45 mg kg-1 [80].
21 vaikuttaa useisiin kohteisiin AD-olosuhteiden parantamiseksi. Yksi 21:n vaikutusmekanismeista on heikentää hermoston tulehdusta [86]. Esimerkiksi in vivo -tutkimus raportoi pro-inflammatoristen välittäjien, mukaan lukien COX-2, IL-12, IL-6, IL-1 ja TNF:n vähenemisen. 21:n antaminen AD-rotan aivoihin [87]. Lisäksi in vivo -tutkimus raportoi, että 21 esti p65-alaosan ilmentymistä ja fosforylaatiota annoksella 50 mg kg-1. p65 on osa NF-KB-heterodimeeriä, joka on elintärkeä tulehdusproteiinituotannon moduloinnissa [88]. Lisäksi in vivo -tutkimus raportoi myös, että 21 pystyi estämään hermoston tulehdusta tukahduttamalla IL-6-, TNF- ja p38-MAPK-signalointikaskadeja [89].
3.3. Neurogeneesi
Aikuisten neurogeneesi on prosessi, joka tapahtuu hippokampuksen subgranulaarisella vyöhykkeellä (SGZ) ja subventrikulaarisella vyöhykkeellä (SVZ) hermosolujen tuottamiseksi koko ihmisen eliniän ajan. Vika aikuisen neurogeneesissä voi mahdollisesti johtaa hermostoa rappeutuviin tiloihin, kuten Alzheimerin tautiin (AD), Parkinsonin tautiin (PD) ja Huntingtonin tautiin (HD) [90]. Esimerkiksi in vivo -tutkimus raportoi, että aikuisen neurogeneesin heikkeneminen on saattanut alkaa AD-taudin varhaisessa vaiheessa jo ennen neurotoksisten neurofibrillisten vyyhtymien ja A-plakkien muodostumista [91,92].
In vitro -tutkimus ehdotti, että 8, 9 ja 12 indusoivat onnistuneesti neurogeneesiä, kun niitä testattiin SGZ:stä ja SVZ:stä viljellyillä esisoluilla. Lisäksi 9:n aineenvaihdunta ihmiskehossa tuotti 8:aa päätuotteena. Nämä -karboliinialkaloidit kykenivät myös indusoimaan hermosolujen erikoistumista, ja tämä todistettiin MAP-2- ja Tuj-1-ilmentymisellä. Tutkimus ehdotti, että näiden -karboliinialkaloidien neurogeneesipotentiaali johtui niiden monoamiinioksidaasia [70] ja DYRK1A:ta [93] estävästä vaikutuksesta.
In vitro -tutkimus, jossa tutkittiin aporfiinialkaloidien neurogeneesipotentiaalia (taulukko 1) PC-12-soluissa, osoitti, että asimilobiini (33) stimuloi merkittävästi neuriitin kasvua PC-12-soluissa, mutta sillä ei ollut selvää vaikutusta mRNA-ekspressio, joka koodaa solun jakautumisen ja erikoistumisen kannalta välttämättömiä proteiineja. Lisäksi tutkimuksessa kerrottiin myös, että 33 läpäisi erittäin hyvin veri-aivoesteen (BBB), mikä tekee siitä mahdollisen lääkekandidaatin hermostoa rappeutuvien sairauksien hoitoon [94].
3.4. Amyloidibeetan aggregoituminen
Amyloidi beeta (A) on tuote, joka syntyy amyloidin esiasteproteiinin (APP) entsymaattisesta hajoamisesta -sekretaasin ja -sekretaasin vaikutuksesta, ja A:lla oletetaan olevan rooli AD:n kehittymisessä. A on peptidi, joka koostuu enimmäkseen 40–42 aminohaposta ja on herkkä aggregaatiolle muodostaen neurotoksisia A-plakkeja. Kun A-plakit kerääntyvät aivoihin, kehittyy epänormaalia synaptista ja hermoston toimintaa, mikä aiheuttaa vaurioita aivoille ja aiheuttaa oireita, kuten kognitiivisia puutteita ja asteittaista muistin menetystä [95,96].
Siksi A:n aggregoitumisen estäminen voi auttaa viivästyttämään AD:n etenemistä. Kasviperäisten alkaloidien osoittaman antikoliiniesteraasiaktiivisuuden lisäksi jotkut niistä kykenevät estämään A-aggregaatiota. Neuvo (19) ja nisatidiini (20) ovat isokinoliinialkaloideja (taulukko 1) ja niillä on kyky estää A:n oligomeroitumista.
In vitro -tutkimus raportoi, että 19 ja 20 osoittivat kohtalaisen voimakasta suppressiota kohti A-aggregaatiota, mikä nähtiin niiden IC50-arvoista 5,56 ja 1,89 µM A:ta kohti. Itse asiassa ehdotettiin myös, että sekä 19:llä että 20:lla oli merkittävin estoaktiivisuus useisiin neurodegeneratiivisiin tiloihin osallistuviin kohteisiin ja niillä oli samanlaiset molekyylirakenteet verrattuna muihin Zanthoxylum rigidumista uutettuihin isokinoliinialkaloideihin. Siksi on rohkaistava tutkimaan molekyylirakennetta, joka liittyy niiden monikohdeaktiivisuuteen [24]. Lisäksi 21:tä on tutkittu vuosia, ja katsauksessa kerrottiin, että se esti ERK1/2:n ja mitogeeniaktivoidun proteiinikinaasin (MAPK) signalointikaskadeja, minkä seurauksena deaktivoi -sekretaasin-1 (BACE-1) ja pienenevä A-sukupolvi [86]. Itse asiassa 21:tä markkinoidaan käsikauppatuotteena, jota kulutetaan suun kautta Kiinassa, koska sen tehoa ja turvallisuutta suullisen nauttimisen jälkeen koskevat tutkimukset raportoivat hyväksyttävistä tuloksista. Paitsi antikoliiniesteraasiaktiivisuutensa, joka on verrattavissa 1:een ja 21:een, sillä oli myös kyky vähentää A-aggregaatiota vähentämällä A:n muodostumista. In vivo -tutkimus raportoi, että 21 kykeni estämään merkittävästi -sekretaasiaktiivisuutta AD-aivoissa, mikä vähentää A:n muodostumista jopa 40 prosenttia ja parantaa AD:n oireita. Sen lisäksi, että se suppressoi -sekretaasia, toinen in vivo -tutkimus raportoi, että 21 lisäsi A 40 -aktiivisuutta, mikä alensi A 42:n neurotoksista potentiaalia modifioimalla A 42:n stabiilisuutta, morfologiaa ja liukoisuutta heikentäen A 42 -aggregaatiota [87,97]. Tätä väitettä tukee myös in vivo -tutkimus, jossa väitettiin, että 21 kynsi pitoisuuksilla 50 ja 100 mg/kg/vrk alentamaan -sekretaasin Pen{40}}, Aph-1 ja PS1 osia. ja -sekretaasi, mikä siten tukahduttaa A:n tuotannon. Lisäksi 21:n osoitettiin lisäävän merkittävästi -sekretaasiaktiivisuutta samoilla pitoisuuksilla [98]. In vitro -tutkimus ehdotti lisäksi, että 21 kykeni estämään A:n oligomeroitumista ja fibrillien muodostumista [99].
3.5. Tau Hyperfosforylaatio
Tau-proteiinilla (τ) on tärkeä rooli hermosolujen mikrotubulusten stabiloinnissa ja siten hermosolujen rakenteen ja ravinteiden solunsisäisen kuljetuksen tukemisessa. Kinaasit, jotka sisältävät kaksoisspesifisen tyrosiinifosforylaatiosäädellyn kinaasi 1A:n (DYRK1A), glykogeenisyntaasikinaasin-3 (GSK-3), Ca2 plus /kalmoduliinin aktivoiman proteiinikinaasi II:n ja sykliinistä riippuvaisen kinaasin-5 (Cdk5) voi indusoida tau-hyperfosforylaation. Tau-proteiinin hyperfosforylaatio johtaa fosforyloituneiden tau-proteiinien paakkuuntumiseen muodostaen parillisen taun kierteisen filamentin neurofibrillaarisia vyyhtymiä. Tämän seurauksena ne eivät enää tue neuronin mikrotubuluksia, mikä lopulta johtaa hermosolujen apoptoosiin ja siten hermoston rappeutumiseen [100].
9:llä havaittiin olevan estäviä vaikutuksia DYRK1A:ta kohtaan, mikä puolestaan esti tau-proteiinin hyperfosforylaatiota. In vitro -tutkimuksessa osoitettiin, että 9 oli voimakas DYRK1A:n estäjä IC50-arvolla noin 80 nM. 9 deaktivoi DYRK1A:n, täten suppressoi tau-fosforylaatiota seriini 396:ssa, minkä jälkeen se vähentää tau-proteiinin kaikkia kolmea fosforyloitua muotoa. Vähentämällä fosforyloidun tau:n määrää, harmiini (9) säilytti tau:n toiminnan tukemaan mikrotubuluksia neuronissa, mikä esti hermosolujen kuoleman. Kuitenkin raportoitiin, että 9 voi olla neurotoksinen yli 8 µM pitoisuuksilla liiallisesta tau-proteiinin ehtymisestä johtuen [100].
9:n lisäksi 21 pystyi myös estämään tau-proteiinin hyperfosforylaatiota. Vaikka 21:n todellista mekanismia tau-hyperfosforylaation vähentämiseksi on tutkittava lisää, kaksi in vitro -tutkimusta on osoittanut, että 21 pystyy estämään kalykuliini A:n stimuloiman tau-proteiinin hyperfosforylaation pitoisuuksilla 20 ja 25 µg ml-1 vähentämällä GSK-3-aktiivisuutta ja lisäämällä proteiinifosfataasi 2A:n aktiivisuutta. Lisäksi 21 indusoi tau-fosforylaation kääntymisen Ser262:ssa [86, 101, 102]. In vivo -tutkimus raportoi myös, että 21:n antioksidanttiset ominaisuudet voisivat auttaa estämään tau-proteiinin yli-ilmentymistä ja tau-hyperfosforylaatiota AD-aivoissa [87].
4. Alkaloidien fysikaalis-kemiallinen analyysi
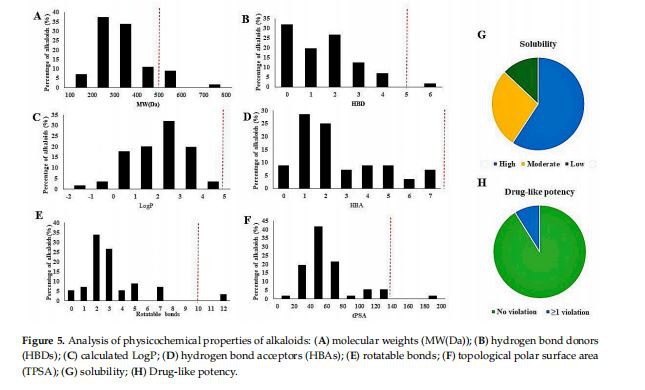
Kuvassa 5 on esitetty tähän katsaukseen sisältyvien alkaloidien fysikaalis-kemiallisten ominaisuuksien analyysi. Useimpien yhdisteiden molekyylipaino oli alle 500 Da. Suurempimolekyylipainoisia yhdisteitä olivat 44, 45 ja makualkaloidit (58–61). Vain yksi yhdiste rikkoo Lipinskin sääntöä vetysidoksen luovuttamisesta, pyörivistä sidoksista ja topologisesta polaarisesta pinta-alasta (TPSA). Mielenkiintoista on, että kaikki tähän katsaukseen sisältyvät yhdisteet noudattivat Log P:n ja vetysidoksen vastaanottajan (HBA) Lipinskin sääntöä. 32 yhdistettä luokiteltiin erittäin liukeneviksi, 15 yhdisteellä oli kohtalainen ja 7 yhdisteellä oli heikko liukoisuus.
5. Menetelmä
Kaikki luonnollisesti johdetut alkaloidit, joiden koliiniesteraasia estävä vaikutus kirjallisuudessa on raportoitu vuosina 2011–2020, sisällytettiin tähän tutkimukseen. Synteettiset alkaloidit, alkaloidit, jotka on alustavasti tunnistettu kaasukromatografia-massaspektrometrialla (GC-MS) ja nestekromatografia-massaspektrometrialla LCMS, jonka raportoitu olevan koliiniesteraasin esto, jätettiin tähän tutkimukseen pois. Kuvio 1 osoittaa, että 38 prosenttia ja 18,7 prosenttia AChE- ja BuChE-inhibiittoreista, joiden IC50 oli pienempi tai yhtä suuri kuin 10 uM, sisällytettiin tähän katsaukseen. Tämän seurauksena 61 yhdistettä, joiden IC50 on pienempi tai yhtä suuri kuin 10 µM, paitsi 1 ja 2, sisällytettiin tekstiin ja katsaukseen sairauden modifiointimahdollisuuksista mukaan lukien amyloidi-beetan esto, tau-hyperfosforylaatiota estävä, hermotulehdus, neurogeneesi ja hermostoa suojaava aine. tehosteita. 59 alkaloidin fysikaaliskemialliset ominaisuudet (paitsi galantamiini ja hupertsiini A) ennustettiin (Instant JChem 17.10.0, 2020 ChemAxon Ltd.).
6. Johtopäätökset
Kasvava määrä näyttöä on osoittanut luonnosta peräisin olevien alkaloidien merkityksen hermostoa rappeuttavien sairauksien modulaattoreina. Vaikka alkaloidit ovat pääasiallinen AChE-estäjien lähde, havaitaan huomattava määrä kaksoiskoliiniesteraasi-inhibiittoreita ja BuChE-estäjiä. On mielenkiintoista huomata, että useat tässä katsauksessa dokumentoidut alkaloidit suojaavat hermosoluja haitallisilta mekanismilta, kuten hermotulehdukselta, oksidatiiviselta stressiltä, eksitotoksisuudesta, apoptoosilta, A:n kertymiseltä ja tau:n fosforylaatiolta, ja niitä voitaisiin kehittää Alzheimerin ja Parkinsonin taudin hoitoon. Erityisesti 9 ja 21 ovat mahdollisia modulaattoreita näiden sairauksien etenemisen hallinnassa. Tästä huolimatta näiden alkaloidien annostelu hermostoa rappeuttavia sairauksia varten jäi epäselväksi. Fysikaalis-kemiallinen analyysi paljasti, että suurin osa alkaloideista noudattaa Lipinskin lääkkeiden todennäköisyyden sääntöjä. Veri-aivoeste on tärkeä tekijä, joka suojaa yhdisteiden tunkeutumista aivoihin, ja siihen on kiinnitettävä lisähuomiota. Luonnollisesti johdettujen yhdisteiden takaiskut, kuten alhainen uuttosaanto, ovat luonnollisesti pysäyttäneet mahdollisten ehdokkaiden kehittymisen terapeuttisiksi johdoksiksi. Lisäkehitystä tarvitaan niiden käyttökelpoisuuden parantamiseksi elinkelpoisina terapeuttisina lääkkeinä.
