Hypoksian aiheuttaman tekijän 1 yli-ilmentyminen hidradenitis suppurativassa: yhteys poikkeavan immuniteetin ja aineenvaihdunnan välillä
Jun 07, 2023
Abstrakti
Hypoksian aiheuttama tekijä-1 (HIF-1) on glykolyysin, Th17-solujen erilaistumisen ja säätelevien T-solujen suppression tärkein transkriptiotekijä. Psoriaasi vulgarista sairastavien potilaiden ihossa ja seerumissa on raportoitu lisääntynyttä HIF-1:n ilmentymistä, kun taas HIF-1:n ilmentymistä ihossa ja seerumissa potilailla, joilla on märkivä hidradenitis (HS) ei ole vielä tutkittu . Tutkimuksen tavoitteena on osoittaa, onko HIF:llä-1 merkitystä hidradenitis suppurativan patogeneesissä ja sen suhdetta HS:n vaikeusasteeseen. Tutkimukseen osallistui 20 potilasta, jotka kärsivät hidradenitis suppurativasta. Punch-biopsiat otettiin leesion iholta HIF-1-ekspression määrittämiseksi immunohistokemiallisella värjäyksellä ja HIF-1-geenin ilmentymisen määrittämiseksi kvantitatiivisella käänteistranskription reaaliaikaisella PCR:llä. HIF{10}}-proteiinipitoisuuden kvantifiointi tehtiin entsyymi-immunosorbenttimäärityksellä. Kaksikymmentä sosiodemografisesti ristiin soveltuvaa tervettä vapaaehtoista toimi kontrolleina.
Löysimme kohonneita seerumin HIF-tasoja-1. Kirjallisuudesta saatu näyttö osoittaa, että HS:n, liikalihavuuden ja tupakoinnin tärkeimmät kliiniset laukaisevat tekijät liittyvät hypoksiaan ja lisääntyneeseen HIF-1-ekspressioon. Pro-inflammatoriset sytokiinit, kuten tuumorinekroositekijä-a, lisäämällä ydintekijän 휅B:n säätelyä tehostavat HIF{5}}-ilmentymistä. HIF-1 näyttelee tärkeätä roolia keratinosyyttien lisääntymisessä, erityisesti anageenikarvatupen keratinosyyteissä, mikä vaatii runsasta glykolyysiä, jotta saadaan riittävästi esiastemolekyylejä biosynteettisille reiteille. Metformiini estämällä mTORC1:tä sekä adalimumabi heikentää HIF-1:n ilmentymistä, joka on tärkein välittäjä Th17--peräisen poikkeavan immuniteetin ja keratinosyyttien hyperproliferaation välillä. Psoriaasin perusteella tutkimuksemme tunnistaa HS:n HIF{10}}in aiheuttamaksi tulehdukselliseksi ihosairaudeksi ja tarjoaa uuden perusteen HS:n ehkäisyyn ja hoitoon kohdistamalla HIF{11}}yliilmentymiseen.
Kohonneet seerumitasot tarkoittavat yleensä sitä, että elimistö kehittää tiettyä immuunivastetta. Immuunijärjestelmä tuottaa vasta-aineita hyökkäämään patogeenejä, kuten viruksia ja bakteereja vastaan, jotka tunkeutuvat elimistöön. Kun keho altistuu taudinaiheuttajille, immuunijärjestelmä tunnistaa ja tuottaa vasta-aineita, jotka vapautuvat veressä ja hyökkäävät taudinaiheuttajia vastaan ja estävät niitä tartuttamasta kehoa edelleen.
Kohonneet seerumipitoisuudet voivat siten viitata siihen, että immuunijärjestelmä toimii puolustautuessaan tunkeutuvia taudinaiheuttajia vastaan. Liian korkeat seerumipitoisuudet voivat kuitenkin johtaa myös ongelmiin, kuten autoimmuunisairauksiin. Siksi seerumitasojen ja immuniteetin välistä suhdetta tutkittaessa on otettava huomioon useita tekijöitä ja tehtävä kattava arviointi. Siksi meidän on kiinnitettävä huomiota vastustuskyvyn parantamiseen. Cistanche voi parantaa merkittävästi immuniteettia. Cistanche sisältää runsaasti erilaisia antioksidantteja, kuten C-vitamiinia, karotenoideja jne. Nämä ainesosat voivat poistaa vapaita radikaaleja, vähentää oksidatiivista stressiä ja parantaa vastustuskykyä. järjestelmän vastus.

Napsauta cistanchen terveyshyötyjä
Avainsanat
Glykolyysi · Hidradenitis suppurativa · Hypoksian aiheuttama tekijä 1 · Keratinosyyttien lisääntyminen · Th17-solut.
Johdanto
Hidradenitis suppurative (HS) on krooninen vammauttava tulehduksellinen ihosairaus, jolle on tunnusomaista kivuliaita, syvälle istuvia kyhmyjä, paiseita, poskionteloita ja arpia, joiden etiopatogeneesi on vielä epävarma [1, 2]. Suurin osa HS-potilaista on satunnaisia tapauksia, kun taas familiaalinen HS on ollut vastaavasti 3,2–35,8 prosenttia HS-potilaista [3, 4]. Kliiniset kokemukset osoittavat, että HS laukaisee ympäristöön kohdistuvat loukkaukset geneettisesti alttiilla yksilöillä. Liikalihavuus ja tupakointi ovat tärkeimpiä laukaisevia tekijöitä [5]. Rapamysiinikompleksi 1:n (mTORC1) mekaanisen kohteen lisääntynyttä aktiivisuutta on havaittu HS:n [6], psoriaattisen epidermiksen [7, 8], liikalihavuuden ja diabetes mellituksen [9, 10] iholla, ja sitä pidetään mahdollisena yhteys aineenvaihdunnan ja immuniteetin poikkeamien välillä HS:ssä [11–13].
Erityisesti hypoksian aiheuttama tekijä -1a (HIF-1a) on mTORC1:n alavirran efektori [14]. mTORC1:n yliaktivoituminen ajaa Th17-solujen indusoimaa interleukiini 17:n (IL-17) ilmentymistä [15, 16]. IL-17-reitillä on keskeinen rooli HS:n ja psoriaasin patogeneesissä [17–21]. HS:lle on ominaista Th17- ja säätelevien T (Treg) -solujen [21] säätelyhäiriö, jota havaitaan myös muissa HS:n autoimmuunisairauksissa [19]. Erityisesti HIF-1 edistää suoraan Th17:n kehitystä aktivoimalla transkriptionaalisesti retinoiinihappoon liittyvää orporeseptoria t (ROR t), joka on tärkeä transkriptiotekijä, joka ohjaa Th17-solujen erilaistumista [22, 23]. Sitä vastoin HIF-1 rajoittaa Treg-solujen erilaistumista ja toimintaa sitoutumalla FoxP3:een ja kohdistaa sen hajoamiseen [22, 23]. HIF-1 näyttelee keskeistä roolia tulehduksen aineenvaihdunnan uudelleenohjelmoinnissa [24] ja säätelee makrofagien, neutrofiilien ja dendriittisolujen aktivaatiota luoden tulehdusta edistävän mikroympäristön autoinflammatorisissa leesioissa [25].
HIF-1 on hypoksian ja glykolyysin tärkein transkriptiotekijä [26, 27]. Glykolyysi on ensisijainen energialähde ja biosynteettisten esiasteiden saatavuus voimakkaasti lisääntyville soluille, mukaan lukien Th17-solut [28], psoriaattiset keratinosyytit [29, 30] ja anageeniset karvatuppisolut [31–33]. HS:n perilesionaalisella iholla on lievä psoriaasia muistuttava hyperplasia [34]. HS:ssä on havaittu ulomman juuritupen keratinosyyttien liiallista proliferaatiota [35, 36].
HIF{0}}:n lisääntynyt ilmentyminen on havaittu psoriaasi [37, 38] ja muita Th17-välitteisiä tulehdussairauksia [25] sairastavien potilaiden ihosta ja seerumista. HS:n mukaan liikalihavuus ja tupakointi ovat psoriaasia edistäviä tekijöitä [39, 40]. Siksi mietimme, onko HIF-1 yli-ilmentynyt myös HS-potilaiden ihossa ja seerumissa ja voiko HIF-1 liittää liikalihavuuden ja tupakoinnin Th17-soluvetoisiin immuniteetin ja infundibulaaristen keratinosyyttien hyperproliferaatioon.
Materiaalit ja menetelmät
Potilaat
Tähän tutkimukseen osallistui 20 potilasta, jotka kärsivät hidradenitis suppurativasta, ja 20 sosiodemografisesti ristiin soveltuvaa tervettä kontrollia. Kaikki osallistujat rekrytoitiin Alexandrian yliopistollisen sairaalan ihotautipoliklinikalta. Kaikilta potilailta ja kontrolleilta saatiin eettisen komitean hyväksyntä sekä kirjallinen tietoinen suostumus. Kaikki toimenpiteet olivat instituution ja/tai kansallisen tutkimuskomitean eettisten standardien ja vuoden 1964 Helsingin julistuksen mukaisia ja rekisteröity IRB-numerolla: 00012098, FWA:n numero: 00018699. Potilaat, joilla oli muita samanaikaisia vaurioita sairastuneella alueella, potilaat, jotka olivat jotka olivat saaneet HS-hoitoa viimeisen 6 kuukauden aikana, ja raskaana olevat ja imettävät naiset jätettiin pois. Potilaille tehtiin täydellinen historia ja yleinen lääketieteellinen ja dermatologinen tutkimus. HS:n vakavuus arvioitiin Hurley-järjestelmällä: vaihe I: yksittäinen tai moninkertainen, eristetty absessin muodostuminen ilman arpia tai poskionteloita; vaihe II: toistuvat paiseet, yksittäiset tai useat toisistaan erillään olevat vauriot, joihin liittyy poskionteloalueen muodostumista; vaihe III: diffuusi tai laaja vaikutus, jossa on useita toisiinsa liittyviä poskionteloputkia ja paiseita [41].
Ihon biopsia
Toimenpide selitettiin kaikille potilaille. Potilaiden ihovauriosta otettiin yksi 5 mm:n lyöntibiopsia (immunohistokemiallista tutkimusta varten) ja kaksi 2,5 mm:n lyöntibiopsiaa (ELISAa ja PCR:ää varten). Kolme 5 mm:n biopsiaa normaalista ihosta otettiin plastiikkakirurgian osastolta rekrytoiduilta kontrollihenkilöiltä, joille tehtiin kirurgisia toimenpiteitä nivusalueella.
Histopatologia ja immunohistokemia
Kaikki näytteet valmistettiin immunohistokemiallista värjäystä varten käyttämällä hiiren monoklonaalista monoklonaalista HIF-1-vasta-ainetta [42]. Immunohistokemiallinen värjäys suoritettiin leimatulla streptavidiini-biotiinikompleksimenetelmällä. Ensisijainen vasta-aine: HIF-1 -vasta-aine (Affinity Biosciences cat # AF1009), streptavidiini-HRP-konjugaatti (Epredia™ UltraVision Quanto Detection HRP DAB-Cat# TL-060-QHD) valmistettiin valmistajan ohjeiden mukaan DAB-työliuos valmistettiin toimitetusta DAB-varastoliuoksesta (Epredia™ UltraVision Quanto Detection HRP DAB–Cat# TL-060-QHD) pitoisuutena 1 mg/ml. HIF-1-positiivisuus otettiin huomioon, kun tunnistettiin sekä tuma- että sytoplasmavärjäytyminen. Laskennallinen kuva-analyysi käyttäen Leica Application Suite 4.12.0:aa (Leica Microsystems CMS, GmbH) positiivisesti värjäytyneiden tulehdussolujen lukumäärän puolikvantifioimiseksi koko kudosbiopsiassa tulehdussolujen kokonaismäärästä laskettiin ja ilmaistiin prosentteina.
Yleiset värjäytymisintensiteetit HIF{0}} monoklonaalisilla vasta-aineilla pisteytettiin käyttämällä digitaalista kuva-analyysiä tietokoneavusteisella valomikroskoopilla. Jokaisen dian kuva otettiin käyttämällä 400 × objektiivia. Kuvia katseltiin ja tallennettiin Olympus-mikroskoopilla (Olympus, Center Valley, PA, USA), joka oli varustettu spot-digitaalikameralla (Spot Imaging Solutions, Sterling Heights, MI, USA) ja MATLAB-ohjelmistolla (MathWorks, Natick, MA, USA). Kunkin reaktion keskiarvot perustuivat keskimääräiseen pikselimäärään. Värin intensiteetin eheys perustui harmaasävyisen siirtymän todennäköisyyksiin digitoiduissa kuvissa tummasta vaaleaan. Monoklonaalisella HIF-1-vasta-aineella värjättyjen objektilasien värjäytymisen kokonaisintensiteetti pisteytettiin tuman tai sytoplasmisen ilmentymisen mukaan nollaan, jos värjäytymisintensiteetti oli<10%,+1 if staining intensity was 10%≤30%,+2 if 31%≤50% and+3 if>50 prosentin värjäytymisintensiteetti [37].

Entsyymi-immunosorbenttimääritys
Seerumin valmistusta varten kokoveri kerättiin ja sen annettiin hyytyä jättämällä se häiriintymättä huoneenlämpötilaan. Tämä kesti 10-20 min. Hyytymä poistettiin sentrifugoimalla 2000–3000 rpm 20 minuutin ajan. Ihobiopsiat säilytettiin -80 asteessa. Näytteen painon määrittämisen ja PBS:n (pH 7,4) lisäämisen jälkeen näytteet homogenisoitiin käsin tai jauhimilla ja lopuksi sentrifugoitiin 3 minuuttia nopeudella 10 000 rpm supernatantin poistamiseksi. ELISA-pakkaus (Abcam, ab171571) oli tarkoitettu HIF-1-proteiinipitoisuuksien määrittämiseen seerumissa ja kudoksessa. Entsyymillä leimattuja vasta-aineita lisättiin 60 minuutin inkubointiajaksi 37 asteessa. Levyjen pesun ja kromogeeniliuosten A ja B lisäämisen jälkeen mitattiin optisen tiheyden (OD) arvot näytteiden HIF-1 proteiinipitoisuuksien laskemista varten [37].
Kvantitatiivinen käänteistranskriptio reaaliaikainen PCR
Kokonais-RNA uutettiin 10 mg:sta ihokudosta lyysin ja homogenoinnin jälkeen käyttämällä RNeasy Mini Kitin (Qiagen) tarjoamaa silikaattigeelitekniikkaa [43]. RNA:n pitoisuus ja puhtaus mitattiin aallonpituudella 260, 280 ja 230 nm käyttäen NanoDrop 2000c spektrofotometriä (Thermo Scientific, USA). Suhde A260/A280=1,8–2,1 ja A260/A230=1,8–2,1 osoittaa erittäin puhdasta RNA:ta. Kokonais-RNA käänteiskopioitiin cDNA:ksi käyttämällä suuren kapasiteetin käänteistranskriptaasipakkausta (Applied Biosystems™, USA, luettelonumero 4368814). HIF-1-geenin ilmentymisen havaitsemiseksi kudosnäytteissä alukkeet oli sovitettu kohdegeenien mRNA-sekvensseihin (NCBI Blast -ohjelmisto). GADPH:ta käytettiin taloudenhoitogeeninä [44]. PCR-monistus suoritettiin 25 ul:n reaktiotilavuudessa, joka sisälsi SYBR vihreää PCR Master Mixiä (Applied Biosystems) käyttäen ABI 7900 -sekvenssidetektoria (Applied Biosystems). Reaktio suoritettiin 10 minuutin sisällä alkuvaiheesta DNA-polymeraasin aktivoimiseksi, mitä seurasi 40 sykliä 95 asteessa 15 s ja 60 asteessa 1 min. Yksittäisen tuotteen muodostuminen varmistettiin sulamispisteanalyysillä ja vertailevaa CT-menetelmää käytettiin laskemaan suhteellinen geeniekspressio GADPH:lla endogeenisenä kontrollina. CT-arvojen tilastolliseen analyysiin sovellettiin 2-ΔΔCT-menetelmää jokaiselle spesifiselle alukkeelle ja reaaliaikaiselle PCR:lle [45].
Tulokset
Potilastiedot
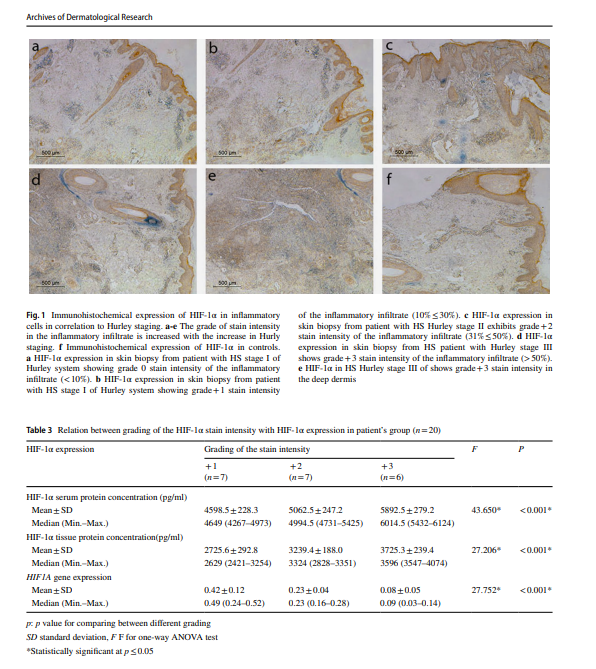
HS-potilaiden ryhmässä oli 15 miestä ja 5 naista. Heidän keski-ikänsä oli 26,10±6,10 vuotta, kun taas kontrolleissa oli 14 miestä ja 6 naista. Heidän keski-ikänsä oli 25,65 ± 4,59 vuotta. Sukupuolen ja iän suhteen ei ollut merkittävää eroa. Sairauden keskimääräinen kesto oli 12,0±9.{15}} kuukautta. Potilailla oli merkittävästi korkeampi BMI verrattuna kontrolleihin. Keskimääräinen BMI HS-ryhmässä oli 29,49±4,56 kg/m2, kun taas vertailuryhmän BMI oli 26,74±3,10 kg/m2 (taulukko 1). Hurley-vaiheesta 25 prosenttia (5 potilasta) oli vaiheessa I, 45 prosenttia (9 potilasta) vaiheessa II ja 30 prosenttia (6 potilasta) vaiheessa III. HS:n kliinisellä vaiheella havaittiin olevan merkittävä yhteys potilaiden HS:n kestoon ja BMI:hen, mutta ei merkittävää yhteyttä sukupuoleen, ikään tai tupakointiin (taulukko 2).
HIF-1:n immunohistokemiallinen havaitseminen leesionaalisessa HS-ihossa
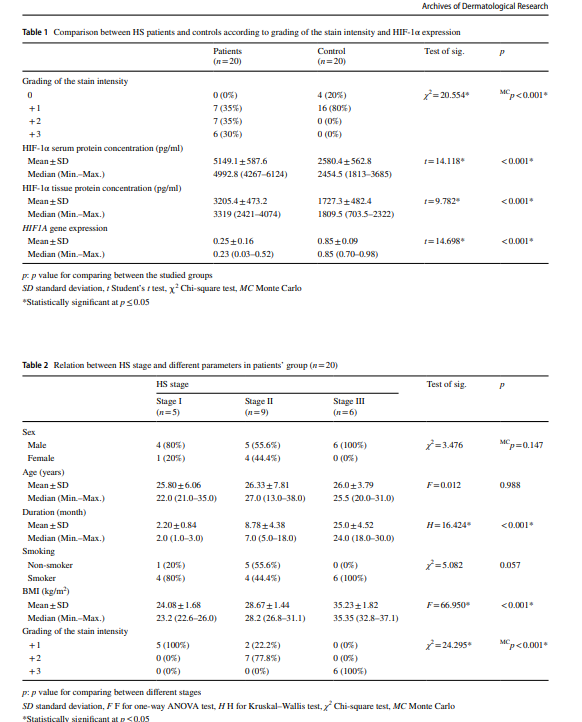
Tahrojen voimakkuus HS-ryhmässä (35 prosentin pistemäärä plus 1, 35 prosentin pistemäärä plus 2, 30 prosentin pistemäärä plus 3) oli merkittävästi korkeampi verrattuna kontrolliryhmään (20 prosentin pistemäärä 0; 80 prosentin pistemäärä plus 1) (Pöytä 1). Kuva 1 ja taulukko 2 esittävät HIF-1:n edustavan immunohistokemiallisen ilmentymisen Hurley-vaiheen suhteen (kuvio 1a–e). Tulehduksellisen infiltraatin lisääntynyt HIF-1-immuunivärjäytyminen voitiin havaita noin Hurley-vaiheessa, kun taas kuvio 1f esittää HIF-1:n immunohistokemiallista ilmentymistä kontrolleissa.
HIF-1-proteiinipitoisuus leesionaalisessa HS-ihossa
Ihon HIF-1-proteiini HS-potilaiden leesionaalisessa ihossa (3205,4±473,2 pg/ml) kasvoi merkittävästi verrattuna terveisiin kontrolleihin (1727,3±482,4 pg/ml) (p<0.001) (Table 1). There was a statistically significant correlation between grading of the staining intensity (Table 3) and Hurley staging of HS (Table 4) and HIF-1α serum level (p<0.001) (Fig. 2c).
HIF-1:n seerumipitoisuudet
Keskimääräiset seerumin HIF-1-tasot HS-potilailla (5149,1±587,6 pg/ml) nousivat merkittävästi verrattuna kontrolliryhmään (2580,4±562,8 pg/ml) (p< 0.001) (Table 1). There was also a positive correlation between HIF-1α serum levels with Hurley staging of HS (Table 4) as well as HIF-1α protein expression (Fig. 2c) and immunohistochemical expression in skin biopsies (Table 3).

Keskustelu
Tutkimuksemme on ensimmäinen tutkimus, joka osoittaa HIF{0}}a:n lisääntyneen ilmentymisen HS-potilaiden ihovauriossa. Normaalissa ihmisen ihossa HIF-1proteiinin ilmentyminen on alhaista ja fokusoitua orvaskessä, toisin kuin karvatuppeissa, talirauhasissa ja hikirauhasissa, joissa HIF-1 on runsaasti ilmentynyt [37]. HIF-1:n lisääntynyt ilmentyminen on havaittu psoriasis vulgariksessa [37, 38, 46–48] ja muissa autoinflammatorisissa sairauksissa, jotka liittyvät Th17-välitteiseen tulehdukseen [25, 49–51]. HIF-1 näyttelee keskeistä roolia Th17-solujen erilaistumisessa [22, 23]. HS:ssä esiintyy ORS-keratinosyyttien hyperproliferaatiota [35, 36] ja se liittyy Th17-välitteiseen autoimmuniteettiin [17–19, 52, 53].
HIF-1a on glykolyysin tärkein transkriptiotekijä [54, 55], jota tarvitaan kiihtyneeseen solujen lisääntymiseen [26]. HIF-1 --indusoitu glykolyysi on yhdistetty keratinosyyttien lisääntymiseen psoriasis vulgariksessa [29, 30, 47]. Huomionarvoista on, että ihmisen karvatuppi osallistuu intensiivisesti aerobiseen glykolyysiin [32, 33] ja HIF{10}}a:n [37] ekspressio on korkea. HIF-1a:n patogeenistä roolia HS:ssä tukee havaintomme HIF-1a:n lisääntyneestä ilmentymisestä HS:n leesioihossa, mikä liittyy positiiviseen korrelaatioon Hurley-vaiheen kanssa (taulukko 2). Analogisesti psoriaasin kanssa [38] havaitsimme myös merkittävästi kohonneita seerumin HIF-1a-tasoja HS-potilaillamme verrattuna terveisiin kontrolleihin. Psoriaasissa korkeat seerumin HIF-1-tasot osoittivat korrelaation IL-6 -yli-ilmentymisen kanssa [38]. IL-6 STAT3-signaloinnin kautta parantaa HIF-1-lauseketta [22].
Psoriaasissa ihmisen ihon mikrovaskulaariset endoteelisolut osoittavat lisääntynyttä angiogeneesiä ja migraatiota [56]. Leesionaalisten HS-alueiden dermissä, joilla on krooninen tulehdus, on myös havaittu lisääntynyttä uudissuonittumista [57, 58]. Tehostettua verisuonten endoteelikasvutekijän (VEGF) ilmentymistä on raportoitu psoriaasissa ja HS:ssä [59]. HIF-1 on angiogeneesin pääsäätelijä ja osallistuu verisuonten muodostumiseen synergististen korrelaatioiden kautta muiden proangiogeenisten tekijöiden, mukaan lukien VEGF:n, kanssa [60].
Käännökset osoittavat, että HIF{{0}}-signaloinnin yli-ilmentyminen liittyy liikalihavuuteen ja tupakointiin, jotka ovat keskeisiä kliinisiä HS:n laukaisevia tekijöitä. Lihavuuden lisääntyneen adiposyyttien hapenkulutuksen on osoitettu lisäävän HIF-1-ilmentymistä [61]. Toisin kuin kohonneilla HIF-1-proteiinitasoilla HS-potilailla, havaitsimme alentuneita HIF-1-mRNA-tasoja, mikä on odottamaton havainto, joka kuitenkin sopii hyvin havaintoihin ihmisen endoteelisoluista, jotka ovat alttiina krooniselle hypoksialle, joka asteittain vähentää HIF-1-mRNA:ta, kun taas HIF-1-proteiinitasot saavuttavat huippunsa nopeasti tuntien kuluttua ja laskevat sitten hitaasti [62, 63]. Huomionarvoista on, että mikroRNA-21 (miR21) säätelee liikaa lihavien ja diabeettisten potilaiden rasvakudoksessa [64–66]. MiR-21, miR-155, miR-223, miR-31, miR-125b ja miR{18}}a:n merkittävä yli-ilmentyminen on havaittu leesionaalisessa HS-ihossa verrattuna terveisiin kontrolleihin [67]. Mielenkiintoista on, että miR-21 kohdistuu ja siten heikentää VHL-mRNA:n ilmentymistä [68–71]. NFkB säätelee MiR-146a:ta, ja se kohdistuu synnynnäisten immuunivasteiden signaaliproteiinien 3´UTR:iin [72] sekä HIF-1-mRNA:han [73]. MiR-148a on toinen liikalihavuuteen ja diabetekseen liittyvä lisääntynyt miR [74–78]. HIF1AN, FIH-1-koodia koodaava geeni, on miR-148a:n, miR-31:n ja miR-125:n suora kohde, jotka kaikki estävät HIF-1 transaktivaatio (TargetScanHuman, julkaisu 8.0).

Krooninen tupakansavulle altistuminen (CS) aiheuttaa systeemistä hypoksiaa [79] CS-uute lisäsi myös miR-21- ja HIF-1a-ilmentymistä ihmisen keuhkoputkien epiteelisoluissa (HBE) [80]. HBE-solut vapauttavat miR-21-rikastettuja eksosomeja CS-altistuksen jälkeen, mikä tehostaa HIF-1-signalointia kohdentamalla pVHL:ää [81, 82]. Lisätodisteet vahvistavat, että CS aktivoi HIF-1a:n [83, 84]. Nikotiini lisäsi HIF{11}}-ilmentymistä ei-pienisoluisissa keuhkosyöpäsoluissa [85]. Bentso(a)pyreeni, CS-uutteen [86] komponentti, parantaa HIF-1:n sitoutumiskykyä HIF-1-proteiiniin [87]. CS ja hypoksia lisäävät sekä oksidatiivista stressiä että tuottavat reaktiivisia happilajeja, jotka indusoivat autoreaktiivisia pro-inflammatorisia T-soluja ja vähentävät Treg-solujen aktiivisuutta [88].
Mielenkiintoista on, että D-vitamiinin puutos on toistuvasti vahvistettu HS-potilailla ja se on liitetty taudin vakavuuteen [89–93]. D-vitamiinilla on estäviä vaikutuksia mTORC1:een [94, 95], mikä edistää HIF{5}}a:n synteesiä [14]. D-vitamiinilisä säätelee mTORC1-aktiivisuutta ja alensi HIF{8}}a-mRNA-tasoja runsasrasvaisen ruokavalion aiheuttamien liikalihavien hiirten CD4- ja T-solualaryhmissä [96]. Huomaa, että D-vitamiini/VDR-signalointi tehostaa VHL:n transkriptiota [97].
Proinflammatoriset sytokiinit, kuten IL-17A, tuumorinekroositekijä-a (TNF-a) ja pääasiassa IL-1, lisääntyvät huomattavasti HS-leesionaalisessa ihossa [98]. IL-1 lisää HIF-1a- ja HIF-1a-riippuvaisen geenin ilmentymistä [99, 100]. Anakinran IL-1 esto osoitti terapeuttisia vaikutuksia vaikeassa HS:ssä [101]. HepG2-soluissa IL-1 ei vaikuttanut reportterigeenin ilmentymiseen normoksiassa, kun taas hypoksian aikana IL-1 vahvisti HIF-1-reportterigeenin aktiivisuutta 25 prosenttia verrattuna pelkkään hypoksiaan [102]. HIF-1a on tunnistettu NF-κB:n kohdegeeniksi, joka yhdistää hypoksian, tulehduksen ja oksidatiivisen stressin [103–106]. TNFa:n kautta säädelty NF-kB tehostaa suoraan HIF-1-mRNA:n ja proteiinin ilmentymistä evoluutionaarisesti konservoituneella tavalla [107]. Äskettäin kokeellisessa autoimmuunisessa enkefalomyeliitissä (EAE) on osoitettu, että IL-17A värvää IL-1 -erittäviä myeloidisoluja, jotka tuottavat patogeeniset δT17- ja Th17-solut [108], kun taas hiiret, joilla on HIF-1 - puutteelliset T-solut ovat resistenttejä Th17-riippuvaisen EAE:n induktiolle [23]. Nämä tiedot korostavat läheistä ylikuulumista proinflammatoristen sytokiinien ja HIF-1-signaloinnin välillä, millä voi myös olla vaikutusta HS-patogeneesiin.
Yksisoluinen RNA-sekvensointi paljastaa solu- ja transkriptionaaliset muutokset, jotka liittyvät M1-makrofagien polarisaatioon HS:ssä, jotka liittyvät HIF-1a:n lisääntyneeseen ilmentymiseen [109]. HIF-1a:lla on keskeinen rooli makrofagiglykolyysin induktiossa ja pro-inflammatorisen M1-polarisaation aktivoinnissa [110]. M1-polarisoiduissa makrofageissa HIF-1a vastaa jatkuvasta IL-1 -tuotannosta [111].
Viimeaikaiset todisteet osoittavat, että sekä Notch- että HIF{0}}a-signalointi koordinoi glykolyysiä [112]. Notch intracellular domain (ICD) tehostaa HIF-1 a:n rekrytointia kohdepromoottoreihinsa [113]. HIF-1 stabiloi Notch-signalointia [114–116]. Yli-ilmentynyt Notch/PI3K/AKT [3] ja mTORC1-signalointi HS:ssä [6] voivat siten edelleen tehostaa HIF-1-välitteistä geenisäätelyä HS:ssä.
Infundibulaarinen hyperkeratoosi ja sitä seuraava follikulaarinen tukkeutuminen triginaalisten ihoalueiden välillä voi johtaa duktaaliseen hypoksiaan, HIF{0}}a:n aiheuttamaan komedogeeniseen mekanismiin, jota aiemmin ehdotettiin aknen patogeneesissä [117, 118]. Hyperbaric happikäsittely (HBOT) parantaa HS:ää ja tehostaa adalimumabin ja ustekinumabin tehoa [119–121]. Valituissa kokeellisissa malleissa HBOT vähensi HIF-1a:n ilmentymistä [122–124].

Viime aikoina on kiinnostanut diabeteslääke metformiini HS:n hoitoon [125–130]. Metformiini ei ainoastaan vähennä mTORC1:n aktiivisuutta [131], vaan myös säätelee HIF-1a:n ilmentymistä [132–137]. Rapamysiinin (sirolimuusi) aiheuttama mTORC1:n esto paransi myös HS:n kliinistä kulkua [138].
Kaiken kaikkiaan tutkimuksemme tarjoaa todisteita leesion HIF{0}}proteiinin ilmentymisestä HS-potilailla, mikä korreloi Hurley-vaiheen kanssa (taulukot 2, 4). Psoriaasin autoimmuunipatogeneesin [37] perusteella havaitsimme lisääntyneen HIF-1a-proteiinin ilmentymisen HS:ssä, mikä molemmilla jaoilla tehosti HIF-1a- ja IL-17-signalointia (kuva 3). On olemassa vakuuttavaa näyttöä siitä, että HIF-1a on HS-patogeneesin säätelemätön päätranskriptiotekijä, joka selittää (1) tehostetun HIF-1a:n aiheuttaman glykolyysin keratinosyyttien liikakasvun kanssa, (2) lisääntyneen HIF-1 a/ROR t -välitteinen Th17-solujen erilaistuminen lisääntyneen IL-17-tuotannon kanssa, (3) vähentynyt Treg-solujen erilaistuminen HIF-1a-välitteisen FoxP3:n hajoamisen vuoksi, (4) liikalihavuuden ja tupakoinnin aiheuttama HS:n paheneminen, HS:n tärkeimmät laukaisutekijät, jotka lisäävät HIF-signalointia. Leesionaaliset epätasapainot HIF-1-signalaatiossa ovat HS:n patogeneesin häiriintyneiden infundibulaaristen keratinosyyttien ja Th17-solujen lisääntymisen keskellä. HIF{24}}a:n farmakologinen kohdentaminen voi olla lupaava lähestymistapa HS:n hallintaan, kuten jo ehdotettiin psoriaasin ja muiden autoimmuunisairauksien hoidossa [48, 50, 139, 140].

Tekijän panokset
BM suunnitteli tutkimuksen ja käsitteli tutkimuskysymyksen. BM ja NA kirjoittivat käsikirjoituksen. OS, RG, DM, SA, NE ja NA osallistuivat yhtä lailla näytteen käsittelyyn, immunofluoresenssileimaukseen ja datan tilastolliseen analyysiin. Kaikki kirjoittajat hyväksyivät käsikirjoituksen lopullisen version.
Rahoitus
Avoimen rahoituksen tarjoaa The Science, Technology & Innovation Funding Authority (STDF) yhteistyössä Egyptin Knowledge Bankin (EKB) kanssa. Ei mitään.
Tietojen saatavuus
Kaikki tässä tutkimuksessa analysoidut tiedot sisältyvät julkaistuun artikkeliin nimellä Dataset S1 ja Dataset S2.
Viitteet
1. Kozera EK, Frew JW (2022) Hidradenitis suppurativan patogeneesi: kehittyvät paradigmat monimutkaisissa sairauksissa. Dermatol Ilm. 3:39–49
2. Wolk K, Join-Lambert O, Sabat R (2020) Hidradenitis suppurativan etiologia ja patogeneesi. Br J Dermatol 183:999-1010
3. Hessam S, Gambichler T, Skrygan M et al (2021) Lisääntynyt NCSTN:n, Notch:n ja PI3K/AKT3:n ilmentymisprofiili hidradenitis suppurativassa. J Eur Acad Dermatol Venereol 35:203–210
4. Vural S, Baumgartner M, Lichtner P et al (2021) Gamma-sekretaasigeenikompleksimutaatioiden tutkiminen Saksan väestössä, jolla on Hidradenitis suppurativa, osoittavat monimutkaisen polygeenisen perinnön. J Eur Acad Dermatol Venereol 35(6):1386-1392
5. Garg A, Zema C, Kim K et al (2022) HS-IGA:n kehittäminen ja alkuperäinen validointi: uusi hidradenitis suppurativa -spesifinen tutkijan globaali arviointi käytettäväksi interventiotutkimuksissa. Br J Dermatol. https://doi.org/10.1111/bjd.21236
6. Lembo S, Fabbrocini G (2016) Rapamysiinin, insuliiniresistenssin ja hidradenitis suppurativan kohde: mahdollinen metabolinen silmukka. J Eur Acad Dermatol Venereol 30:1631–1633
7. Balato A, Lembo S, Ayala F et al (2017) Rapamysiinikompleksin 1 mekaaninen kohde on osallisena psoriaasissa ja sitä säätelee anti-TNF-hoito. Exp Dermatol 26:325–327
8. Buerger C (2018) Epidermaalinen mTORC1-signalointi edistää psoriaasin patogeneesiä ja voisi toimia terapeuttisena kohteena. Front Immunol 9:2786
9. Ali M, Bukhari SA, Ali M et al (2017) Upstream signaling of mTORC1 ja sen hyperaktivaatio tyypin 2 diabeteksessa (T2D). BMB Rep 50:601–609 (virhe: BMB Rep 51:45-53)
10. Cota D (2009) nisäkäskohde rapamysiinikompleksin 1 (mTORC1) signaalin energiatasapainossa ja liikalihavuudessa. Physiol Behav 97:520–524
11. De Vita V, Melnik BC (2018) Aktivoitu mTORC1-signalointi: tyypin 2 diabeteksen ja hidradenitis suppurativan yhteinen liikkeellepaneva voima. J Am Acad Dermatol 78:e121
12. De Vita V, Melnik BC (2019) mTORC1 aineenvaihdunnan ja immuniteetin risteyksessä hidradenitis suppurativassa. J Eur Acad Dermatol Venereol 33:e107
13. Linke M, Fritsch SD, Sukhbaatar N et al (2017) mTORC1 ja mTORC2 solumetabolian säätelijöinä immuniteetissa. FEBS Lett 591:3089–3103
14. Laplante M, Sabatini DM (2013) mTORC1:n säätely ja sen vaikutus geenin ilmentymiseen yhdellä silmäyksellä. J Cell Sei 126:1713-1719
15. Nagai S, Kurebayashi Y, Koyasu S (2013) PI3K/Akt- ja mTOR-kompleksien rooli Th17-solujen erilaistumisessa. Ann NY Acad Sci 1280:30–34
16. Ren W, Yin J, Duan J et al (2016) mTORC1-signalointi ja IL-17-ilmentyminen: reittien ja mahdollisten terapeuttisten kohteiden määrittely. Eur J Immunol 46:291-299
17. Fletcher JM, Moran B, Petrasca A et al (2020) IL-17 tulehduksellisissa ihosairauksissa psoriaasissa ja hidradenitis suppurativassa. Clin Exp Immunol 201:121-134
18. Frew JW (2022) Autovasta-ainevälitteiset makrofagivasteet tarjoavat puuttuvan linkin synnynnäisen ja adaptiivisen immuunihäiriön välillä hidradenitis suppurativassa. J Invest Dermatol 142:747-749
19. Melnik BC, John SM, Chen W et al (2018) Helper 17 -solujen/säätely-T-solujen epätasapaino hidradenitis suppurativassa/acne inversassa: yhteys karvatupen dissektioon, liikalihavuuteen, tupakointiin ja autoimmuunisairauksiin. Br J Dermatol 179:260-272
20. Monfrecola G, Balato A, Caiazzo G, et al (2020) IL-17 tulehduksellisissa ihosairauksissa psoriaasissa ja hidradenitis suppurativassa. Clin Exp Immunol 201:121-134
21. Moran B, Sweeney CM, Hughes R et al (2017) Hidradenitis suppurativalle on ominaista Th17: Treg -soluakselin säätelyhäiriö, joka korjataan anti-TNF-hoidolla. J Invest Dermatol 137:2389-2395
22. Dang EV, Barbi J, Yang HY et ai. (2011) T(H)17/T(reg)-tasapainon kontrollointi hypoksialla indusoituvalla tekijällä 1. Cell 146:772–784
23. Shi LZ, Wang R, Huang G et al (2011) HIF1alfa-riippuvainen glykolyyttinen reitti järjestää metabolisen tarkistuspisteen TH17- ja Treg-solujen erilaistumista varten. J Exp Med 208:1367–1376
24. Corcoran SE, O'Neill LA (2016) HIF1 ja metabolinen uudelleenohjelmointi tulehduksissa. J Clin Invest 126:3699-3707
For more information:1950477648nn@gmail.com
