Uudet fenyylietanoidiglykosidit Cistanche Tubulosasta
Apr 12, 2024
Cistanche spp.:n kemiallisia aineosia koskevassa tutkimussarjassamme. (Orobanchaceae),fenyylietanoidiglykosidit1-3) ja iridoide4) alkaenCistanche salsa(CA MEY.) G. BECK on raportoitu. Tämä artikkeli käsittelee Cistanche tubulosa (SCHRENK) HOOK -bakteerin fenyylietanoidiglykosideja. f. kerätty Pakistanissa.Cistanche tubulosa(SCHRENK) KOUKKU. f.5) on Salvadoran ja Calotropis spp.:n juurissa kasvava loiskavi, jota esiintyy laajalti Pohjois-Afrikassa, Arabiassa, Länsi-Aasiassa, Pakistanissa ja Intiassa. Koko kasvia käytetään lääketieteellisesti Pakistanissa ripulin ja haavaumien lääkkeenä.6) Haluamme nyt raportoida neljän uuden fenyylietanoidiglykosidin, nimeltä tubulosidit A (II), B (VI), C (VII) ja D (VIII), sekä neljän tunnetun fenyylietanoidiglykosidin, ekinakosidin (I), akteosidin ( III), akteosidi-isomeeri (IV) ja 2'-asetyylilakteosidi (V). Näiden yhdisteiden rakenteet määritettiin kemiallisten todisteiden ja spektroskooppisten tutkimusten perusteella.
Koko kasvin etanoliuute suspendoitiin veteen. Tämä suspensio uutettiin etyyliasetaatilla ja sitten vedellä kyllästetyllä n-butanolilla. N-butanoliin liukeneva fraktio kromatografoitiin polyamidi- ja silikageelikolonneilla ja sille suoritettiin korkean suorituskyvyn nestekromatografia (HPLC) peräkkäin, jolloin saatiin kahdeksanfenyylietanoidiglykosidit(I-VIII).

LUONNOLLINEN CISTANCHE TUBULOSA YRTTI CISTANCHE KASVIT PHGS75% ECH 30% ACT 12%
Yhdisteet I, III, IV ja V eristettiin amorfisina jauheina, joilla oli samanlaiset spektrit kuin yhdisteillä.ekinakosidi, 1) akteosidi, 1) akteosidi-isomeeri7) ja 2'-asetyylilakteosidi,2) ja ne tunnistettiin suoraan vertaamalla autenttisiin näytteisiin [ohutkerroskromatografia (TLC), infrapuna (IR), protoniydinmagneettinen resonanssi (1H-NMR) ja hiili-13 ydinmagneettinen resonanssi (13C-NMR) spektrit].
Tubulosidi A (II) eristettiin amorfisena jauheena, [ƒ¿]D{{0}},7•‹ (MeOH), C37H48O21.3/2 H2O. IR-spektri viittasi hydroksyyliryhmien (3440 cm-1), konjugoidun esterin (1705 cm-1), kaksoissidoksen (1634 cm-1) ja aromaattisten renkaiden (1608) esiintymiseen. , 1522 cm-1), ja ultravioletti (UV) spektri osoitti absorptiomaksimit aallonpituudella 220, 250 sh, 292 sh ja 334 nm. Yhdisteen II 1H-NMR-spektri osoitti ramnoosin metyyliryhmän signaaleja [6 1.07 (3H, d, J= 6 Hz)], asetoksiryhmän metyylisignaalia [{{27} },98 (3H, s)], bentsyylimetyleeniprotonit [6 2,70 (2H, t, J= 7 Hz)], kaksi glukoosianomeeristä protonia [6 4,32, 4,54 (1H kumpikin, d, J= 8 Hz)], ramnoosi-anomeerinen protoni [6 5,11 (1H, br s)], kaksi trans-olefiinistä protonia [6 6,25 , 7,64 (kukin 1H, d, J= 16 Hz)] ja aromaattiset protonit [6 6.5 7 ,2 (6H)]. Asetyloinnissa II tuotti undekaasetaatin (Ila), joka oli identtinen ekinakosidin (I) dode-kapasitaatin kanssa. Yhdisteen II13C-NMR-spektri oli lähes identtinen I:n kanssa, lukuun ottamatta signaaleja, jotka johtuivat suoraan aglykoniin sitoutuneesta glukoosista ja asetoksyyliryhmästä [6 20,9 (CH3), 171,5 (C {{63). }})], mikä viittaa siihen, että asetoksyyliryhmä on kiinnittynyt glukoosiosaan. Yhdisteen II13C-NMR-spektrissä asylaatio siirtyy81 [-2,3 (C-1), -0,9 (C-2) ja -1 .0 (C-3)] havaittiin sisäisen glukoosin C-1, C-2 ja C-3 kohdissa yksityiskohtaisella vertailulla I:n spektriin, mikä osoittaa, että asetoksiryhmä on kytketty II:n glukoosiosan C-2-hydroksyyliryhmään. Yhdisteen II metanolyysissä asetyylikloridilla metanolissa metyylikafeaattia ja 3,{81}}dihydroksifenetyylialkoholia havaittiin TLC:llä ja HPLC:llä. Yhdisteen II happohydrolyysi 10-prosenttisella rikkihapolla tuotti glukoosia ja ramnoosia suhteessa 2:1.

LUONNOLLINEN CISTANCHE TUBULOSA SEKSUAALISTEN TOIMINTOJEN PARANTAMISEEN PHGS75% ECH 30% ACT 12%
Edellä mainittujen todisteiden perusteella taulukon A rakenteen määritettiin olevan 2-(3,4-dihydroksifenyyli)etyyli-0-aL-ramnopyranosyyli-(1•¨3)- [ƒÀ-D-glu-kopyranosyyli-(1-6)]-(4-O-caffeoy1)-2-O-asetyyli-fl-D-glukopyranosidi (II).
Tubulosidi B (VI) eristettiin amorfisena jauheena [a]D,{0}}.0•‹ (MeOH), C31H38016, jonka 1H-NMR-spektri osoitti alifaattisen asetoksyyliryhmän läsnäolon. [6 1,98 (3H, s)]. Yhdisteen VI13C-NMR-spektri oli hyvin samanlainen kuin akteosidi-isomeerin (IV), mutta erosi hieman signaaleissa johtuen glukoosiosasta ja asetoksiryhmän [6 20.9 (CH3), 171,6 ( C =0)]. Asetoksiryhmän sijainti yhdisteen VI glukoosiosassa määritettiin sen13C-NMR-spektristä vertaamalla yksityiskohtaisesti IV:n vastaavaan.
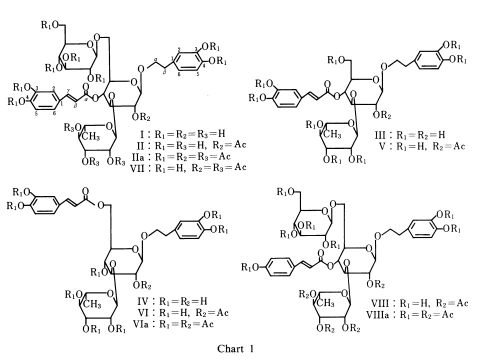
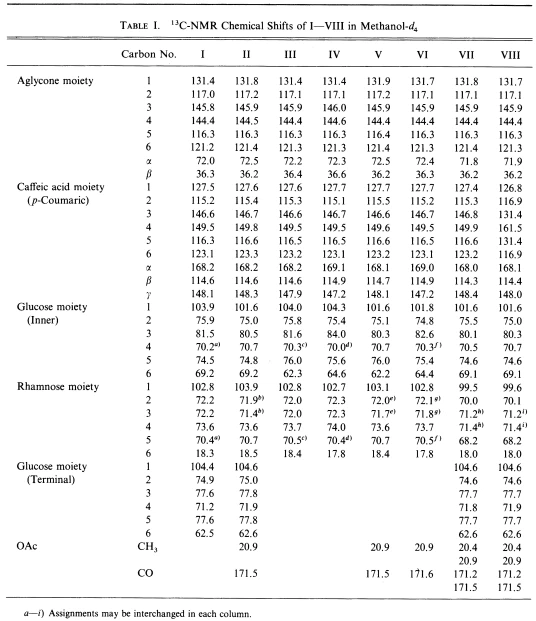
Glukoosiosan C{{0}}, C-2 ja C-3 signaalit osoittivat asylaatiosiirtymiä (-2.5 (C-1) ), -0 ,6 (C-2) ja -1.4 (C-3)], kuten II:n tapauksessa, mikä osoittaa, että asetoksiryhmä on liittynyt C{:een {12}} glukoosiosan hydroksyyliryhmä Asetyloinnissa VI tuotti oktaasetaatin (VIa), joka oli identtinen yhdisteen IV nonaasetaatin kanssa Metanolissa VI asetyylikloridilla metanolissa,{{ 14}}dihydroksifenetyylialkoholi havaittiin TLC:llä ja HPLC:llä. VI:n happohydrolyysi 10 % rikkihapolla tuotti glukoosia ja ramnoosia suhteessa 1:1. Nämä tulokset johtivat päätelmään, että tubulosidi B:n rakenne on {{18}. }(3,4-dihydroksifenyyli)etyyli-0-aL-ramnopyranosyyli-(1-3)-(6-0-kafeo1)- 2-0-asetti143-D- glukopyranosidi (VI).

LUONNOLLINEN CISTANCHE TUBULOSA IMMUUNITEETTA PARANTAAN PHGS75% ECH 30% ACT 12%
Tubulosidi C (VII) eristettiin amorfisena jauheena [a],-104.8•‹ (MeOH), C43H54024 H20, jonka 1H-NMR-spektri osoitti neljän alifaattisen asetoksyyliryhmän läsnäolon [{{7} },80, 1,92, 1,95 ja 2,08 (kukin 3H, s)]. Yhdisteen VII "C-NMR-spektri oli lähes identtinen tubulosidi A:n (II) kanssa, jonka sisäisessä glukoosissa on alifaattinen asetoksyyliryhmä, lukuun ottamatta ramnoosiosasta johtuvia signaaleja. Lisäksi 13C-NMR-spektri VII, asylaatiosiirtymät') havaittiin ramnoosiosan C-2, C-3 ja C-4 aiheuttamissa signaaleissa vertaamalla yksityiskohtaisesti II:n tietoihin neljän asetoksiryhmän sijainneiksi määritettiin sisäisen glukoosin C-2 ja ramnoosiosan C-2, C-4 kohdassa VII asetylointi, VII tuotti oktaasetaatin, joka oli identtinen tubulosidi A undekaasetaatin (IIa) kanssa. Yhdisteen VII metanolisointi asetyylikloridilla metanolissa, metyylikaffeaatti ja 3, 4--dihydroksifenetyylialkoholi havaittiin TLC:llä ja hapon HPLC:llä VII 10-prosenttisella rikkihapolla tuotti glukoosia ja ramnoosia suhteessa 2:1.
Yllä olevista tuloksista taulukon C rakenteen määritettiin olevan 2-(3,4- hydroksifenyyli)etyyli-2,3,4-tri-O-asetyyli-aL-tamnopyranosyyli-( 1 -+ 3)-[/9-D-glukopyranosyyli- (1 -+ 6)]-(4-0-kafeoy1)-2-0-asetyyli-fl-D-glukopyranosidi (VII) .
TubulosidiD (VIII) eristettiin amorfisena jauheena, [oc], -91,4 astetta (MeOH), C43H54023. H20, jonka 1H-NMR-spektri osoitti neljän alifaattisen asetoksiryhmän läsnäolon [6 1,81, 1,93, 1,96 ja 2,09 (kukin 3H, s)]. Asetyloinnissa VIII tuotti heptaasetaatin (VIIIa), jonka 1H-NMR-spektri osoitti kahdeksan alifaattista [6 1,87, 1,94, 1,96, 1,99, 2,10 (kukin 3H, s) ja 2,02 (9H, s)] ja kolme aromaattista [6 2,27, 2,30 ja 2,32 (kukin 3H, s)] asetoksyylimetyylisignaalia. VIII:n13C-NMR-spektri oli lähes identtinen tubulosidi C:n (VII) kanssa, lukuun ottamatta p-kumaarihappoosasta johtuvia signaaleja. Yhdisteen VIII metanolyysissä asetyylikloridilla metanolissa metyyli-p-kumaraattia ja 3,{44}}dihydroksifenetyylialkoholia havaittiin TLC:llä ja HPLC:llä. VIII:n happohydrolyysi 10-prosenttisella rikkihapolla tuotti glukoosia ja ramnoosia suhteessa 2:1.
Näiden tulosten perusteella taulukkosivun D rakenteeksi määritettiin 2-(3,4- dihydroksifenyyli)etyyli-2,3,4-tri-O-asetyyli-a-Lrhamnopyranosyyli- (1•¨3)-[ƒÀ-D-glukopyranoosy-] (1→6)} (4-0-p-kumari1)-2-0-asetyyli-fl-D-glukopyranosidi (VIII).
monetfenyylietanoidiglykosiditkuten forsytosidi A, 'aste) leukoskeposidi A,7 isomar-tynosidell) ja niin edelleen, joissa on ramnoosiosa terminaalisena sokerina. Näissä tapauksissa ramnoosiosa ei asetyloidu. Tubulosidit C (VII) ja D (VIII) sisältävät asetyloidun ramnoosiosan ja ovat ensimmäisiä luonnossa esiintyviä yhdisteitä, joissa on triasetyyliramnoosiosa, joista on raportoitu.

LUONNOLLINEN CISTANCHE TUBULOSA TESTOSTERONIN TUOTANNON TEHOSTAMISEEN PHGS75% ECH 30% ACT 12%

