KidneyNetwork: Munuaisista peräisin olevien geenien ilmentymistietojen käyttäminen munuaissairauksiin liittyvien uusien geenien ennustamiseen ja priorisoimiseen Ⅰ
Aug 07, 2023
Geneettinen testaus potilailla, joilla epäillään perinnöllistämunuaissairausei välttämättä paljasta häiriön geneettistä syytä, koska mahdollisesti patogeeniset variantit voivat sijaita geeneissä, joiden ei vielä tiedetä liittyvänmunuaissairaus. Olemme kehittäneet Kidney Networkin, joka hyödyntää kudosspesifistä ilmentymistä tiedottaakseen ehdokasgeenien priorisoinnista erityisesti munuaissairauksia varten. KidneyNetwork on uusi menetelmä, joka on rakennettu integroimalla 878 näytteen munuais-RNA-sekvensointiverkosto 31 499 näytteen monikudosverkkoon. Se käyttää ilmentymismalleja ja vakiintuneita geeni-fenotyyppiassosiaatioita ennustaakseen, mitkä geenit voivat liittyä mihinkin (sairaus)fenotyyppiin puolueettomasti. Sovelsimme KidneyNetworkia harvinaisiin muunnelmiin 13 munuaissairauspotilaan, joilla ei ollut geneettistä diagnoosia, eksomesekvensointitiedoissa ehdokasgeenien priorisoimiseksi. KidneyNetwork voi ennustaa tarkasti munuaisspesifisiä geenitoimintoja ja (munuaistauti) fenotyyppejä sairauksiin liittyville geeneille. Priorisoitujen geenien ja harvinaisia variantteja kantavien geenien leikkaus potilaalla, jolla oli munuais- ja maksakysta, identifioi ALG6:n uskottavaksi kandidaattigeeniksi. Vahvistamme tätä uskottavuutta tunnistamalla ALG6-variantteja useissa kystisten munuais- ja maksasairaustapauksissa ilman vaihtoehtoisia geneettisiä selityksiä. Esittelemme KidneyNetworkin, julkisesti saatavilla olevan munuaisspesifisen yhteisilmentymisverkoston, jossa on optimoituja geenifenotyyppiennusteita munuaissairauksien fenotyypeille.

Suunnittelimme helppokäyttöisen verkkokäyttöliittymän, jonka avulla lääkärit ja tutkijat voivat käyttää geenien ilmentymis- ja yhteissäätelytietoja jageenifenotyyppiyhteyksiä nopeuttamaan perinnöllisten munuaissairauksien diagnosointia ja tutkimusta.
Käännöslausunto:Geneettinen testaus potilailla, joilla epäillään perinnöllistämunuaissairausei välttämättä paljasta potilaan häiriön geneettistä syytä. Mahdollisesti patogeeniset variantit voivat sijaita geeneissä, joiden ei vielä tiedetä liittyvän munuaissairauksiin, mikä vaikeuttaa näiden varianttien merkityksen tulkintaa. Tämä paljastaa selkeän tarpeen menetelmille geneettisen variaation fenotyyppisten seurausten ennustamiseksi puolueettomasti. Tässä kuvataan KidneyNetwork, työkalu, joka käyttää kudosspesifistä ilmentymistä ennustamaan munuaisspesifisiä geenitoimintoja. KidneyNetworkin soveltaminen diagnosoimattomien tapausten ryhmään tunnisti ALG6:n ehdokasgeeniksi kystisessä munuaisissa jamaksasairaus. Yhteenvetona voidaan todeta, että KidneyNetwork voi auttaa geneettisten varianttien tulkinnassa ja voi siksi olla arvokasta translaationefrogeneesissä ja auttaa parantamaan munuaissairauspotilaiden diagnostista saantoa.

NAPSAUTA TÄSTÄ SAATAksesi CISTANCHE MUNAISEENSAIRAUS
JOHDANTO
Geneettinen testaus potilailla, joilla epäillään perinnöllistä munuaissairautta, voi paljastaa aiheuttavia patogeenisiä varianttejamunuaisiin liittyvät geenit. Monissa tapauksissa geneettistä syytä ei kuitenkaan voida vielä havaita. Patogeenisia variantteja tunnetuissa munuaisiin liittyvissä geeneissä havaitaan noin 10–30 prosentilla geneettisesti testatuista potilaista, joilla on mistä tahansa syystä krooninen munuaissairaus [1–3]. Nämä prosenttiosuudet ovat kuitenkin todennäköisesti aliarvioita niiden potilaiden lukumäärästä, joilla on monogeeninen syy, koska muunnelmat geeneissä, jotka eivät vielä liity munuaissairauteen, jäävät huomaamatta. Näissä geeneissä voi olla mahdollisesti haitallisia variantteja, mikä vaikeuttaa näiden varianttien tärkeysjärjestystä ja tulkintaa. Siksi nykyisellä genomisella lääketieteen aikakaudella yksi suurimmista haasteista tunnetuissa geeneissä saadun negatiivisen diagnostisen tuloksen jälkeen on havaita ja priorisoida uusia ehdokasgeenejä, joissa on mahdollisesti patogeenisiä variantteja, jotka voivat selittää potilaan sairauden [4].
RNA-sekvensointitietoja voidaan käyttää ehdokkaan ennustamiseensairauden geenit[5]. Kehitimme äskettäin GeneNetworkin ja GeneNetwork-Assisted Diagnostic Optimization (GADO) -menetelmän priorisoidaksemme uusia ehdokassairausgeenejä RNA-sekvensointitietojen perusteella [6]. Tämän menetelmän ideana on, että tietyt harvinaiset sairaudet voivat johtua useiden geenien muunnelmista. Vaikka nämä geenit ovat erilaisia, niillä on yleensä samanlaiset biologiset toiminnot. Kun tutkitaan geenien ilmentymistietoja suuresta määrästä näytteitä, nämä sairauden geenit osoittavat yleensä voimakasta yhteisilmentymistä [6]. Jos siis on muita geenejä, jotka ilmentyvät voimakkaasti tunnettujen harvinaisten sairauksien geenien kanssa, on mahdollista, että myös näiden muiden geenien variantit voivat aiheuttaa saman taudin.
Jotta tällainen työkalu toimisi optimaalisesti, yhteisilmaisutietojen tulee olla mahdollisimman tarkkoja. GADOa varten rakensimme geenien yhteisilmentymisverkoston, joka perustui julkisesti saatavilla oleviin RNA-sekvensointitietosarjoihin monista eri kudoksista, ja käytimme tätä verkkoa ennustamaan, mitkä geenit saattavat aiheuttaa harvinaisia sairauksia. Nämä ennusteet opetettiin käyttämällä ihmisen fenotyyppiontologiatietokantaa (HPO) [7]. HPO-tietokannassa geenit on jaettu fenotyyppeihin, joita kutsutaan HPO-termeiksi, jotka perustuvat OMIM [8]- ja Orphanet [9] -tietokannassa oleviin geenitautimerkintöihin ja sairauden oireisiin. Integroimalla HPO-tietokannan tiedot geenien yhteisilmentymisverkostoon, voisimme laskea ennustepisteet jokaiselle geenille HPO-termiä kohti. Yhdessä nämä pisteet muodostavat GeneNetworkin. GADO priorisoi sitten geenit yhdistämällä syöteluettelon HPO-termeistä, jotka kuvaavat potilaan fenotyyppiä, luetteloon geeneistä, joissa on mahdollisia haitallisia variantteja kyseisestä potilaasta. Geeniluettelon priorisointi perustuu syötettyjen HPO-termien yhdistettyihin geeniennustuspisteisiin [6].
Koska havaitsimme, että GeneNetworkin ennustekyky munuaisiin liittyville HPO-fenotyypeille oli rajallinen, pyrimme parantamaan ennustetta kehittämällä munuaisspesifistä verkkoa. Teimme tämän käyttämällä 878 munuaisen RNA-sekvensointinäytettä, joita rikastimme olemassa olevalla 31 499 näytteen tietojoukolla muista kudoksista [6]. Kehittämällä uuden ennustealgoritmin, joka voi punnita molemmissa tietojoukoissa olevat tiedot, paransimme munuaisiin liittyvien reittien suorituskykyä. Tässä artikkelissa esittelemme tuloksena syntyneen KidneyNetworkin, yhteisilmentymisverkoston, jota voidaan käyttää ennustamaan tarkasti munuaisiin liittyville HPO-termeille tuntemattomien geenien geenifenotyyppiyhdistykset. Todisteeksi periaatteesta sovelsimme KidneyNetwork-sekvensointidataa potilaille, joilla oli aiemmin ratkaisemattomia munuaissairauksia.
MENETELMÄT
Parantaaksemme munuaisiin liittyvien fenotyyppien ennustamista keräsimme munuaisperäisiä RNA-sekvensointitietoja, päivitimme GeneNetworkin uusimmilla viitetietokantoilla ja parannettiin tilastollisia analyyseja, minkä jälkeen integroimme kudosspesifisiä tietoja.
Tietojoukot KidneyNetworkissa
RNA-sekvensointitiedot useista eri alkuperää olevista valituista munuaisnäytteistä, mukaan lukien primaari-, kasvain- ja sikiökudos, yhdistettiin olemassa olevaan monikudos-RNA-sekvensointitietoaineistoon, jota käytettiin aiemmin kuvatun geeniverkostomme perustana [6] (taulukko S1, S2) . Päätimme sisällyttää usean kudoksen tietojoukon kahdesta syystä. Ensin tarvitsimme riittävän määrän näytteitä perusverkon rakentamiseen. Toiseksi halusimme säilyttää ilmentymisen, joka on spesifinen useille tai kaikille munuaissolutyypeille, mutta ei muille kudoksille. Teimme tämän, koska geenifenotyyppipisteet perustuvat näytteiden välisiin ilmentymiseroihin; jos kaikilla geeneillä on korkea (tai alhainen) ilmentyminen kaikissa analyysiin sisältyvissä näytteissä, ne eivät lisää riittävästi tietoa ennustusalgoritmiin. GeneNetworkin kehittämiseen käytettyä monikudosaineistoa ihmisen RNA-sekvensointinäytteistä käytettiin uudelleen ja käsiteltiin aiemmin kuvatulla tavalla [6]. Esikäsittelyn jälkeen tämä tietojoukko sisälsi 31 499 näytettä ja 56 435 geeniä.
3 194 munuaisperäistä RNA-sekvensoitua näytettä ladattiin European Nucleotide Archivesta (ENA) ja Genotype-Tissue Expression (GTEx) -projektista (Huomautus S1). Munuaistietojoukon esikäsittely tehtiin samalla tavalla kuin monikudosaineisto [6] (huomautus S2, huomautus S3). Näytteen ja geenin valinnan jälkeen jäljelle jäi 58 283 geeniä ja 878 munuaisnäytettä. Tutkimme loput 878 RNA-sekvensointinäytettä käyttämällä UMAP-klusterialgoritmia (huomautus S4).
HPO-suodatus. KidneyNetworkin rakentamiseen käytimme geenifenotyyppiassosiaatioita HPO-tietokannan [7] versiosta 1268. HPO-tietokannassa geenien merkitseminen HPO:n määrittämiin fenotyyppeihin perustuu OMIM-sairaustutkimuksen [8] geenitaudin annotaatioihin. kartta (ladattu 26. maaliskuuta 2018) ja Orphanet [9] "en_product6.xml" -tiedoston versio 1.3.1. Näiden tietokantojen geenitautimerkinnät voivat perustua useisiin tekijöihin, mukaan lukien tilastolliset assosiaatiot ja laajamittaiset kopiomäärän vaihtelut. Halusimme kouluttaa KidneyNetworkia käyttämällä vain geenejä, joiden yhteys geenin ja harvinaisen sairauden välillä on vakiintunut. Siksi sulkimme pois multigeeniset oireyhtymät, koska usein ei ole selvää, mitkä kopioluvun muunnelmien geeneistä vaikuttavat mihinkin fenotyyppeihin. Jätimme pois myös pelkät herkkyysgeenit (huomautus S5).
Ilmaisujen normalisointi. Näytteen ja geenin laadunvalvonnan (QC) jälkeen jäljellä olevien näytteiden ja geenien ekspressiomatriisi log2- transformoitiin ja geenimäärät normalisoitiin käyttämällä DESeq:ia mediaanisuhteiden menetelmää noudattaen. Tämän jälkeen korjasimme geeniekspressiotiedot kovariaattien osalta (Huomautus S6).

Hajoaminen
Suodatuksen ja koko tietojoukon QC:n jälkeen seuraava vaihe oli suorittaa hajotus tietojoukon ominaisvektorien laskemiseksi (Huomautus S7). Sekä GeneNetworkille että munuaisperäiseen dataan perustuvalle geenisäätelyverkostolle määritimme optimaalisen komponenttien määrän (Huomautus S8). Ensimmäiset 165 ominaisvektoria GeneNetworkille ja ensimmäiset 170 ominaisvektoria munuaisperäisille tiedoille tunnistettiin ja yhdistettiin suuremmaksi matriisiksi, joka sisältää kaikki 335 ominaisvektoria.
Geeni-HPO-termipistemäärän laskenta Geenifenotyypin pisteytyslaskelma tehtiin useassa vaiheessa (kuva S5). Ensin suoritimme logistisen regression käyttämällä yhdistettyjä ominaisvektoreita ja geenifenotyyppiannotaatiotiedostoa syötteenä. Käytimme tuloksena saatuja arvoja ja ominaisvektoripisteitä laskeaksemme geenin log-odds-pisteet jokaiselle geenille jokaisessa ominaisvektorissa (huomautus S9).

Välttääksemme jo annotoitujen geenien geenilogaritmit-pisteiden liiallista sovittamista, sovelsimme jätä yksi pois ristiinvalidointimenetelmää (huomautus S10). Log odds muutettiin myöhemmin geenin z-pisteiksi käyttämällä permutoitua nollajakaumaa jokaiselle fenotyypille (Huomautus S11).
Ennusteen tarkkuuden määrittämiseksi laskemme ROC-käyrän alla olevan alueen (AUC). AUC laskettiin HPO-termiä kohti käyttämällä ennustettuja geenin z-pisteitä ja tunnettuja huomautuksia. Ennusteiden merkitsevyys laskettiin käyttämällä kaksipuolista Mann-Whitney-arvotestiä. Bonferroni-korjauksen jälkeen ennustetta pidettiin merkitsevänä p < 0,05.
Ennusteen suorituskyvyn vertailu
Vertailimme neljän erillisen verkon ennustekykyä: (1) alkuperäinen GeneNetwork, (2) päivitetty GeneNetwork, (3) munuaisspesifinen geenisäätelyverkosto, joka perustuu yksinomaan munuaisperäisiin näytteisiin, ja lopuksi (4) KidneyNetwork, joka yhdistää kaksi jälkimmäistä. Näiden verkkojen tekemien HPO-ennusteiden laatu arvioitiin kunkin munuaiseen liittyvän fenotyypin AUC:n perusteella (taulukko S3). Verkon laadun parantuminen määriteltiin parantuneeksi ennustetarkkuudeksi munuaisiin liittyville termeille, jotka ennustettiin merkittävästi jokaisessa kahden verkon vertailussa, ja lisääntyneellä merkittävästi ennustettujen munuaisiin liittyvien termien lukumäärällä. Verkon ennustetarkkuuden paranemisen merkitystä verrattiin verkosta toiseen käyttämällä DeLong-testiä [10], joka on integroitu pROC R -pakettiin [11].
KidneyNetworkin soveltaminen 13 potilaaseen, joilla epäillään perinnöllistä munuaistautia Yksi KidneyNetworkin sovelluksista on priorisoida ehdokasgeenit potilailla, joilla on ratkaisematon munuaissairaus. Tämän kliinisen sovelluksen arvioimiseksi käytimme KidneyNetworkia priorisoidaksemme kandidaattigeenit potilaille, joilla on erilaisia munuaissairauksia GADO-menetelmällä [6]. GADO yhdistää KidneyNetworkin kautta annetut geeniennusteen z-pisteet tietylle HPO-termijoukolle. Geenit, joiden yhdistetty z-pistemäärä oli suurempi tai yhtä suuri kuin 5 jokaiseen potilaaseen liittyvälle ainutlaatuiselle HPO-termijoukolle, pidettiin mahdollisina ehdokasgeeneinä kyseiselle potilaalle.

Kuvio 1 UMAP-visualisointi munuaisperäisestä ilmentymisdatasta. 878 näytettä ryhmiteltiin kolmeen pääryhmään: terve primaarikudos (keskellä ja alaosa), kehitysnäytteet (vasemmalla) ja munuaissolukarsinoomanäytteet (RCC) (oikealla). Kuvan vasemmalla puolella näkyy pluripotenteista kantasoluista (PSC) peräisin olevien podosyyttien ja PSC-peräisten organoidien klusteroituminen primääristen sikiönäytteiden ja nefronien esisolujen kanssa. Oikealla puolella RCC-näytteet ryhmittyvät lähelle proksimaalisia tubulusnäytteitä, ja RCC-klusteri, joka on lähinnä terveitä primäärikudosnäytteitä, koostuu ei-kirkassoluisista RCC-näytteistä (nccRCC). Keskellä ja alaosassa terveet primaariset munuaisnäytteet ryhmittyvät niiden alkuperäkudoksen perusteella.
Kaikilla tutkimukseen osallistuneilla 13 potilaalla epäiltiin monogeenista munuaistautia, mutta heillä ei ollut geneettistä diagnoosia (Huomautus S12). Näille tapauksille määritettiin HPO-termit niiden fenotyypin perusteella. Jokaisen potilaan täydelliset eksomin sekvensointitiedot analysoitiin käyttämällä CAPICEa [12] mahdollisesti patogeenisten varianttien tunnistamiseksi. Geenit, jotka sisältävät muunnelmia, joissa on gnomAD Popmax -suodatus AF [13]<0.005 and a recall ≥99%, corresponding with a mild CAPICE cut-off of ≥0.0027, were considered interesting candidates.
GADO:n KidneyNetwork-integraation tunnistamien geenien päällekkäisyys CAPICE:n tunnistamien geenien kanssa johti luetteloon geeneistä jokaiselle potilaalle. Nefrogeneesin asiantuntijapaneeli (AMvE, LRC, NVAMK) tarkasteli manuaalisesti nämä geenit ja näiden geenien variantit niiden patogeneettisen potentiaalin suhteen populaatiometriikan, ennustetyökalujen, saatavilla olevan kirjallisuuden ja erottelun perusteella (Huomautus S13). Tuloksena olevalle ehdokasgeenille tunnistettiin lisää potilaita, joilla oli saman geenin variantteja, yhteistyökumppaneiden ja 100,{2}} genomiprojektin [14] kautta. Myös GeneMatcher-työkalua [15] käytettiin, eikä se tuottanut uusia potilaita 15. helmikuuta 2023 mennessä.
Lisäpotilaiden tunnistaminen Harvinaisten varianttien arvioinnissa käytettiin aiemmin kuvattua ratkaisematonta monirakkulatautien kohorttia [16] (huomautus S14). Käytimme Fisherin tarkkaa testiä vertaillaksemme tunnistettujen varianttien esiintyvyyttä ei-suomalaisten eurooppalaisten eurooppalaiseen osajoukkoon gnomAD-tietokannassa [17]. Lisäksi käytimme 100,{5}} genomiprojektia [14] lisäpotilaiden tunnistamiseen tunnistettujen varianttien perusteella (huomautus S15).

TULOKSET
Tiedonhaku ja näytteiden klusterointi Valitsimme 878 munuaisnäytettä (kuva S2), jotka ryhmittelimme ja piirsimme UMAP-algoritmin avulla (kuva 1). Yleensä tiedot ryhmittyvät kolmeen pääklusteriin: primaariset ei-kasvaintiedot, munuaisten kehitysnäytteet ja proksimaaliset tubulus-, glomerulus- ja munuaissolukarsinoomanäytteet (RCC).
KidneyNetwork parantaa geenifenotyyppiennusteita Ensinnäkin päivitimme GeneNetworkin päivitetyllä HPO-tietokannalla (kuva S6) ja optimoimme geeniverkoston rakennusputkilinjan (kuva S7). Nämä muutokset tuottivat parannuksen yleiseen GeneNetworkiin verrattuna edelliseen versioon (kuva S8). Sitten käytimme parannettua putkistoa munuaisspesifisen geenisäätelyverkoston rakentamiseen. Kuten odotettiin, koska pieni otoskoko, tämä versio munuaiskohtaisen verkon toiminut huonommin kuin GeneNetwork (kuva S9). Myöhemmin GeneNetworkin ja munuaisspesifisen geenin yhteisilmentymisverkoston yhdistäminen KidneyNetworkiin tuotti parhaat tulokset munuaisiin liittyville HPO-termeille (Kuva 2A; Taulukko S5). Jokaisen ennustetun reitin ennuste AUC-, tarkkuus-, herkkyys- ja f{11}}pisteet on annettu (taulukko S6).
Kaksi esimerkkiä parantuneista munuaisiin liittyvistä HPO-termeistä ovat hypomagnesemia ja tubulointerstitiaalinen poikkeavuus (kuvio 2B). Näiden fenotyyppien visualisointi tiheyskäyrillä osoittaa korkeampia priorisoinnin z-pisteitä tunnetuille sairauteen liittyville geeneille verrattuna geeneihin, joita ei ole merkitty. Tuntemattomien geenien osalta mitä korkeampi ennusteen z-piste on, sitä todennäköisemmin ne ovat ehdokassairausgeeni. Tunnettujen sairausgeenien geenivuorovaikutusverkostojen visualisointi ennustepisteiden perusteella osoittaa jälleen KidneyNetworkillä saatujen vuorovaikutusten määrän ja voimakkuuden lisääntymisen GeneNetworkiin verrattuna.
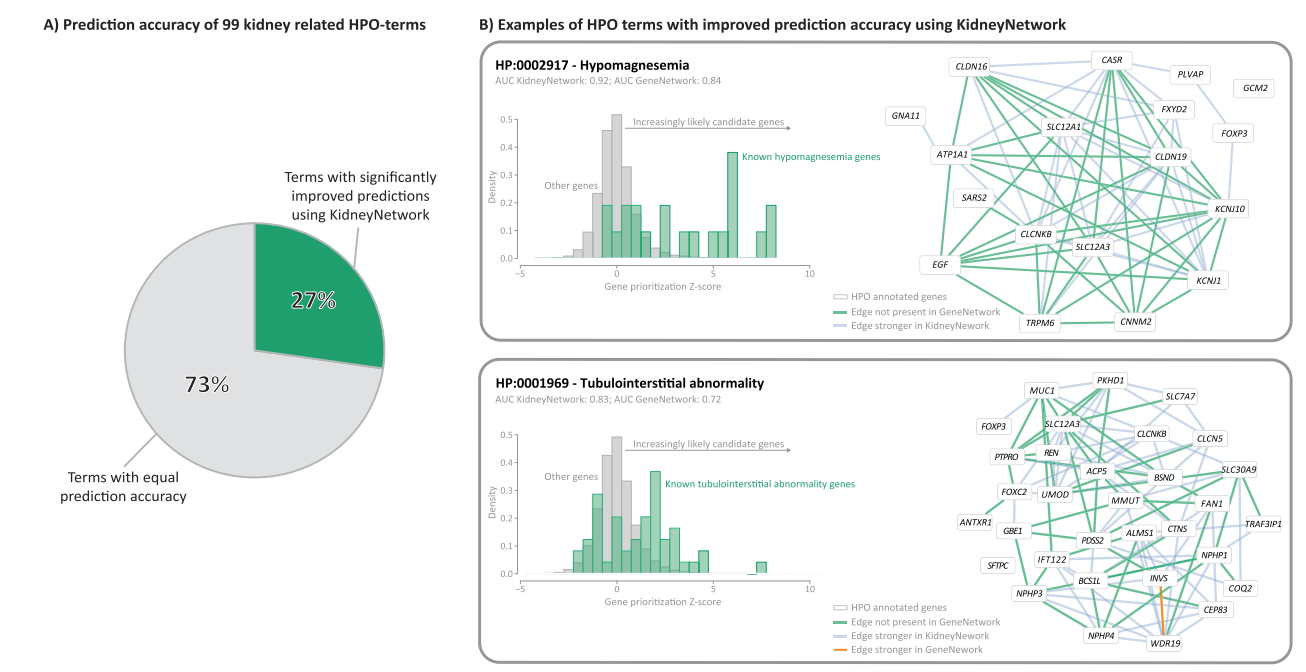
Kuva 2 KidneyNetwork toimii paremmin munuaisiin liittyvillä HPO-termeillä kuin päivitetty GeneNetwork. 27 prosenttia munuaisiin liittyvistä fenotyypeistä ennustetaan huomattavasti paremmin KidneyNetworkin avulla verrattuna GeneNetworkiin. B Geenin ennustepisteiden tiheyskäyrät kahdessa parantuneimmassa fenotyypissä, hypomagnesemia ja tubulointerstitiaalinen poikkeavuus, osoittavat korkeampia ennustusarvoja geeneille, joihin on merkitty fenotyyppi, ja ennustavat myös mahdollisia tuntemattomia ehdokasgeenejä. KidneyNetworkin avulla ennustetut verkot osoittavat enemmän ja vahvempia korrelaatioita annotoitujen geenien välillä kuin GeneNetworkillä ennustetut verkot.
Näimme myös lisääntyneen merkittävien ennustettujen munuaisiin liittyvien HPO-termien määrässä munuaisverkostolle (n=71) verrattuna GeneNetworkiin (n=63). Tämä sai meidät olettamaan, että KidneyNetwork ennustaa munuaisiin liittyviä termejä kokonaistarkkuudella ja pystyy siksi ennustamaan enemmän munuaisiin liittyviä fenotyyppejä, joilla on suurempi merkitys. Parillinen t-testi osoittaa, että kaiken kaikkiaan HPO AUC-pisteet olivat huomattavasti parempi Munuaisverkon verrattuna GeneNetworkiin (keskimääräinen AUC: 0,76 vs. 0,74; t-testin p-arvo: 4,5 × 10 -8). Tämä tulos viittaa siihen, että KidneyNetwork ennustaa enemmän munuaisspesifisiä HPO-termejä paremmalla ennustetarkkuudella kuin GeneNetwork.
KidneyNetwork priorisoi ALG6:n ehdokassairausgeeninä potilailla, joilla on munuaiskystat ja maksakystat. Tutkiaksemme KidneyNetworkin kliinistä käyttökelpoisuutta asetimme etusijalle geenit 13 potilaalle, joilla epäillään perinnöllistä munuaissairautta, mutta joilla ei ollut geneettistä diagnoosia, ja leikkaamme nämä geenit, jotka sisältävät mahdollisesti patogeenisiä variantteja. Tuloksena saadut geeniluettelot sisälsivät 1-4 kandidaattigeeniä yhdeksälle 13 potilaasta (taulukko S7). Yhdellä potilaalla (NÄYTE 6) tämän luettelon manuaalinen kuratointi tunnisti ALG6:n (ALG6 alfa-1, 3-glukosyylitransferaasi) mahdolliseksi ehdokasgeeniksi, joka selittää potilaan munuais- ja maksakystat (kuva 3). Yhdistetty z-pistemäärä ALG6:lle lasketuille HPO-termeille oli merkittävä munuaisverkossa usean testauksen korjauksen jälkeen (z=5.43). Tämä geeni olisi jäänyt huomaamatta, jos olisimme käyttäneet GeneNetworkia: siellä ALG6 ei saavuttanut z-pisteen merkitsevyyskynnystä, joka on suurempi tai yhtä suuri kuin 5.

ALG6 ehdokasgeeninä potilaille, joilla on munuais- ja maksakysta. NÄYTTEEN 6 kantama ALG6-variantti c.680 plus 2 T > G on heterotsygoottinen. Tämä on tunnettu patogeeninen silmukointikohdan variantti, joka johtaa synnynnäiseen glykosylaatiohäiriöön (CDG) tyyppi Ic, kun patogeenisiä variantteja on molemmissa alleeleissa [18, 19]. ALG6 muistuttaa vahvasti ALG8:aa, joka on osallisena munuaisten ja maksan kystafenotyyppeihin [20], ja KidneyNetworkin mukaan ALG6 ja ALG8 ovat voimakkaasti yhteissäädeltyjä (z-pisteet=8.59).
Tämän biologisen uskottavuuden vuoksi tutkimme ALG6:ssa harvinaisten varianttien, MAF < 0.001, polykystisen munuaissairauden ja maksasairauden 120 toisiinsa liittymättömän tapauksen kohorttia. Tämä kohortti on hieman päivitetty, koska se on kuvattu aiemmin ja se on suljettu pois exome-sekvensointianalyysillä toimintamutaatioiden menettämisen tai raportoitujen patogeenisten ei-typistyvien varianttien varalta PKD1:ssä, PKD2:ssa, PRKCSH:ssa, SEC63:ssa, GANABissa, ALG8:ssa, ALG9:ssä, SEC61B:ssä, PKHD1:ssä tai DNAJB11 [16]. Kolmessa toisiinsa liittymättömässä tapauksessa (YU372, YU378, YU481) oli harvinaisia ALG6-variantteja; jokaisella oli sama ALG6 c.257 plus 5 G > Ei-kanoninen silmukointivariantti, jonka tiedettiin olevan patogeeninen ALG6-CDG:lle ja silmukoitumista muuttavalle in vitro [19, 21]. Jaetusta mutaatiosta huolimatta nämä kolme tapausta raportoivat, ettei yhtään tunnettua sairastuneen perheenjäsentä ollut rekisteröitynä eri osavaltioista Yhdysvalloista, eivätkä ne liity VCFtools relatedness2-algoritmin parhaaseen havaitsemisrajaan, jonka Relatedness_PHI < 0,005.
Ottaen huomioon tämän muunnelman edustuksen kolmessa eurooppalaisen syntyperän tapauksessa tässä fenotyyppisesti määritellyssä kohortissa, vertasimme sen esiintymistiheyttä tapausten eurooppalaisessa osajoukossa (n=105) ei-suomalaisiin eurooppalaisiin gnomAD:ssa [17] kattavuuden ollessa tämä asema (n=64,466) [17]. Potilaskohortissa 3 alleelista 210:stä sisälsi tämän variantin, kun taas gnomAD:ssa, kohortissa, jota ei valittu munuaisten tai maksan kystataakan suhteen, se löydettiin 121:stä 128 932 alleelista. Tämä suunnilleen 10-kertainen rikastuminen on tilastollisesti merkitsevä Fisherin tarkalla testillä, p=0.0011. Tämä mutaatio toistui myös ALG6-CDG-tapauksissa [19].
Tutkimme myös 100,000 genomiprojektin tietojoukkoa [14] ja otimme yhteyttä yhteistyökumppaneisiin, jotka tunnistivat kolme lisätietoa munuaissairauksiin sovellettavaksi. Merkittävä osa potilaista, joilla epäillään geneettistä munuaissairautta, jää ilman geneettistä diagnoosia, koska monien sairauksien sairausgeeniluettelot ovat epätäydellisiä. Munuaissairauteen vaikuttavien geenien tunnistaminen on välttämätöntä munuaissairauspotilaiden diagnostisen tuoton parantamiseksi ja taudin patogeneesin tutkimiseksi hoitomahdollisuuksien lähestymiseksi. Uusien sairausgeenien muodostaminen vaatii huolellista biologista validointia. Tällaisten tutkimusten arvoisten geenien osallistuminen on kriittistä. KidneyNetworkin käyttö yhdessä WES- tai GWAS-tietojen kanssa nefrologien, kliinisten geneetikkojen tai tutkijoiden toimesta auttaa jokaista näistä ryhmistä osallistumaan geeniimplikaatioon. KidneyNetwork yhdistää munuaisnäytetietoaineistoon perustuvan yhteisilmentymisverkon aiemmin julkaistuun usean kudoksen tietoaineistoon, jota käytetään GeneNet-työn rakentamiseen. Tietojen yhdistäminen KidneyNetworkiin paransi munuaissairauksiin liittyviä fenotyyppiennusteita verrattuna kahteen tietokokonaisuuteen erikseen perustuviin verkkoihin. Todisteeksi periaatteesta osoitamme, että KidneyNetworkin tuottaman munuais- ja maksakystien yhdistetyn fenotyypin ehdokasgeeniluettelossa asetettiin etusijalle hallittavissa oleva lista ehdokasgeenejä pitkästä geeniluettelosta, joka sisälsi harvinaisia variantteja potilaallamme, jolla on tämä fenotyyppi.
Tutkimme myös 100,000 genomiprojektin tietojoukkoa [14] ja otimme yhteyttä yhteistyökumppaneisiin, jotka tunnistivat kolme muuta potilasta, joilla oli munuais- ja/tai maksakysta, joilla oli heterotsygoottinen, mahdollisesti haitallinen variantti ALG6:ssa, ilman vaihtoehtoista geneettistä selitystä.

Kuva 3 KidneyNetwork sisällytetty GADO-menetelmään SAMPLE6:ssa, potilaalla, jolla on munuais- ja maksakysta. KidneyNetwork priorisoi 89 ehdokasgeeniä kaikista geeneistä käyttämällä GADOa HPO-termien "munuaiskystat" (HP:0000107) ja "maksakystat" (HP:0001407) perusteella. Exome-sekvensointitietojen tulkintamenetelmä CAPICE tuotti 322 geeniä, jotka sisälsivät potentiaalisesti patogeenisiä variantteja potilaan eksomin sekvensointitiedoissa. Kun nämä geeniluettelot limitettiin, tunnistettiin kolme valintakriteerit täyttävää geeniä, joista yksi oli ALG6.
Kaikkiaan tunnistimme seitsemän potilasta, joilla oli tunnettuja silmukointikohdan variantteja, joiden ilmoitettiin aiheuttavan tautia vakavasti sairastuneilla CDG-potilailla homotsygoottisuuden tai yhdisteen heterotsygoottisuuden vuoksi, ja yhden potilaan, jolla oli todennäköinen patogeeninen silmukointikohdan variantti (taulukko 1). Toisin kuin vakavasti sairastuneet ALG6-CDG-potilaat (joissa esiintyi useita elimiä, mukaan lukien kehitysviive ja useita neurologisia oireita), potilaillamme oli useiden munuaiskystojen ja/tai maksakystojen fenotyyppi (kuva 4). . Vaikka PCLD voi olla laaja, munuaisten fenotyyppi näyttää olevan lievä, eikä eGFR:n laskua ole raportoitu korkeasta iästä huolimatta (eli yksi potilas on kolmekymppinen ja muut 45–80-vuotiaita). Lisäksi havaitsimme, että ALG6-variantti erottui muutamissa perheenjäsenissä, jotka myös sairastuivat (taulukko 1; kuva 4).
Tukipalvelu:
Sähköposti:wallence.suen@wecistanche.com
Whatsapp/Puh.: plus 86 15292862950
Myymälä:
https://www.xjcistanche.com/cistanche-shop






