Yksiselitteinen NMR-rakenteellinen määritys (plus)-katekiini-lakkaasin dimeerireaktiotuotteista mahdollisina rypäleiden ja viinin hapettumisen merkkiaineina
Mar 12, 2022
Lisätietoja saat ottamalla yhteyttä:tina.xiang@wecistanche.com
Abstrakti:( plus )-Katekiini-lakasihapettumistadimeeriset standardit hemisyntetisoitiin käyttämällä Trametesin lakkaasia. Versicolor on vesi-etanoliliuos pH:ssa 3,6. Havaittiin kahdeksan fraktiota, jotka vastasivat kahdeksaa potentiaalista hapettumisdimeeristä tuotetta. Fraktioprofiileja verrattiin kahdella muulla oksidoreduktaasilla saatuihin profiileihin:polyfenolioksidaasiuutettu rypäleistä ja lakkaasi Botrytis cinereasta. Profiilit olivat hyvin samankaltaisia, vaikka jotkut pienet erot viittasivat mahdollisiin eroihin näiden entsyymien reaktiivisuudessa. Sitten viisi fraktiota eristettiin ja analysoitiin 1D- ja 2D-NMR-spektroskopialla. Kadmiumnitraatin jäämien lisääminen asetoniin liuotettuihin näytteisiin johti fenolisten protonien täysin erottuneisiin NMR-signaaleihin, mikä mahdollisti kuuden reaktiotuotteen yksiselitteisen rakenteellisen määrityksen, joista toinen sisältää kaksi enantiomeeriä. Näitä tuotteita voidaan edelleen käyttää hapettumismerkkiaineina niiden läsnäolon ja kehityksen tutkimiseksi viinissä viininvalmistuksen ja viinin ikääntymisen aikana.
Avainsanat: hapettumismerkki;( plus )-katekiini; fenoliset NMR-signaalit; lakkaasi; kadmiumnitraatti; polyfenolioksidaasi

Napsauta saadaksesi lisätietoja
1. Esittely
Polyfenolitovat ryhmä kemiallisia yhdisteitä, joita esiintyy laajasti luonnossa. Niitä löytyy merkittäviä määriä teessä [1], kaakaossa [2,3], mustikoissa [4], viinirypäleissä [5 litraa] ja fermentoiduissa tuotteissa, kuten viinissä [6]. Polyfenolien kemialliset rakenteet kehittyvät jatkuvasti, koska ne ovat ensisijaisia hapetuskohteita J7,8]. Nämä muutokset vaikuttavat monentyyppisten elintarvikkeiden organoleptisiin ominaisuuksiin; ne ovat vastuussa ilmiöistä, kuten ruoan ruskistumisesta [9] ja viinin aistinvaraisten ominaisuuksien muutoksista [10,11. Enologiassa tämä hapettumisilmiö tapahtuu rypäleissä tai viineissä. Mitä tulee entsymaattiseen hapettumiseen, tärkeimmät ruskehtamisesta vastaavat entsyymit ovat oksidoreduktaasit, tarkemmin sanottunapolyfenolioksidaasirypäleissä ja Botrytis cinerean tuottamassa lakkaasissa [12].
Entsymaattinenhapettumistaesiintyy pääasiassa rypäleen puristemehussa, mutta viinin ruskistuminen edelleen voi johtua kemiallisista hapetusreaktioista |7,13]tai Botrytis cinerea -lakkaasista, joka voi olla erittäin stabiili viinin ikääntymisen aikana14. Fenolisubstraateilla voi esiintyä kahta hapetusentsymaattista aktiivisuutta: monofenolioksidaasiaktiivisuus, jolle on tunnusomaista olemassa olevan hydroksyyliryhmän viereisen aseman hydroksylaatio ja difenolioksidaasiaktiivisuus, joka vastaa orto-dihydroksibentseenien hapettumista orto-bentsokinoneiksi.
Kansainvälisen biokemian ja molekyylibiologian liiton (NC-IUBMB) nimikkeistökomitean mukaan näitä entsymaattisia aktiivisuuksia katalysoivat oksidoreduktaaseja vastaavat EC1--luokan entsyymit. Niiden joukossa polyfenolien hapettumista katalysoivien oksidoreduktaasien kolme pääluokkaa ovat EC1.14.18.1 (monofenolimono-oksigenaasi), EC1.11.1 (peroksidaasi/POD) ja EC1.10.3 (difenoleihin vaikuttavat oksidoreduktaasit).
Tämä viimeinen luokka on jaettu eri alaluokkiin, ja kaksi niistä vaikutti erityisen mielenkiintoisilta tämän tutkimuksen kannalta: EC1.10.3.1 (polyfenolioksidaasi/PPO) ja EC1.10.3.2 (lakaasi) (katso lisämateriaalit kuva S1).
PPO, lakkaasi ja peroksidaasi ovat oksidoreduktaaseja, jotka ovat pääasiassa vastuussa ruskistumisesta rypäleiden käsittelyn aikana [13]. POD:n aiheuttama ruskistuminen on vähäistä hedelmissä, mutta se voi lisätä fenolien hajoamista yhdistettynä PPO:n kanssa[15]. PPO:ta on luonnollisesti rypäleissä ja se pystyy katalysoimaan monofenolien hapettumista katekoleiksi ja katekolien hapettumista ruskeiksi pigmenteiksi [8,13,16]. Botrytis-tartunnan saaneissa rypäleissä esiintyvillä lakkaaseilla on laajempi vaikutusspektri|17|koska ne voivat katalysoida monien eri substraattien hapettumista. Lakkaasien pääasialliset hapettumiskohteet ovat 1-2 ja 1-4 dihydroksibentseeni.
Viinissä hapetuksella syntyvä bentsokinoni (PPO tai lakkaasit) voi helposti joutua lisäreaktioihin riippuen niiden redox-ominaisuuksista ja elektronisista affiniteeteista [15]. Ne voivat joko toimia elektrofiileinä ja reagoida aminojohdannaisten kanssa [18] tai toimia hapettimina ja reagoida muun muassa fenolisubstraattien kanssa. Kemiallisesta konformaatiostaan (kinoni tai puolikinoni) riippuen bentsokinoni voi johtaa erilaisiin hapettumisreaktiotuotteisiin. Neutraalissa pH:ssa (plus)-katekiini hapettuu kinoniksi A-renkaan asemassa C5 tai C7 ja johtaa kuuden mahdollisen dimeerisen isomeerin muodostumiseen, mikä tarkoittaa sidosta B-renkaan aseman C2', C5' tai välillä. Ylemmän katekiiniyksikön C6' ja alayksikön A-renkaan asema C6 tai C8 [19,20]. Dehydrodikatekiini on tämän kytkennän hyvin tunnettu tuote [21]. Rakenteiden merkintäpaikat on esitetty kuvassa 1. Happamissa olosuhteissa puolikinonimuotoja voi esiintyä myös B-renkaassa (asema OH3' tai OH4') ja johtaa neljään mahdolliseen dimeeriseen isomeeriin [20,22]. ylempi katekiiniyksikkö ja alemman yksikön A-rengas (asento C6 tai C8). Katekiinin entsymaattista hapettumista tutkittiin aikaisemmissa tutkimuksissa [22, 23], ja siihen liittyvät hapetustuotteet karakterisoitiin HPLC:llä [24], joskin harvemmin eristetty eikä koskaan täysin karakterisoitu NMR:llä.

Tämän työn tavoitteena oli ensin verrata UHPLC-MS:llä dimeeristen (plus)-katekiinin hapettumistuotteiden profiileja kolmen oksidoreduktaasiuutteen, eli rypäleistä uutetun PPO:n, Botrytis cinerea -sienen lakkaasin, läsnä ollessa botrytisoiduissa makeissa viineissä. [14] ja Trametes Versicolorin lakkaasi.
Toinen tavoite oli hemisyntetisoida ja karakterisoida joidenkin dimeeristen hapetustuotteiden rakenteet NMR-spektroskopialla, joka on saatu Trametes Versicolorin lakkaasilla.

2. Tulokset ja keskustelu
2.1. Dimeeristen reaktiotuotteiden profiilien vertailu, jossa on kolme erilaista oksidoreduktaasia ja (plus)-katekiini
(plus)-Katekiini hapetettiin ensin Trametes Versicolorin lakkaasin läsnä ollessa pH 3,6:ssa malliviiniliuoksessa. Sen jälkeen kun dimeerifraktio oli erotettu jäännös(plus)-katekiinistä ja muista polymeerifraktioista, kerättiin kahdeksan pääfraktiota ja analysoitiin UHPLC-UV-MS:llä, merkittiin N1:stä N8:aan kasvavassa retentioaikajärjestyksessä (taulukko 1). Sähkösumutusmassaspektrit positiivisessa moodissa osoittivat ionihuiput [M plus H] plus arvolla m/z 579 N1-N6:lle, mikä vastaa hypoteettisesti dimeeriä, jonka muodostaa yksittäinen sidos kahden katekiiniyksikön välillä, ja [M plus H] plus kohdassa m/577 N7:lle ja N8:lle, mikä viittaa hypoteettisesti lisäsidoksen muodostumiseen.
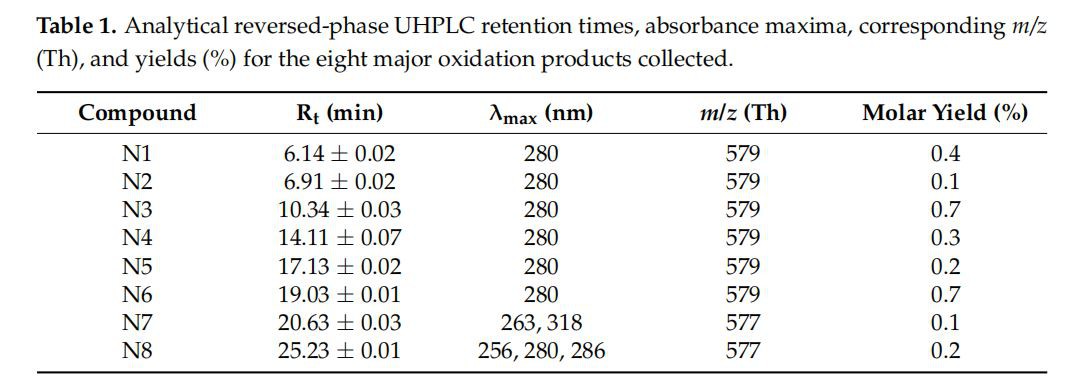
Nämä kahdeksanhapettumistafraktioita havaittiin mahdollisesti tanniinifraktion kemiallisen depolymeroinnin jälkeen aikaisemmissa töissä [25,26], ja ne voivat mahdollisesti olla samoja kuin Guyot et al. [20], vaikka koeolosuhteet olisivatkin hieman erilaiset. Todellakin, tässä aiemmassa tutkimuksessa raakaa PPO-uutetta käytettiin pH:ssa 3 ja 6 kahdeksan fraktion saamiseksi. Tässä tutkimuksessa vertailtiin kolmea eri entsyymiä pH 3,6:ssa malliviiniliuoksessa. Kolmella eri entsyymillä (Trametes Versicolorin lakaasi, Botrytis cinereasta lac-case ja rypäleistä uutettu polyfenolioksidaasi) saatujen tärkeimpien hapetusfraktioiden LC-MS-vertailuanalyysi on esitetty taulukossa 2. Jokaisen kahdeksasta fraktiosta retentioajat olivat lähes identtiset eri entsyymeillä ja samanlaiset m/z määritettiin MS-analyysillä. Nämä tulokset tukevat hypoteesia, että jokaiselle entsyymille saatiin samat fraktiot, jotka sisälsivät tuotteita, joiden rakenteet ovat samanlaiset kuin Guyotin et ai. [20]. Lopez-Serrano ja Ros Barcel6 [27] suorittivat myös vertailevan tutkimuksen (plus)-katekiinin hapettumistuotteista kahdella eri entsyymillä: peroksidaasilla ja polyfenolioksidaasilla, jotka molemmat uutettiin mansikoista. He päättelivät, että näillä kahdella entsyymillä saadut tuotteet olivat laadullisesti samoja. Lisäyhdiste nimeltä N4', jonka m/z=578 Th ja Rt=15.66 min havaittiin kokeissa Botrytis cinerean lakkaasilla ja uutetulla PPO:lla, mutta ei Trametes Versicolorin lakkaasilla, mikä viittaa mahdollisiin eroihin. reaktiivisuus näiden entsyymien suhteen.
2.2. Fysikaalis-kemiallisten parametrien tutkimus ja optimointi 1H-NMR-fenolisissa ja alifaattisissa OH-signaaleissa
Prosyanidiinidimeerien rakenteellinen karakterisointi voidaan saada NMR-analyysillä. Erityisesti tarkka kytkentäkohta yksiköiden välillä voidaan määrittää käyttämällä HMBC- ja/tai ROESY-korrelaatiospektrejä [28,29] (kuvat S2 ja S3). Eetterityyppisen (COC) sidoksen tapauksessa hydroksyylisignaalin protonien attribuutio on välttämätöntä. Se voi myös olla ratkaisevaa CC-sidosten tapauksessa, jos jotkut alifaattiset tai aromaattiset protonit menevät päällekkäin tai jos joitain keskeisiä korrelaatioita puuttuu. Kuitenkin jopa aproottisessa liuottimessa polyfenolien hydroksyyliprotonit näyttävät usein leveinä signaaleina, joista ei voida saada rakenteellista tietoa [30]. Tämä ongelma on alustavasti käsitelty lisäämällä jälkiä
Cd(NO3)2 näyteliuoksissa. Itse asiassa OH-ryhmien 'H-leveät signaalit johtuvat näiden OH-protonien ja liuottimen tai liuenneen aineen muiden protonien välisestä molekyylien välisestä vaihdosta. Vähentämällä molekyylien välisiä sidoksia, kadmiumnitraatin läsnäolo näytteissä voi vähentää näitä vaihtoja, mikä parantaa OH-protonisignaalien terävyyttä.
2.2.1.Kadmiumin lisäyksen vaikutus
Pakastekuivauksen jälkeen viisi fraktiota N2, N3, N4, N6 ja N8 liuotettiin asetoni-dg:aan. Sitten 1D-protoni-NMR-spektrit hankittiin 25 asteessa ennen pienten kadmiumimäärien lisäämistä (kuvio 2A) ja sen jälkeen (kuvio 2B). Puhtaassa asetoni-d.:ssä kaikkien fraktioiden fenoliset OH-protonit ilmestyivät leveinä piikkinä. Kadmiumin lisäyksen jälkeen nämä protonit osoittivat erittäin erottuneita signaaleja fraktioiden N6 ja N8 tapauksessa, kun taas fraktioiden N2, N3 ja N4 signaalit olivat vain hieman terävämpiä. On myös mainittava, että Cd-pitoisuuden lisäämisellä ei ollut vaikutusta OH-signaalin erottelukykyyn, koska huipun viivanleveyden terävyyttä tai leveyttä ei havaittu, kun näytteisiin lisättiin peräkkäin pieniä määriä Cd:tä (tietoja ei esitetty).

Erittäin erottuneita fenolisia OH-signaaleja tuotteista N2, N3 ja N4 saavutettiin lisäkuivauksen ja uudelleenliuotuksen ansiosta (kuvio 2C, D).

Fraktioiden välinen käyttäytymisero Cd:n lisäyksen yhteydessä voidaan selittää molekyylien vuorovaikutusten vahvuudella: N2:n, N3:n ja N4:n tapauksessa vahvempi verrattuna N6:aan ja N8:aan, lisävaihe on välttämätön näiden sidosten katkaisemiseksi.
Tämä lisävaihe voi olla avainvaihe, kun käytetään Cd:tä erittäin erottuneiden fenolisten OH-signaalien saamiseksi missä tahansa tilanteessa riippumatta näytteiden alkuperästä, synteesireaktiosta tai luonnollisista polyfenolituotteista.
Edellinen työ, joka käsittelee yksiselitteistä rakenteellista karakterisointiapolyfenolidimeerit, jotka käyttävät erittäin erottuneita OH-fenolisia NMR-signaaleja kadmiumnitraatin lisäyksen ansiosta, julkaistiin vuonna 1996[30]. Tietojemme mukaan mitään muuta tätä menetelmää käyttävää tutkimuspaperia ei ole julkaistu sen jälkeen. Tämän tavoitteen saavuttamiseksi tehtiin myöhemmin muita tutkimuksia joko pikriinihapon lisäyksillä [31] tai käyttämällä alhaista hankintalämpötilaa [32]. Tämä voidaan selittää lisävaiheella, joka tarvitaan ratkaisevan vaikutuksen saamiseksi OH-piikin terävyyteen Cd-lisäyksellä, kuten edellä on kuvattu. Kadmium näyttää kuitenkin olevan suuri arvo, koska erittäin erottuvia signaaleja voidaan saada ilman, että tarvitsee lisätä tarkkoja määriä, toisin kuin pikriinihapon tai NMR-spektrien hankinnassa matalissa lämpötiloissa.
2.2.2. Lämpötilan vaikutus
Lämpötilan lasku 25 astetta 15 asteeseen ei vaikuttanut fenolisten OH- tai alifaattisten OH-signaalien terävyyteen. Siitä huolimatta vaihdettavien protonihuippujen alakenttäsiirtymät mahdollistivat joidenkin päällekkäisten fenolisten ja alifaattisten OH-signaalien erottamisen, mikä teki niiden tunnistamisesta selvemmän (kuva 3). Lämpötilaa laskemalla protonien vaihtonopeus pieneni ja alifaattisten OH-huippujen voitiin odottaa olevan terävämpiä [31]. 15 asteen lämpötila ei selvästikään ole tarpeeksi alhainen saadakseen hyvin erottuvia alifaattisia OH-signaaleja. Sen avulla pystyimme kuitenkin selvästi tunnistamaan kahden alifaattisen OH-protonin resonanssin näytteissä N3 ja N6 ja yhden näytteessä N8. Näytteen N2 spektrissä oli myös kaksi OH-alifaattista protonisignaalia, jotka erottuivat paremmin 25 asteessa kuin 15 asteessa (kuva 2E). Näytteen N4 tapauksessa alifaattisesta OH:sta peräisin olevat signaalit olivat vain osittain näkyvissä. spektrit, olipa lämpötila asetettu 25 asteeseen vai 15 asteeseen C jatkuvan päällekkäisyyden vuoksi (kuva 2E).

2.3. Dimeeristen standardien rakenteellinen karakterisointi – NMR-spektrianalyysi
Fraktioiden N2, N3, N4, N6 ja N8 NMR-spektrit osoittivat, että hapettumistuotteet olivat erittäin puhtaita, koska muiden havaittujen yhdisteiden signaalin intensiteetit olivat alle 10 prosenttia näiden tuotteiden vastaaviin verrattuna.
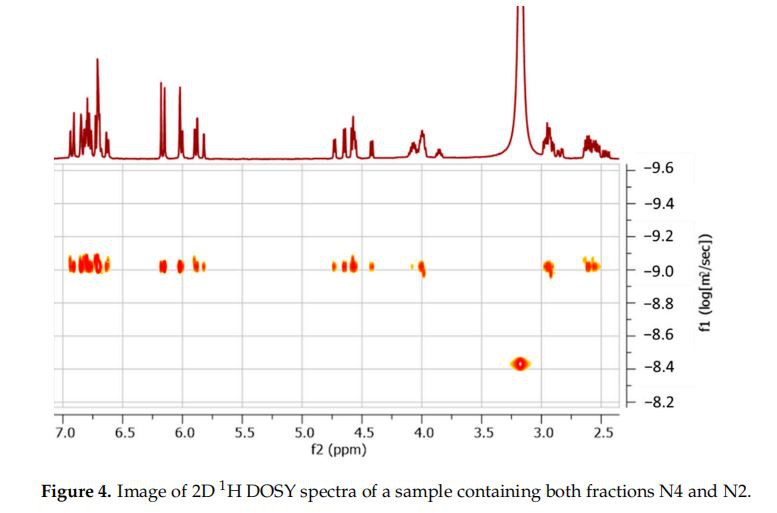
Kaikissa spektreissä voidaan erottaa neljä katekiiniyksiköille tyypillistä lH-kemiallista siirtymäaluetta (kuva 2C): pyraanirenkaiden alifaattisten protonien (C-renkaat) signaaleja löytyy alueelta 2,3-5.0 ppm, ja resorsinolirenkaiden (A-renkaat) ja katekolirenkaiden (Brings) aromaattisten signaaliprotonien 5,5 - 6,3 ppm ja 6,3 - 7,1 ppm, vastaavasti. Sekä A- että B-renkaiden OH-fenolisignaalit ilmestyivät välillä 7,1 - 10 ppm. Molempien fraktioiden NMR-spektrit osoittivat erillisten katekiiniyksiköiden signaalijoukkojen läsnäolon tasaisella intensiteettisuhteella: fraktioiden N2, N3, N6 ja N8 spektreissä havaittiin kaksi signaalisarjaa dimeerien läsnäolon mukaisesti, ja neljä sarjaa N4-spektreissä, jotka voivat vastata yhtä tetrameeriä, kahta dimeeriä tai eri oligomeerien seosta, eli yhtä trimeeriä plus yhtä monomeeriä. Fraktiossa N4 olevien tuotteiden oligomeroitumisasteen määrittämiseksi suoritettiin 'H DOSY -koe käyttämällä seosta, joka sisälsi alikvootteja molemmista fraktioista N4 ja N2. Kaikkien signaalien diffuusiokertoimet näyttivät samanlaisia arvoja (kuvio 4), mikä osoittaa kahden katekiinin dimeerin läsnäolon fraktiossa N4.
Täysin erottuneiden OH-fenolisignaalien ansiosta, jotka tarjoavat luotettavia kvantitatiivisia tuloksia, katekiiniyksiköiden välisen sidoksen tyyppi voidaan päätellä suoraan piikin pinta-alan integraatiosta. Siten molemmissa fraktioissa, N3 ja N6, yhden OH-fenolin (joka kuului joko resorsinoliin tai katekolirenkaaseen) ja yhden resorsinolin aromaattisen protonin puuttuminen osoitti eetterityyppisen interflavanisen sidoksen (IFL), mikä merkitsi oppositiota A:ssa. tai B-rengas ja C6- tai C8-asema A-renkaassa. Näytteen N2 tapauksessa puuttui kaksi aromaattista protonia, toinen B-renkaasta ja toinen A-renkaasta, mikä viittaa CA-CB IFL:ään. Fraktion N4 1D'H-spektri osoitti, että B-renkaasta puuttui kaksi protonia sekä A-renkaan kaksi protonia. Fraktion N4 dimeeriyksiköiden väliset sidokset ovat siis molemmat CC-tyyppisiä. Fraktion N8 spektrit olivat melko erilaisia kuin neljä muuta. Jotkut signaalit olivat tyypillisiä katekiiniyksiköille, joista puuttui kolme OH-fenolia, yksi aromaattinen A-rengas ja yksi B-renkaan protoni sekä yksi alifaattinen OH. Toisaalta jotkut muut NMR-signaalit ovat epätyypillisiä katekiiniyksikölle: metyleeni, jonka 13C-kemialliset siirtymät on poistettu (~40 ppm) ja ketoniryhmä (~192 ppm).
C-, A- ja B-renkaiden protoni-spin-järjestelmät määritettiin käyttämällä sekä 'H 1D- että 1H 2D TOCSY -spektrejä (ei esitetty). Fraktioiden N2, N3, N6 ja N8 spektreissä havaittiin kaksi ABMX C-rengasspin järjestelmää (tyypillistä katekiinille) ja neljä fraktiolle N4. Fraktioiden N2, N3, N6 ja N8 spektreissä kaksi metakytkettyä duplettia (J~2Hz) ja yksi aromaattisen A-rengasalueen yksittäinen osoitettiin vastaavasti kytkemättömän katekiiniyksikön A-renkaan protoneille. ja C6-- tai C8--kytketyn katekiiniyksikön A-renkaan jäännösprotoniin. N4:n spektreissä havaittiin kahden dimeerin läsnäolon vuoksi neljä metakytkettyä duplettia ja kaksi singlettiä ja osoitettiin edellä kuvatulla tavalla. B-renkaan protonijärjestelmät määritettiin myös helposti näistä spektreistä, ja niiden avulla pystyimme tunnistamaan kaksi ABM-protonin spin-järjestelmää fraktioiden N3 ja N6 dimeereille, kun taas yksi ABM- ja yksi AB-protoni spin-järjestelmä havaittiin dimeerille N2 ja yksi ABM- ja yksi AM protonin spin-järjestelmä dimeerille N4. Dimeeri N8 osoitti vain yhtä katekiinimonomeerille tyypillistä ABM B-renkaan pyörimisjärjestelmää.
2.3.1. Fraktioiden N2, N3, N4 ja N6 dimeerien IFL:n A-renkaan sijainnin määrittäminen
Dimeerien A-renkaaseen (eli C6A- tai C8A-asemaan) sijaitsevan sillan muodostaminen edellyttää CA-kytketyn katekiiniyksikön jäännös-HA-protonin määrittämistä. Erittäin erottuneiden fenolisten OH-signaalien ansiosta helppo lähtökohta oli A-renkaaseen kytkeytyneiden yksiköiden kahden OH-fenoliprotonin tunnistaminen, eli A-rengas, joka
had one isolated lHspin. This may be achieved using lH-13C long-range correlations, as illustrated in Figure5. The OH5A has readily been identified thanks to a correlation with the C4aC. This quaternary carbon is indeed characterized by both its chemical shift at~100 ppm and a long-range correlation observed with the H4Cprotons. OH5A also correlated with two other carbons∶ the most deshielded (δ>145 ppm) was obviously C5A, while the other (6>125 ppm) was C6A, which also showed a correlation with the other OHA phenol proton,i.e., OH7A. This latter correlated with two other carbons: a deshielded quaternary carbon(δ>145ppm) and a more shielded carbon(δ>125 ppm), jotka johtuivat helposti C7A:sta ja C8A:sta. Kun C6A ja C8A on osoitettu, jäännös-HA-protoni voidaan liittää suoraan HSQC-spektreihin. Siten havaittiin, että tämä jäännös-HA-protoni oli H6A kaikille fraktioille N2, N3, N4, N6. IFL katekiiniyksiköiden välillä merkitsi siten C8A-asemaa kaikille dimeereille.
2.3.2. IFL:n B-renkaan sijainnin määrittäminen
Fraktioiden N2 ja N4 dimeerit. Fraktion N2 spektrit osoittivat kahta eri tyyppistä B-renkaan protonin spin-järjestelmää: yksi AMX, joka vastasi kytkemättömän yksikön B-rengasta, ja yksi AM, jonka kytkentävakio oli noin 8 Hz, tyypillistä H6'B:lle ja H5':lle. C2'B-kytketyn yksikön B. N2-dimeerin yksiköiden välinen sidos on siis C2'B-C8A. Jakeen N4 NMR-spektrit osoittivat myös erilaisia B-spin-järjestelmiä: kaksi AMX-järjestelmää, jotka vastaavat kytkemätöntä B-rengasta, ja kaksi AX-spin-järjestelmää, jotka molemmat näyttivät noin 2 Hz:n kytkentävakiot, jotka ovat ominaisia H2'B:lle ja H6':lle. C5'B-kytkettyjen yksiköiden B-protonit. Pitkän kantaman'H/13C-korrelaatioiden läsnäolo H6'-kaistan C8A välillä, jotka havaittiin kahden dimeerin HMBC-spektreissä, ovat C5/'B-C8A-sidoksen mukaisia (kuvio 5).

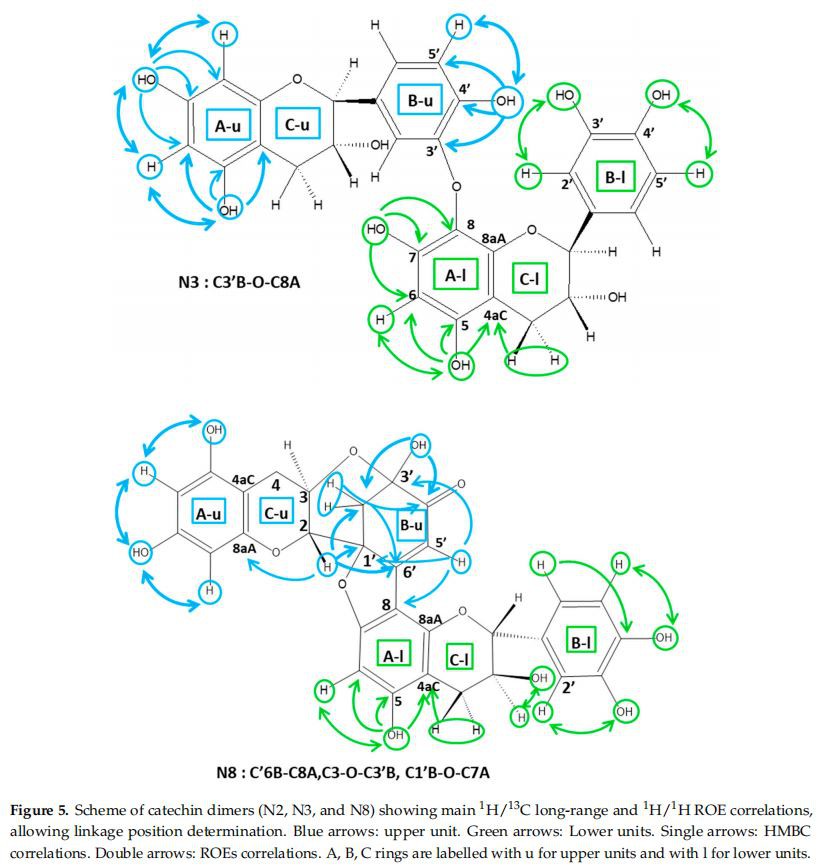
Fraktioiden N3 ja N6 dimeerit. Fraktioiden N3 ja N6 spektrit osoittivat kahden AMX B-renkaan protonijärjestelmän läsnäolon ja yhden OH-fenolisignaalin puuttumisen. Koska kaikki dimeeriyksiköiden OHA-fenoliset protonit tunnistettiin (kuten yllä on kuvattu), puuttuva OH-fenolisignaali voi olla joko OH3'B:n tai OH4'B:n signaali.
OH-asema (3'B tai 4'B) voidaan määrittää helposti ROE-korrelaatioiden avulla H2'Bor H5'B:n kanssa, tai käyttämällä pitkän kantaman HMBC-korrelaatioita, kuten kuvassa 5 on esitetty.
B-renkaiden jäännös-OH:n määrittäminen suoritettiin helposti käyttämällä joko pitkän kantaman HMBC- tai ROESY-korrelaatioita, kuten kuvassa 5. Dimeerin N3 tapauksessa havaittiin ROE-korrelaatio H5'B:n ja jäännös-OH:n välillä. 'B katekiiniyksiköstä, joka on yhdistetty sen B-renkaan kautta. Tämä OH tunnistettiin siten OH4'B:ksi. Fraktion N6 tapauksessa jäännös-OH'B määritettiin OH3'B:ksi, koska tämän OH:n ja H2'B:n välillä havaittiin ROE-korrelaatio. Pitkän kantaman HMBC-korrelaatiot ovat näiden attribuuttien mukaisia. Näiden kahden dimeerin kytkentäkohdat määritettiin sitten seuraavasti: CO3'B-C8A ja CO4'B-C8A N3:lle ja N6:lle. vastaavasti.
Fraktio N8. Dimeerin N8 spektrianalyysi osoitti, että yksi tämän dimeerin yksikkö on katekiini, jossa on kaksi kytkentäkohtaa, joista toinen on A-rengas, toinen C8A-asemassa ja toinen C-O7A-asemassa, koska protonit H8A ja OH7A ovat puuttuu. Tämän dimeerin toisella yksiköllä oli yksittäisiä spektripiirteitä, jotka osoittivat B-renkaan aromaattisuuden menetystä ja useiden sidosasemien läsnäoloa sekä B- että C-renkaissa.
B-renkaasta peräisin olevat'H-NMR-signaalit olivat kaksi duplettia 2,49 ja 2,71 ppm:ssä, jotka osoittivat metyleeniryhmälle tyypillistä -15 Hz:n (12,03 ppm) geminaalista kytkentää ja etyleenistä protonista johtuvaa singlettiä 6,38 ppm:ssä. Koska nämä metyleeni- ja eteeniprotonit eivät olleet kytkettyinä, ne ovat todennäköisesti asemissa 2'B ja 5'B. HIMBC-spektri osoitti kaikki korrelaatiot, mikä mahdollisti näiden B-renkaan hiilten tarkan attribuution, kuten kuvassa 5 on esitetty. Tämän yksikön H2C antoi kolme korrelaatiota B-renkaan hiilen kanssa: yksi on metyleenihiili noin 45 ppm:ssä, mikä johtui näin ollen C2'B ja loput kaksi, joiden hiilet resonoivat arvoilla ~90 ppm ja ~162 ppm, jotka voidaan osoittaa C1'B:lle ja C6'B:lle.H5'B antoivat vain vahvat 3J-korrelaatiot tämän B-renkaan kahden kvaternaarisen hiilen kanssa. : yksi on hiili, joka on aiemmin osoitettu C3'B:lle (~ 95 ppm), ja toinen, joka resonoi noin 90 ppm:ssä, voitaisiin siten lukea C1'B:n ansioksi. Hiilen -162 ppm:ssä pääteltiin sitten olevan C6'B.
Alifaattisen OH:n (~5,8 ppm) läsnäolo C3'B-asemassa (~95 ppm) määritettiin sen ROE-korrelaatiolla molempien H2'B-protonien kanssa. Lisäksi OH3/B antoi HMBC-korrelaation kvaternäärisen hiilen kanssa -192,5 ppm:ssä, mikä on ominaista ketoniryhmälle C4'B-asemassa.
Tämän C1'B:n noin 40 ppm:n suojaus vastaa B-renkaan aromaattisuuden menetystä. Lisäksi OH:n puute toisen yksikön C7A-asemassa on sopusoinnussa eetterisidoksen C1'BO-C7A kanssa.
NMR-tiedot osoittivat, että tämän yksikön C-renkaassa ei ole OH3C:tä. C3C-O-C3'B-sidoksen läsnäolo on sopusoinnussa C3C:n noin 1,5 ppm:n suojauksen kanssa sekä C3'B:n kemiallisen siirtymän kanssa, joka on tyypillinen hemiketaalihiilelle (95 ppm).
Kaiken kaikkiaan NMR-spektritiedot antavat meille mahdollisuuden päätellä, että tämä dimeeri vastaa dehydrokekiini A:ta, jonka ovat kuvanneet Winges et al.[33] ja sitten Guyot et al.[20].
Näillä NMR-analyyseillä määritetyn kuuden dimeerisen yhdisteen rakenteet esitetään kuviossa 6, jolloin N2, N3, N6 ja N8 ovat puhtaita tuotteita ja N4 on kahden isomeerin seos.


3. Materiaalit ja menetelmät
3.1. Kemikaalit
(plus)-katekiinihydraatti Enintään 98 prosenttia; Lakkasi Trametes Versicolorilta (0.94 U·mg-1); kaksiemäksinen natriumfosfaattidihydraatti Suurin tai yhtä suuri kuin 98 prosenttia; sitruunahappo (ACS-reagenssi, kadmiumnitraattitetrahydraatti 99,997 prosenttia; muurahaishappo ja Amberlite XAD7HP hankittiin Sigma-Aldrichilta) (Saint-Louis, MO, USA). Asetoni-dg ostettiin Euriso-topilta (Saarbrüicken, Saksa) ja happo (TFA) Roth Labolta (Karlsruhe, Saksa). Vesi LC-MS, asetonitriili LC-MS (ACN) ja metanoli LC-MS (MeOH) olivat kaikki VWR:ltä (Radnor, PA, USA).
3.2. Malliviiniliuoksen valmistus
Malliviiniliuos oli etanoli/vesiliuos (12/88;o/o), jossa oli 0,033 M viinihappoa, pH säädettiin arvoon 3,6 1 M NaOH:lla [34].
3.3. Raaka rypäleen PPO-uutteet
PPO-uute valmistettiin Singletonin et ai. [35] aiemmin kuvaamalla tavalla. Jäädytetyt viinirypäleet sekoitettiin ensin asetaattipuskurissa (1,5 M, pH 5; 10 gL-I askorbiinihappoa). Sitten seos suodatettiin ja sentrifugoitiin (3000 g; 10 min). Lopuksi jäännös pestiin asetonilla (80 %) ja ilmakuivattiin.
3.4. Lakkasi Botrytis Cinerealta
Lakkaasi Botrytis cinereasta saatiin Quijada-Morin et ai. [36] kuvaamalla tavalla. Se tuotettiin VA612-kannasta (kerätty vuonna 2005 viinitarhasta Hautvillersissä, Champagnessa, Ranskassa, Pinot Noir -lajikkeesta). Lyhyesti sanottuna viljelmät kiinteällä mallashiivaväliaineella jätettiin yhdeksi viikoksi 24 asteeseen sinisen valon alla. Sen jälkeen itiöt kaavittiin ja siirrostettiin 500 ml:n erlenmeyerpulloon, joka sisälsi 125 ml viljelyalustaa (4{{30}} gL-1glukoosia, 7 gL{{10}}glyseroli, 0,5 g·L-1L-histidiini, 0,1 g:L-1 CuSO, 1,8 gL-1 NaNO3, 0,5 g:L -1 KCl, 0,5 gL-1 CaCl2·H2O, 0,05 g:L-1 FeSO4,7H2O, 1,0 g L-1KH2PO4 ja 0,7 gL-1 MgSO 4-7H2O). Kolmen päivän inkuboinnin ja 2 päivän kasvun jälkeen samassa edellisessä alustassa esiviljelmiin lisättiin gallushappoa (2 gL-1). 5 päivän kuluttua nestemäinen väliaine suodatettiin ja supernatantti suodatettiin tangentiaalisesti Quixstand-suodatusjärjestelmässä (GE Healthcare UK, Little Chalfont, Englanti), joka oli varustettu 30 kDa:n molekyylipainon katkaisulla kalvosta. Konsentraatille suoritettiin lopuksi diasuodatus tislattua vettä vastaan, ja vain ne fraktiot, joilla oli hapettavaa aktiivisuutta ABTS:ää vastaan, säilytettiin (-80 aste).
3.5. Hapetusmenettely
Lakkaasiliuos (1 gL-1) fosfaatti-sitraattipuskurissa valmistettiin aiemmin ja lisättiin 6 g.l -1( plus )-katekiiniliuokseen (malliviini), jotta saatiin lakkaasin lopullinen pitoisuus { {6}}.3 gL-1. Saatua liuosta sekoitettiin sitten hitaasti (180 rpm) huoneenlämpötilassa 2 tuntia. Konsentraatiot optimoitiin aiemmin, ja koe suoritettiin kolmena rinnakkaisena.
3.6. Reaktion pysähtyminen Resin Amberlite XAD7HP:ssä
Meripihkanvärinen lite-kolonni käsiteltiin etanolilla (absoluuttinen) ja huuhdeltiin kahdella kolonnitilavuudella milli-O-vettä. Edellinen lakkaasi/(plus)-katekiini-reaktioväliaine tiputettiin pylvääseen ja eluoitiin ensin kahdella kolonnitilavuudella milli-Q-vettä [37]. Pylväs eluoitiin sitten etanolilla, kunnes kerätty fraktio oli väritön. Vain etanolifraktiot säilytettiin, haihdutettiin ja lyofilisoitiin. Jauhetta säilytettiin -80 asteessa käyttöön asti.
3.7. Dimeerisen fraktion puhdistusmenetelmä flash-kromatografiaa käyttäen
Lyofilisoitu jauhe puhdistettiin ensin käyttämällä flash-kromatografiajärjestelmää puriflash430, joka oli varustettu UV-detektorilla, joka oli asetettu 280 nm:iin, ja Puriflash diol 50 um f0025 -kolonnilla. Binäärinen liikkuva faasi koostui asetonitriilistä (liuotin A) ja metanolista (liuotin B), jotka molemmat oli tehty happamaksi 0,1 % TFA:lla. Sarja injektioita suoritettiin vakiovirtausnopeudella 20 ml·min-1 käyttäen seuraavaa gradienttia: 100 % A 4,4 minuuttia; 0-10 prosenttia B:tä 10 minuutissa; 10 prosenttia B:tä 5 minuutissa; 10-90 prosenttia B 5 minuutissa; 90 prosenttia B 3 minuutissa; 90-10 prosenttia B 2 minuutissa; 10 prosenttia B 10 minuutissa. Injektiotilavuus oli 1 ml (300 mg lyofilisoitua jauhetta liuotettuna 1 ml:aan liuotinta A). Kullakin kerralla kerättiin kolme erillistä fraktiota. Ensimmäinen vastasi jäännös(plus)-katekiiniä ja kolmas oli sekoitus suurimolekyylipainoisia polyfenoleja. Toinen eluoitunut fraktio, joka sisälsi dimeeristen hapetustuotteiden seoksen, haihdutettiin ja lyofilisoitiin ennen toista puhdistusvaihetta.
3.8. Dimeerifraktiosta peräisin olevien hapetustuotteiden puhdistusmenetelmä puolivalmistekromatografiajärjestelmää käyttäen
Dimeerisiä hapetustuotteita sisältävä fraktio puhdistettiin käyttämällä puolipreparatiivista Bio-Rad NGC 10 keskipainekromatografiajärjestelmää, joka oli varustettu käänteisfaasi Varian Dynamax C18 Microsorb -kolonnilla (250 × 21,2 mm; 3 um). Binäärinen liikkuva faasi koostui milli-O-vedestä (liuotin A) ja 80 prosentista asetonitriilistä, 20 prosentista Milli-Q-vedestä (liuotin B), jotka molemmat oli tehty happamaksi 0,05 prosentilla TFA:ta. Sarja injektiot (300 µl) lyofilisoitua jauhetta (20 mg liuotettuna 200 ul:aan liuotinta A ja 100 ul:aan ACN:a) suoritettiin seuraavissa eluointiolosuhteissa: 100 % A 4 minuuttia; 0-35 prosenttia B 46 minuutissa; 35-100 prosenttia B 2 minuutissa; 100 prosenttia B 5 minuutissa. Joka kerta kerättiin kahdeksan erillistä fraktiota, jotka vastaavat puhtaita UPLC-signaaleja 280 nm:ssä. Jokainen fraktio haihdutettiin ja lyofilisoitiin ennen NMR-analyysiä.
3.9 Näytteen valmistelu NMR-analyysiä varten
Noin 1 mg kutakin lyofilisoitua jauhetta, joka oli punnittu Eppendorf-putkiin, liuotettiin 500 µl:aan asetoni-dg. Sitten näytteisiin lisättiin ~10 ui väkevää kadmiumnitraatin liuosta asetoni-d:ssä ja saadut liuokset siirrettiin 5 mm:n NMR-putkiin NMR-analyysiä varten. Joillekin näytteille suoritettiin lisävaihe: sen jälkeen, kun lyofilisoidut jauheet oli liuotettu asetoni-dg:hen kadmiumin jäännösten läsnä ollessa, näytteet haihdutettiin kuiviin ja liuotettiin sitten uudelleen asetoni-d:hen lisäämättä Cd:tä.
3.10. Laitteen tekniset tiedot
UPLC-MS-analyysi. Reaktioita seurattiin käyttämällä kahta UPLC-MS-järjestelmää. Ensimmäistä menetelmää käytettiin tuotteiden retentioaikojen täsmälliseen tunnistamiseen pitkällä gradienttimenetelmällä. eli Watersin käänteisfaasin ultrakorkean suorituskyvyn nestekromatografia yhdistettynä massaspektrometriaan (UHPLC-MS). Nestekromatografiajärjestelmä oli Acquity UPLC (Waters, Milford, MA, USA), joka oli varustettu fotodiodirividetektorilla. Käytimme Acquity UPLC HSS T3 -kolonnia (1,8 um, 2,1 × 15 0 mm). Kolonnin lämpötila oli 25 astetta. Binäärinen liikkuva faasi koostui 0,1 % muurahaishaposta vedessä (liuotin A) ja asetonitriilistä (liuotin B). Erotus suoritettiin vakiovirtausnopeudella 0,25 ml·min-1 käyttäen seuraavaa gradienttia: 8-11 prosenttia B 2 minuutissa; 11 prosenttia B 8 minuuttia; 11-25 prosenttia Bin 15 minuutissa; 25-55 prosenttia Bin 5 min; 55-99 prosenttia Bin 1 min; 99 prosenttia B 4 min; 99-8 prosenttia Bin1 min; 8 prosenttia Bin 4 min ajan. Injektiotilavuus oli 5 µl. Massaspektrometri oli Waters Acquity QDa electrospray ionization (ESI) yksinkertainen kvadrupoli (Waters, Milford, MA, USA). Kapillaarijännite asetettiin 0,8 kV:iin. Massaspektrit saatiin massaalueella 200-900 Ohut positiivinen ionimoodi.
Toinen UHPLC-MS-järjestelmä, jota käytettiin nopeaan todentamiseen puhdistusvaiheiden aikana, oli sama kuin aiemmin kuvattu, Acquity UHPLC HSS T3 -kolonni (1,8 μm, 2,1 × 100 mm) lämmitettynä. 38 asteessa. Erotus suoritettiin vakiovirtausnopeudella 0,55 ml·min-1 käyttäen seuraavaa nopeaa gradienttia: 0.1-40 prosenttia B 5 minuutissa; 40-99 prosenttia B 2 minuutissa; 99 prosenttia B:tä 1 minuutin ajan; 99-0,1 prosenttia B 1 minuutissa. Injektiotilavuus oli 2 µl. Massaspektrometri oli Bruker Amazon X electrospray ionization (ESI) -ioniloukku (Bruker Daltonics, Bremen, Saksa). Kapillaarijännite asetettiin arvoon -5,5 kV. Massaspektrit saatiin massaalueella 50-2000 Ohut positiivinen ionimoodi.
Kaikki UPLC-MS-analyysit suoritettiin kolmena rinnakkaisena.
NMR-instrumentointi. Kaikki NMR-spektrit tallennettiin Agilent DD{{0}} MHz spektrometrillä (Agilent Technologies, Santa Clara, CA, USA), joka toimi taajuuksilla 500,05 ja 125,74 MHz protoni- ja hiili-13-ytimille, vastaavasti käyttämällä 5 mm:n epäsuoraa havainnointianturia, joka oli varustettu gradienttikelalla.1D'H ja 13C,2Dhomonuclear1H TOCSY ja ROESY sekä heteronukleaarinen lH/13C HSQC ja HMBC. Kokeet suoritettiin käyttäen klassisia pulssisekvenssejä ja analysoitiin käyttämällä sekä VNMRJ4.2:ta että 13C:tä1 MestRe2.2:ta. .1 (Mestrelab Research, Espanja) -ohjelmisto. DOSY-mittaukset hankittiin ja käsiteltiin aiemmin kuvatulla tavalla 38]. DgcsteSL-pulssisekvenssin hankintaparametrit olivat seuraavat: diffuusioviiveeksi ja gradientin pulssin leveydeksi asetettiin 50 ms ja 2 ms, vastaavasti, gradientin voimakkuutta (g) lisättiin 16 askeleessa yhtä suurella g2-välillä 0,3:sta 32 G·cm-I. Vaihekorjauksen jälkeen 2D DOSY -spektrit muodostettiin huipun korkeuden mittauksesta VNMRJ4.2-ohjelmistolla.
Kaikki spektrit verrattiin liuottimen asetoni-dg-signaaleihin ('H-jäännössignaali 2,05 ppm:ssä ja 13C-signaali 29,92 ppm:ssä).

4. Johtopäätökset
Kolmen erilaisen oksidoreduktaasin (rypäleistä uutettu polyfenolioksidaasi, Botrytis cinereasta lakkaasi ja Trametes Versicolorin lakkaasi) vaikutusta (plus)-katekiiniin tutkittiin, ja tuloksena saadut LC-UV-MS-profiilit olivat hyvin samankaltaisia, vaikkakin pieniä eroja. ehdotti mahdollisia eroavaisuuksia näiden entsyymien reaktiivisuudessa.
Kuuden katekiini-lakaasi-hapetustuotteen rakenteet (käyttäen Trametes Versicolorin lakkaasia) saatiin spesifisten NMR-signatuurien perusteella (neljä puhdasta tuotetta eli N2, N3, N6 ja N8 ja N4, jotka vastaavat seosta kaksi isomeeriä). Fenolisten OH-signaalien täydellinen antaminen oli mahdollista kadmiumnitraatin lisäämisen ansiosta näytteenvalmistusmenettelyllä, joka mahdollisti joidenkin kiinnostavien yhdisteiden katekiiniyksiköiden välisten sidosten yksiselitteisen antamisen. Tämä menetelmä yksinkertaistaa huomattavasti polyfenoliseosten NMR-analyysiä, joko syntetisoituja tai luonnontuotteista uutettuja.
Tässä työssä saatuja standardeja voidaan jatkossa käyttää hapettumismerkkiaineina tutkittaessa niiden esiintymistä ja kehitystä rypäleiden kypsymisen ja viinin ikääntymisen aikana. Katekiinin lisäksi muita polyfenoliyhdisteitä, mukaan lukien flavonoidit ja ei-flavonoidit, voidaan käyttää lakkaasin substraatteina uusien lisästandardien saamiseksi.
Lyhenteet
NMR: ydinmagneettinen resonanssi,
CD: kadmium,
TOCSY: kokonaiskorrelaatiospektroskopia,
ROESY: Pyörivän rungon ydin Overhauser-efektispektroskopia,
HSQC: heteronukleaarinen yhden kvantin korrelaatiokoe,
HMBC: heteroydin monikaistayhteys,
DOSY: diffuusiojärjestetty spektroskopia.
Viitteet
1. Khan, N.; Mukhtar, H. Tea polyfenolit terveyden edistämiseen. Life Sci. 2007, 81, 519–533. [CrossRef]
2. Fayeulle, N.; Vallverdu-Queralt, A.; Meudec, E.; Hue, C.; Boulanger, R.; Cheynier, V.; Sommerer, N. Fermentoiduissa kaakaopavuissa olevien uusien flavan{2}ol-johdannaisten karakterisointi. Food Chem. 2018, 259, 207–212. [CrossRef] [PubMed]
3. Rimbach, G.; Melchin, M.; Moehring, J.; Wagner, AE Polyfenolit kaakaosta ja verisuonten terveys – kriittinen katsaus. Int. J. Mol. Sci. 2009, 10, 4290–4309. [CrossRef]
4. Avram, AM; Morin, P.; Brownmiller, C.; Howard, LR; Sengupta, A.; Wickramasinghe, SR Polyfenolipitoisuudet mustikan puristemassauutteesta nanosuodatuksella. Food Bioprod. Prosessi. 2017, 106, 91–101. [CrossRef]
5. Antoniolli, A.; Fontana, AR; Piccoli, P.; Bottini, R. Polyfenolien karakterisointi ja antioksidanttikapasiteetin arviointi Cv:n rypäleen puristemassassa. Malbec. Food Chem. 2015, 178, 172–178. [CrossRef]
6. Saucier, C. Miten viinin polyfenolit kehittyvät viinin ikääntymisen aikana? Cerevisia 2010, 35, 11–15. [CrossRef]
7. Oliveira, CM; Ferreira, ACS; De Freitas, V.; Silva, AMS Viineissä esiintyvät hapetusmekanismit. Food Res. Int. 2011, 44, 1115–1126. [CrossRef]
8. Singleton, VL Happi fenolien kanssa ja siihen liittyvät reaktiot rypälemehuissa, viineissä ja mallijärjestelmissä: Havainnot ja käytännön vaikutukset. Olen. J. Enol. Vitic. 1987, 38, 69–77.
9. Mathew, AG; Parpia, HAB Elintarvikkeiden ruskistuminen polyfenolireaktiona. In Advances in Food Research; Chichester, CO, Mrak, EM, Stewart, GF, toim.; Academic Press: Cambridge, MA, USA, 1971; Osa 19, s. 75–145. [CrossRef]
10. Gambuti, A.; Rinaldi, A.; Ugliano, M.; Moio, L. Fenoliyhdisteiden kehittyminen ja supistaminen punaviinin ikääntymisen aikana: Happialtistuksen vaikutus ennen ja jälkeen pullotuksen. J. Agric. Food Chem. 2013, 61, 1618–1627. [CrossRef] [PubMed]






