Osa 1: Finerenonin kardiovaskulaariset ja munuaisvaikutukset potilailla, joilla on tyypin 2 diabetes ja krooninen munuaissairaus: FIDELITY-yhdistelmäanalyysi
May 26, 2022
Lisätietoja: ottaa yhteyttätina.xiang@wecistanche.com
Tavoitteet
Täydentävät tutkimukset FIDELIO-DKD ja FIGARO-DKD potilailla, joilla oli tyypin 2 diabetes ja krooninen munuaissairaus (CKD), tarkastelivat sydän- ja verisuonisairauksia ja munuaisten tuloksia CKD:n eri, päällekkäisissä vaiheissa. FIDELITY-analyysin tarkoituksena oli suorittaa yksilöllinen potilastasolla ennalta määritetty yhdistetty teho- ja turvallisuusanalyysi laajasta kroonisesta munuaistaudista, jotta saataisiin luotettavampia arvioita finerenonin turvallisuudesta ja tehosta lumelääkkeeseen verrattuna.
Menetelmät ja tulokset
For this prespecified analysis, two-phase, multicentre, double-blind trials involving patients with CKD and type 2 diabetes, randomized 1:1 to finerenone or placebo, were combined. Main time-to-event efficacy outcomes were a composite of cardiovascular death, non-fatal myocardial infarction, non-fatal stroke, or hospitalization for heart failure, and a composite of kidney failure, a sustained >57% decrease in estimated glomerular filtration rate from baseline over >4 viikkoa. tai munuaiskuolema. 13 026 potilaalla, joiden seurannan mediaani oli 3.0 vuotta (neljännesten välinen vaihteluväli 2.3-3,8 vuotta), yhdistetty kardiovaskulaarinen lopputulos esiintyi 825 (12,7 prosenttia) potilaalla, jotka saivat finerenoni ja 939 (14,4 prosenttia ) lumelääkettä saaneita Hazard ratio (HR), 0.86:95 prosentin luottamusväli(C), 0.78-0.95: P {{20}}.0018]. Yhdistelmä munuaistulos esiintyi 360 (5,5 prosenttia) potilaalla, jotka saivat finerenonia ja 465 (7,1 prosenttia) lumelääkettä (HR, 0,77; 95 prosenttia Cl, 0.67-0.88;P=0.0002) . Yleiset turvallisuustulokset olivat yleensä samanlaisia hoitoryhmien välillä. Hyperkalemiaa, joka johti hoidon pysyvään keskeyttämiseen, esiintyi useammin potilailla, jotka saivat finerenonia (1,7 prosenttia) kuin lumelääkettä (0,6 prosenttia).
Johtopäätös
Finerenoni vähensi kliinisesti merkittävien sydän- ja verisuonisairauksien ja munuaissairauksien riskiä lumelääkkeeseen verrattuna kroonisessa munuaissairauspotilailla tyypin 2 diabetesta sairastavilla potilailla.
Keskeinen kysymys
Vähentääkö finerenoni, uusi selektiivinen, ei-steroidinen mineralokortikoidireseptorin antagonisti, joka sietää reniini-angiotensiinijärjestelmän estoa, sydän- ja verisuonisairauksia ja munuaissairauden etenemistä useissa kroonisissa munuaissairauksissa tyypin 2 diabetesta sairastavilla potilailla?
Avaimen löytäminen
In a prespecified, pooled individual-level analysis from two randomized trials, we found reductions both in cardiovascular events and kidney failure outcomes with finerenone. Because 40% of the patients had an estimated glomerular filtration rate of>60 mlmin/1,73m ne tunnistettiin yksinomaan albuminuriaan perustuen.
Viesti kotiin
Finerenoni vähentää kliinisten kardiovaskulaaristen tulosten ja munuaissairauden etenemisen riskiä monilla potilailla, joilla on krooninen munuaissairaus ja tyypin 2 diabetes. Albuminuria-seulonta riskipotilaiden tunnistamiseksi tyypin 2 diabetesta sairastavien potilaiden joukosta helpottaa sekä sydän- ja verisuonitautien että munuaisten sairauksien taakkaa.
Avainsanat
Kardiorenaaliset seuraukset · Krooninen munuaissairaus · Finerenoni ·Sairaalahoito sydämen vajaatoiminnan vuoksi ● Hyperkalemia · Tyypin 2 diabetes
Napsauta tätä saadaksesi lisätietoja cistanche tubulosa -uutteen eduista
Johdanto
Potilaat, joillakrooninen munuaissairaus(CKD) jatyypin 2 diabeteson korkea jäännöskardioreaalinensairastuvuus ja kuolleisuus nykyisistä hoidoista huolimatta sekä munuaisten vajaatoiminnan ja sydän- ja verisuonitapahtumien etenemisen riskit lisääntyvät kroonisen taudin vaikeusasteen ja vaiheen myötä. Verrattuna potilaisiin, joilla on edennyt munuaissairaus ja jotka todennäköisemmin etenevät dialyysihoitoon, potilailla, joiden arvioitu glomerulussuodatusnopeus (eGFR) on paremmin säilynyt, on suurempi elinikäinen riski saada sydän- ja verisuonisairauksia, kuten sydämen vajaatoiminta, sydäninfarkti (M), aivohalvaus tai kuolema sydän- ja verisuonisairauksiin.
Todisteet viittaavat siihen, että mineralokortikoidireseptorin (MR) yliaktivoituminen johtaatulehdusja fibroosi sydämessä, munuaisissa ja verisuonistoon, jossa MR ilmentyy laajasti, mikä voi aiheuttaa kroonista munuaista jasydän-ja verisuonitautietenemistä. Finerenoni on uusi, selektiivinen, ei-steroidinen MR-antagonisti (MRA), joka estää MR-välitteisen natriumin reabsorption ja MR-yliaktivaation ja on osoittanut anti-inflammatorisia ja antifibroottisia vaikutuksia prekliinisissä munuais- ja sydän- ja verisuonitautimalleissa.89 FInerenoni vähentää munuaisten vajaatoimintaa. ja taudin eteneminen diabeettisessa munuaissairaudessa (FIDELIO-DKD) ja FINerenoni sydän- ja verisuonikuolleisuuden ja sairastuvuuden vähentämisessä diabeettisessa munuaissairaudessa (FIGARO-DKD) -vaiheen 1 tutkimukset ovat toisiaan täydentäviä ominaisuuksien, kuten niiden samankaltaisen suunnittelun ja päätepisteiden, vuoksi. Yhdessä ne muodostavat tähän mennessä suurimman sydän- ja munuaissairauksien hoitoon liittyvän ohjelman tyypin 2 diabeteksessa. He tutkivat finerenonin tehoa ja turvallisuutta suurimman siedetyn reniini-angiotensiinijärjestelmän eston lisäksi munuais- ja sydän- ja verisuonisairauksiin potilailla, joilla oli lievä tai vaikea CKD tyypin 2 diabeteksessa (lisämateriaali verkossa, kuva S1). FIDELIO-DKD:ssä finerenoni vähensi merkittävästi riskiä primaarisen munuaisyhdistelmätuloksen ja keskeisen sekundaarisen sydän- ja verisuonikomposiittisen lopputuloksen riskiä potilailla, joilla oli pääasiallisesti vaiheen 3-4 krooninen munuaistauti, jossa albuminuria on lisääntynyt ja tyypin 2 diabetes. FIGARO-DKD:ssä finerenoni vähensi merkitsevästi primaarista kardiovaskulaarista komposiittisen lopputuloksen riskiä laajemmassa potilaspopulaatiossa kuin tutkittiin FIDELIO-DKD:ssä (potilaat, joilla oli vaiheen 2-4 CKD ja kohtalaisesti lisääntynyt albuminuria tai vaiheen 1-2 CKD, jossa vakava lisääntyminen albuminuria).710
FIDELIO-DKD-tutkimus suunniteltiin havaitsemaan finerenonin hoitovaikutus munuaisten vajaatoiminnan päätepisteisiin, kun taas FIGARO-DKD-tutkimuksen tavoitteena oli havaita vaikutus sydän- ja verisuonijärjestelmän yhdistettyyn ensisijaiseen päätepisteeseen.710 Parantaa kykyä havaita hoidon vaikutus munuaisiin. potilaat, joilla oli korkeampi virtsan albumiini-kreatiniinisuhde (UACR), valittiin ensisijaisesti FIDELIO-DKD-tutkimukseen. Jotta saataisiin aikaan suurempi munuaisten vajaatoiminnasta vapaa aika kardiovaskulaaristen tapahtumien hoitovaikutuksen havaitsemiseksi, FIGARO-DKD:ssä valittiin populaatio, jolla oli kohtalainen UACR ja laajempi eGFR-alue. Näin ollen nämä kaksi koetta täydensivät toisiaan hieman päällekkäin tutkituissa populaatioissa, ja niiden samankaltainen suunnittelu ja päällekkäiset tutkimuspaikat mahdollistivat tulosten vertailun ja yhdistämisen.
Finenenonin tehoa ja turvallisuutta ei ole kuitenkaan täysin arvioitu tyypin 2 diabeteksen kroonisessa munuaissairauskirjeessä. Fnerenoni kroonisessa munuaissairaudessa ja tyypin 2 diabeteksessa: Yhdistetty FIDELIO-DKD- ja FIGARO-DKD-koeohjelman analyysi (FIDELITY) yhdistää nämä täydentävät tutkimukset samanlaisiin suunnitelmiin, arviointeihin ja käytäntöön. FIDELITY:n ennalta määritellyn yhdistetyn analyysin tarkoituksena oli antaa tarkempia arvioita finerenonin tehosta ja turvallisuudesta kroonisesti kroonista munuaistautia ja tyypin 2 diabetesta sairastavien potilaiden joukossa, jotta voidaan taata tuloksia useilla potilailla sellaisella tarkkuudella, jota ei ollut mahdollista saada. tarkastelemalla kahta koetta erikseen.

menetelmät
Opintojen suunnittelu
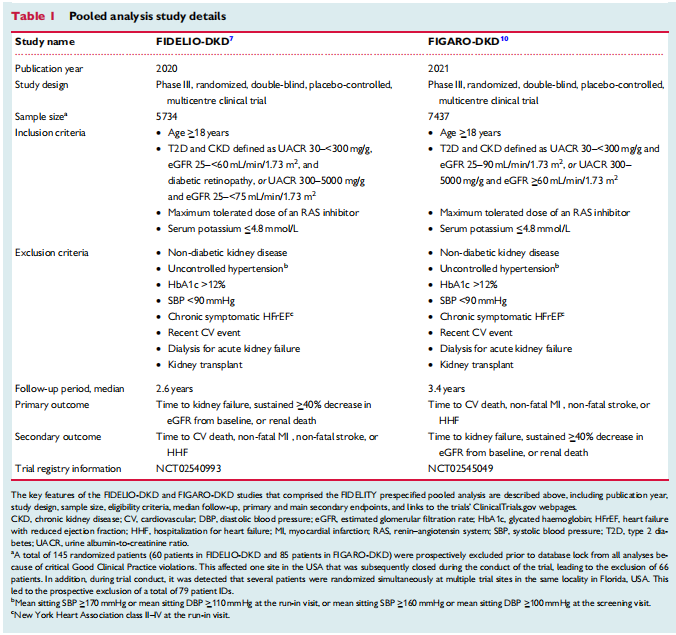
Tämä ennalta määrätty yhdistetty teho- ja turvallisuusanalyysi, joka määriteltiin etukäteen virallisessa tilastollisessa analyysisuunnitelmassa, yhdistää tiedot FIDELIO-DKD:stä (NCT02540993) ja FIGARO-DKD:stä (NCTO2545049), kaksivaiheisesta III, satunnaistetusta, kaksoissokkoutetusta, lumekontrolloidusta, monikeskuskliiniset tutkimukset (taulukko 1 ja lisämateriaali verkossa, kuva S2). Tutkimussuunnitelman ja tutkimusprotokollan yksityiskohdat on julkaistu aiemmin.11 Potilaat
Tukikelpoiset potilaat olivat aikuisia (yli 18-vuotiaita), joilla oli tyypin 2 diabetes ja krooninen munuaistauti ja joita hoidettiin suurimmalla siedetyllä annoksella angiotensiinia konvertoivan entsyymin estäjää (ACEi) tai angiotensiinireseptorin salpaajaa (ARB).
Krooninen munuaissairaus FIDELIO-DKD:ssä
CKD FIDELIO-DKD:ssä määriteltiin joko:(i) pysyväksi (osoitettu sekä sisäänajo- että seulontakäynneillä, jotka tapahtuivat vähintään 4–16 viikon välein), kohtalaisen lisääntyneeksi albuminuriaksi (UACR suurempi kuin tai yhtä suuri kuin 30-<300mg )="" with="" an="" egfr="" of=""><60ml in/1.73="" m²="" and="" the="" presence="" of="" diabetic="" retinopathy,="" or(i)="" persistent,="" severely="" increased=""><5000mg )and="" an="" egfr="" of=""><75ml in/1.73="">
Krooninen munuaissairaus FIGARO-DKD:ssä
CKD in FIGARO-DKD was defined as either:(i) persistent, moderately increased albuminuria (UACR >30-<300mg )="" with="" an="" egfr="" of=""><90ml in/1.73="" m²,="" or="" (i)="" persistent,="" severely="" increased="" albuminuria="" (uacr=""><5000mg )and="" an="" egfr="" ≥60ml/min/1.73="" m².="" patients="" in="" both="" trials="" had="" to="" have="" serum="" potassium≤4.8mmol/l="" at="" both="" the="" run-in="" and="" screening="" visits.="" other="" key="" exclusion="" criteria="" included="" a="" clinical="" diagnosis="" of="" symptomatic="" chronic="" heart="" failure="" with="" reduced="" ejection="" fraction="" (ie.,="" a="" class="" ia="" recommendation="" for="" mra="" treatment).="" inclusion="" and="" exclusion="" criteria="" are="" listed="" in="" the="" supplementary="" material="" online,="">
Menettelyt
FIDELIO-DKD- ja FIGARO-DKD-tutkimusten menettelyt on kuvattu aiemmin. Lyhyesti sanottuna kelvolliset potilaat satunnaistettiin 1:1 saamaan suun kautta annettavaa finerenonia (10 tai 20 mg) tai lumelääkettä. Molemmat tutkimukset käsittivät sisäänajon, seulonnan, kaksoissokkohoidon ja turvallisuuden seurantajaksot (lisämateriaalia verkossa, kuva S2).10 Sisäänajojakso vaati ACEi- tai ARB-hoidon säätämistä suurimmaksi siedetyksi merkittyyn annokseen. joka ei johtanut ei-hyväksyttäviin sivuvaikutuksiin. Tutkimuslääke hylättiin, jos kaliumpitoisuudet ylittivät 5,5 mmol/l ja aloitettiin uudelleen, kun kaliumpitoisuus laski<5.0mmol .="" further="" details="" are="" found="" in="" the="" supplementary="" material="" online,="">
Tulokset
The outcome definitions for FIDELIO-DKD and FIGARO-DKD have been described previously.10 The efficacy outcomes selected for this analysis were either a primary or a secondary outcome or those prespecified in the hierarchical outcomes in the complementary studies. The eff-cacy outcomes of interest for this pooled analysis were a composite cardiovascular outcome of time to cardiovascular death, non-fatal MI, non-fatal stroke, or hospitalization for heart failure(HHF), and a composite kidney outcome of time to the first onset of kidney failure, sustained >57 prosentin lasku eGFR:ssä lähtötilanteesta yli 4 viikkoa tai yhtä suuri kuin 4 viikkoa tai munuaiskuolema. Sisään
yhdistetty munuaistulos, munuaisten vajaatoiminta määriteltiin loppuvaiheen munuaissairaudeksi (ESKD) tai eGFR:n jatkuvaksi laskuksi<15 ml/min/1.73="" m2,="" and="" eskd="" was="" defined="" as="" the="" initiation="" of="" chronic="" dialysis(for="">90days) or kidney transplantation. Other prespecified outcomes included: a second composite kidney outcome of time to the first occurrence of kidney failure, sustained >40% decrease in eGFR from baseline over >4 viikkoa tai munuaiskuolema; aika kaikkiin syihin liittyvään kuolleisuuteen; aika kaikista syistä sairaalahoitoon; ja UACR:n muutos lähtötasosta 4 kuukauteen.
The eGFR ≥40% composite kidney outcome was the primary or secondary outcome in the complimentary trials.10 However, a sustained >57% decrease in eGFR(equivalent to doubling of serum creatinine)was selected in FIDELITY because it is a classic outcome in diabetic nephropathy studies.12-14and is a more robust kidney failure surrogate outcome than a ≥40% decrease in eGFR, particularly when initial changes in eGFR occur.415 This outcome was selected before data pooling and analysis. Furthermore, the eGFR>57 prosentin tulos oli ennalta määritetty tulos ilmaiskokeissa.
Turvallisuusanalyyseissä haittatapahtumia pidettiin hoitoon liittyvinä, jos ne alkoivat tai pahenivat tutkimuslääkkeen käytön aikana tai enintään 3 päivää tilapäisen tai pysyvän keskeytyksen jälkeen. Hyperkalemian hoitomenettely on kuvattu aiemmin.

Tilastolliset analyysit
Tilastolliset analyysit olivat ennalta määrättyjä tutkivia arvioita eikä hypoteesin vahvistavia. Tilastolliset testit, joissa P-arvot on annettu, olivat tutkivia; sen vuoksi oikaisua monikertaisuuden suhteen ei tehty.
Täysi analyysisarja käsitti kaikki satunnaistetut potilaat [lukuun ottamatta niitä, joilla oli kriittisiä hyvän kliinisen käytännön (GCP) rikkomuksia, jotka jätettiin erittäin hyvin pois kaikista analyyseistä]. Turvallisuusanalyysit suoritettiin turvallisuusanalyysisarjassa, joka määriteltiin kaikiksi satunnaistetuiksi potilaiksi, joilla ei ollut kriittisiä GCP-rikkomuksia ja jotka ottivat enemmän tai yhtä kuin 1 annoksen tutkimuslääkettä. Tutkimustulokset analysoitiin käyttämällä kerrostettuja Coxin suhteellisia vaaramalleja, jotka on sovitettu käyttämällä kerrostustekijöitä: tutkimus, alue (Pohjois-Amerikka, Latinalainen Amerikka, Eurooppa, Aasia ja muut), eGFR-luokka seulonnassa (25-<><60, and="" ≥60mlmin/1.73="" m),="" albuminuria="" category="" (moderately="" increased="" and="" severely="" increased)="" at="" screening,="" and="" a="" history="" of="" cardiovascular="" dis-ease="" (present="" or="" absent;="" see="" supplementary="" material="" online,="" appendix,="" for="" further="" details).p-values="" for="" the="" comparison="" of="" treatment="" groups="" are="" presented="" based="" on="" a="" stratified="" log-rank="" test="" treatment="" effects="" are="" expressed="" as="" hazard="" ratios(hrs)="" with="" corresponding="" 95%="" confidence="" intervals(cls)="" from="" the="" stratified="" cox="" proportional="" hazards="" models.="" events="" were="" counted="" from="" randomization="" up="" to="" the="" end-of-study="" visit="" and="" patients="" without="" an="" event="" were="" censored="" at="" the="" date="" of="" their="" last="" contact="" with="" complete="" information="" on="" all="" components="" of="" the="" respective="" outcome.="" the="" time-to-event="" analysis="" reporting="" included="" first="" events="" only.="" events="" based="" on="" a="" sustained="" decrease="" in="" egfr="" were="" considered="" in="" the="" analysis="" from="" randomization="" up="" until="" 5="" months="" after="" the="" last="" egfr="" was="" recorded="" at="" a="" clinic="" visit.="" for="" subgroup="" analyses,="" hrs="" were="" derived="" from="" stratified="" cox="" proportional="" hazards="" models,="" including="" a="" treatment="" sub-group="" and="" a="" subgroup="" by="" treatment="" interaction="" term="" as="" fixed="">
Kumulatiivinen ilmaantuvuus, joka perustui siihen, että Aalen-Johansen piti kuolleisuutta kilpailevana riskinä ja vastaavat hoitoon tarvittavat luvut, laskettiin 6-kuukauden välein kardiovaskulaarisen yhdistelmätuloksen ja munuaissairauksien keskeisen yhdistetyn tuloksen osalta. Kaplan-Meieriin perustuvat kumulatiivinen ilmaantuvuus laskettiin kaikesta kuolleisuudesta. Hoidon aikana suoritettu herkkyysanalyysi suoritettiin tuloksille ottaen huomioon vain tapahtumat, jotka tapahtuivat 30 päivään asti tutkimuslääkkeen lopettamisen jälkeen koko analyysisarjassa.
Sponsori Bayer suoritti tilastolliset analyysit, ja kaikki kirjoittajat pääsivät käsiksi tietoihin ja osallistuivat niiden tulkintaan. Kaikki analyysit suoritettiin käyttämällä SAS-ohjelmistoa, versiota 9.4 (SAS Institute, Cary, NC, USA). Muita tilastollisia menetelmiä löytyy Täydentävästä materiaalista verkossa, liitteestä.

