Osa Ⅰ: Liikalihavuuden vaikutus munuaissairauksiin
Apr 11, 2023
Abstrakti
Liikalihavuuden kliiniset seuraukset munuaisissa, aineenvaihduntahäiriöiden kanssa tai ilman, liittyvät munuaisten toimintaan ja rakenteeseen. Liikalihavuuden ja munuaisvaurion yhdistävät mekanismit tunnetaan hyvin, ja niihin sisältyy useita toisiinsa liittyviä vaikutusmekanismeja. Suuremman virtsan albumiinin erittymisen, subnefroottisen oireyhtymän, munuaiskivien, lisääntyneen CKD-riskin ja ESKD:n etenemisen on havaittu liittyvän liikalihavuuteen ja niillä on merkittäviä kliinisiä vaikutuksia. Lisäksi lihavuus vaikuttaa myös munuaiskorvaushoitoon ja munuaisensiirtoon. Painonpudotus on avainasemassa liikalihavuuden munuaisvaikutusten rajoittamisessa vähentämällä proteinuriaa/proteinuriaa, hidastamalla eGFR:n heikkenemistä, viivästyttäen CKD:n ja ESKD:n etenemistä ja parantamalla munuaisensiirtotuloksia. Painonpudotus edesauttaa myös kardiometabolisten riskitekijöiden, kuten verenpainetaudin, metabolisen oireyhtymän, diabeteksen ja dyslipidemian, asianmukaista hallintaa, jotka voivat suojata paitsi munuaisvaurioilta myös sydän- ja verisuonisairauksilta. Nämä edut on osoitettu elämäntapamuutoksilla, joillakin lääkkeillä ja bariatrisella kirurgialla.
Avainsanat
liikalihavuus; rasvainen munuainen; glomerulopatia; CKD; ESRD; bariatrinen kirurgia ;Cistanche-lisäuute.

Napsauta tätä saadaksesi tietääCistanchen vaikutukset munuaisiin
Johdanto
Lihavuusepidemian jatkuva kasvu tuo mukanaan joukon sairauksia, jotka ylittävät lihavuuden klassisen tunnustetut metaboliset, ortopediset, psykologiset ja kardiovaskulaariset seuraukset. Tämän lisäksi, vaikka liikalihavuuden vaikutukset liittyvätkin jollain tapaa liikalihavuuteen, munuaisiin kohdistuvat vaikutukset ovat yleensä hiljaisia vuosia ennen kuin aiheuttavat siihen liittyviä vaurioita kliinisissä ilmenemismuodoissa. Epidemiologisia, mekanistisia, kliinisiä ja terapeuttisia näkökohtia tarkastellaan uudelleen.
1. Epidemiologia
Riippumattomia, asteittainen korrelaatioita heikentyneen GFR-arvioiden ja kuolemanriskin, sydän- ja verisuonitapahtumien ja sairaalahoidon välillä raportoitiin suurella yhteisöpohjaisella aikuisväestöllä integroidussa terveydenhuoltojärjestelmässä, joilla seerumin kreatiniini mitattiin vuosina 1996-2000 ja jotka eivät saaneet dialyysihoitoa tai munuaishoitoa. elinsiirto. Kun GFR laski arvosta 59:stä 45:een (ml/min/1,73 m2), kuolinriski nousi 1,8:aan, ja loppuvaiheen munuaissairautta [1] sairastavien potilaiden kuolemanriski saavutti vähitellen korkeimman arvonsa, lähes kuusinkertainen. lisääntyä. Samanlaisia tuloksia CKD:n etenemisen ja sydän- ja verisuonitautien ja kuoleman välillä on raportoitu meta-analyysitutkimuksissa [2,3]. 1990-luvun lopulta 2000-luvun alkuun säätämättömän vaiheen 3 ja 4 CKD:n esiintyvyys lisääntyi Yhdysvalloissa ja diabeteksen, verenpainetaudin ja liikalihavuuden esiintyvyys lisääntyi. Yleinen esiintyvyys kuitenkin vakiintui vuosina 2003–2004, ja 6,9 prosentilla väestöstä oli krooninen munuaistauti vuosina 2011–2012. Huolimatta Yhdysvaltojen väestön jatkuvasta ikääntymisestä ja liikalihavuuden lisääntymisestä, CKD:n yleisen esiintyvyyden viimeaikainen vakiintuminen on katsottu paremman hallinnan ansioksi. verenpainetauti, onnistunut glykeeminen hallinta uusilla lääkkeillä ja [4] proteinuriapotilaiden laajennettu käyttö lääkkeissä, jotka salpaavat reniini-angiotensiinijärjestelmää. Isossa-Britanniassa eGFR<60 mL/min/ 1-73 m2 was 7.7%, 7.0%, and 7.3% in 2003, 2009/2010, and 2016, respectively, before starting to decline in 2010 and rising again in 2016 [5]. Meanwhile, in the UK, the prevalence of diabetes and obesity increased between 2003 and 2016, while the prevalence of hypertension and smoking decreased.
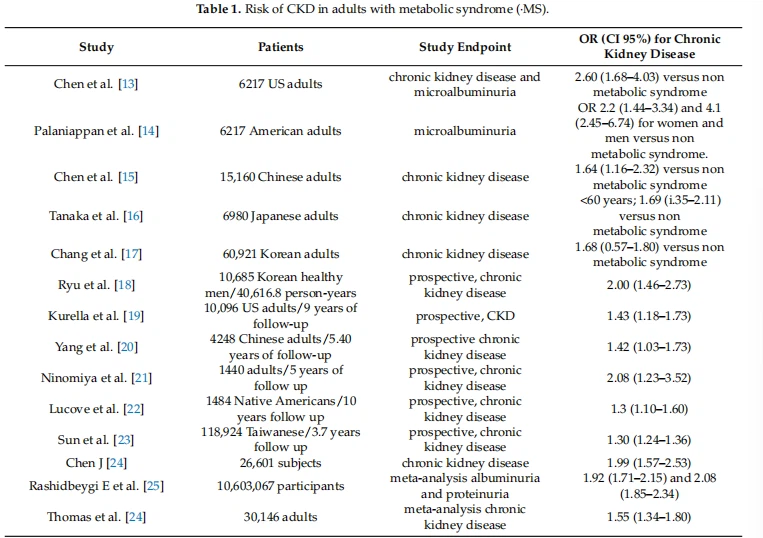
Sen lisäksi, että diabeteksen ja verenpainetaudin vaikutus lisääntyneeseen CKD-riskiin liikalihavilla potilailla, liikalihavuuden suora rooli munuaisvaurioissa on osoitettu eläinmalleissa ja ihmisepidemiologisissa tutkimuksissa. Useimmissa tutkimuksissa BMI:n ilmoitettiin olevan riippumaton merkittävä tekijä kroonisen munuaisten vajaatoiminnan kehittymiselle [{{0}}], ja BMI:n ja ESKD:n suhde vaihteli alhaisesta korkeimpaan arvoon 1,273 iän mukauttamisen jälkeen. sukupuoli, systolinen verenpaine ja proteinuria [6], mutta muissa tutkimuksissa lihavuusriski näytti olevan pääasiassa diabeteksen ja verenpainetaudin välittäjä [8] tai se ei liittynyt ESKD:hen [11]. Hiljattain tehty meta-analyysi yleisväestöstä, jonka munuaisten toiminta oli lähtötilanteessa normaali, raportoi, että liikalihavuus lisäsi alhaisen eGFR:n suhteellista riskiä 1,28:lla ja proteinurian riskiä 151 miljoonalla b0. Taulukkoon 1 on koottu tutkimuksia kroonisen taudin riskistä aikuisilla, joilla on metabolinen oireyhtymä.
Kansallisen kolesterolikoulutusohjelman mukaan ei-diabeettiset osallistujat, joilla oli normaali munuaisten toiminta ja metabolinen oireyhtymä, otettiin mukaan yhteisön ateroskleroosiriskitutkimukseen, jonka CKD:n riski oli 1,43 verrattuna osallistujiin, joilla ei ollut metabolista oireyhtymää [19]. Keskirasvojen jakautumisindeksi eli vyötärön ja lonkan ympärysmitta tai sisäelinten rasvakudos liittyi paremmin ESKD-riskiin verrattuna BMI:hen [26-28 ]. Meta-analyysi raportoi, että metabolisen oireyhtymän komponentit, kuten liikalihavuus, heikentynyt paastoglukoosi, kohonnut verenpaine ja hypertriglyseridemia, liittyivät merkittävästi lisääntyneeseen proteinurian ja albuminuriaan [25].
Metabolisesti terve lihavuus (MHO) on liikalihavuuden fenotyyppi, jossa lihavuuteen ei liity metabolisia komplikaatioita, kuten insuliiniresistenssiä, tulehdusta, verenpainetautia tai T2D:tä. Verrattuna metabolisesti terveeseen ei-lihavaan fenotyyppiin MHO:ssa esiintyvien kroonisten munuaistautien suhde oli samanlainen kuin kontrolleissa, mutta sekaannuksiin sopeutumisen jälkeen CKD:n suhde lisääntyi merkittävästi metabolisesti epänormaalissa ei-lihavassa fenotyypissä ja lihavassa fenotyypissä. 29-31]. Muut tutkimukset ovat kuitenkin raportoineet, että MHO:lla voi olla keskimääräinen riski saada ESKD.

Herba Cistanche
2. Patologia
Liikalihavuuteen liittyvä glomerulopatia
Munuaisen fyysinen puristuminen peri-orgaanisen rasvakudoksen kerääntyessä korostaa viskeraalisen liikalihavuuden mahdollista merkitystä munuaissairauden kehittymisessä. Solunulkoiset matriksikertymät, jotka leviävät koko munuaisytimen alueelle, ovat laajentuneet ja perivaskulaarisella kudoksella on taipumus luistaa Bellini-kanavan vaskulaarisessa napassa. Lihavilla potilailla munuaisten interstitiaaliset solut lisääntyvät, ja runsaasti lipidejä ja proteoglykaaneja sisältävä materiaali puristaa munuaisen parenkyymiä kohti munuaisnapaa muodostaen pyöreän, laajentuneen munuaisen. Munuaisten puristus vaikuttaa sekä vaskulaarisiin (suorat verisuonet) että putkimaisiin (Henryn sivut) elementteihin, mikä johtaa RAS-aktivoitumiseen ja lisääntyneeseen natriumin takaisinabsorptioon [32-34].
Tärkeimmät histologiset piirteet ovat muutama fokaalisegmentaalinen glomeruloskleroosivaurio, glomerulusten hyalinoosi, vakavaan glomerulusten laajentumiseen johtava fibroosi, glomerulusten lipidien kertyminen ja Bowmanin vaippaadheesioita [33,36]. Muutokset munuaisten lipidiaineenvaihdunnassa aiheuttavat lipidien kertymistä, mikä viittaa siihen, että runsaalla rasvan käytöllä voi olla suora lipotoksinen vaikutus munuaisiin. Ektooppinen lipidien kerääntyminen munuaiseen voi aiheuttaa rakenteellisia ja toiminnallisia muutoksia tylakoidisoluissa, podosyyteissä ja proksimaalisissa tubulussoluissa. Munuaisten poskionteloiden ympärillä oleva rasva näyttää osallistuvan verisuonten toimintaan, mikä muuttaa verenkiertoa alla olevissa valtimoissa. Liikalihavuus lisää munuaisten massaa ja glomerulusten halkaisijaa. Podosyyttien on laajennettava prosessejaan kattamaan laajentunut alue, mikä johtaa podosyyttien irtoamiseen, selektiiviseen proteiinien menetykseen, paljaiden alueiden muodostumiseen, laukaisee matriisin kerrostumisen ja johtaa podosyyttien vaurioitumiseen.
Glomerulaariset muutokset liikalihavuuden aiheuttamassa munuaisvauriossa eroavat diabeettisen nefropatian vastaavista, koska ensimmäisellä on vähäisempi muutosaste tylakoiditilassa. Proteinuriaa, proteinuriaa ja ESKD:tä havaitaan useammin potilailla, joilla on diabeettinen nefropatia kuin lihavilla nefropatialla, jonka lopputulos on hitaampi ja eteneminen harvemmin loppuvaiheen munuaissairauteen. Runsaan rasvan saannin lisäksi muita munuaisvaurion syitä voivat olla Ang II:n yli-ilmentyminen, joka johtaa lisääntyneisiin proliferatiivisiin tekijöihin, kuten transformoivan kasvutekijän (TGF-) ja fibrinogeeniaktivaattorin estäjiin, sekä insuliinin määrään, joka johtaa solujen kasvuun. Natriumin reabsorption aiheuttama liiallinen suodatus lisää veren virtausta munuaisiin, mikä aiheuttaa fysikaalisen leikkausjännityksen aiheuttaman munuaiskerästen seinämän progressiivisen skleroosin, mikä käynnistää vaarallisen syklin: munuaissoluvauriot, jotka johtavat apoptoosiin, natriumin retentio vähenee ja verenpaineen nousu natriumin homeostaasin ylläpitämiseksi. . Nefroottisen alueen proteinuria on harvinainen liikalihavilla yksilöillä, mutta sitä voi myös esiintyä [35,37]. Nämä havainnot viittaavat siihen, että liikalihavuuteen liittyvä munuaisvaurio tulisi määritellä fokaalisegmenttisen glomeruloskleroosin spesifiseksi muodoksi, joka etenee hitaasti loppuvaiheen munuaissairaudeksi. Potilailla, joilla on metabolinen oireyhtymä, on suuri esiintyvyys mikrovaskulaarisia sairauksia, jotka ilmenevät tubulaarisena atrofiana, interstitiaalisena fibroosina ja arterioskleroosina [38].
3. Endoteelin toimintahäiriö ja muutokset verisuonten rakenteessa
Endoteelin toimintahäiriöllä on tärkeä rooli CKD:n ja proteinurian patogeneesissä [50]. Insuliiniresistenssi, alhaiset lipokaliinitasot, korkeat plasman leptiinitasot, kohonneet plasman glukoositasot ja FFA:t indusoivat tulehdusta, mikä johtaa endoteelin toimintahäiriöön, mikä johtaa lisääntyneeseen munuaisten proteiinin menetykseen.
Endoteelisolut tuottavat typpioksidia (NO), ja se edistää vasodilataatiota ja vähentää tulehdusta ja verihiutaleiden aggregaatiota. Fosfatidyyli-inositoli-3-kinaasiaktivaatio johtaa endoteelin NO-syntaasien (e-NO:iden) fosforylaatioon, jotka tuottavat NO:ta [51]. Liikalihavuus liittyy NO:n biologisen hyötyosuuden vähenemiseen. Insuliiniresistenssin läsnäollessa tämä reitti heikkenee, kun taas hyperinsulinemia lisää endoteliini-1-tasoja, mikä johtaa epätasapainoon verisuonia laajentavien ja verisuonia supistavien endoteelitekijöiden välillä, mikä johtaa verenpaineeseen [52,53]. Verisuonten soluadheesiomolekyyli-1 (VCAM-1), solujen välinen adheesiomolekyyli-1 (ICAM-1) ja e-selektiini lisäävät monosyyttien kiinnittymistä verisuonen seinämään aiheuttaen ateroskleroosi. Nämä verisuonitekijät edistävät verenkiertoa, mikä johtaa munuaisvaurioihin ja verenpaineeseen.

Cistanche-uutteen edut
4. Mekanismit
CKD:n rakenteellisten poikkeavuuksien mekanismit liittyvät liikalihavuuden ja l:n rinnakkaissairauksiin, nimittäin kohonneeseen verenpaineeseen, insuliiniresistenssiin, tyypin 2 diabetekseen ja aterogeeniseen dyslipidemiaan, jotka johtavat munuaisvaurioihin mekanismien, kuten tulehduksen, kautta. l Oksidatiivinen stressi, RAAS-sääntely, lisääntynyt SNS-aktiivisuus ja endoteelin toimintahäiriö johtavat lopulta munuaisvaurioihin [39].
Hemodynamiikka
Sympaattisen hermoston (SNS) aktivoitumisen uskotaan olevan tärkeä rooli liikalihavien henkilöiden verenpainetaudin ja CKD:n patogeneesissä (40 Plasman reniiniaktiivisuus osoittaa merkittävästi liikalihavuuden lisääntymistä, samoin kuin paikallisen perivaskulaarisen rasvakudoksen angiotensiini ll:n (33). Angiotensiini ll nostaa efferenttejä valtimoita glomeruluksessa tuottaen TGF-, fibroosia ja podosyyttien apoptoosia Liikalihavuuteen liittyvien munuaisvaurioiden alkuvaiheessa e-GFR lisääntyy tilavuuden ylikuormituksen aiheuttaman hyperperfuusion vuoksi. Lisääntynyt fyysinen voima munuaisissa, jotka syntyvät rasvan kertymisestä munuaisytimen ympärille ja sisään, heikentävät suodoksen virtausnopeutta Henlen renkaassa ja havaitaan natriumin retentiota (33). Nämä varhaiset muutokset voidaan kumota painonpudotuksilla, suolarajoitteilla ja reniinin estämisellä. angiotensiinijärjestelmä.
Tulehdus
Krooninen matala-asteinen tulehdus kehittyy paikallisesti makrofagien laajennetuissa rasvasoluissa, mutta muuttuu systeemiseksi vapauttamalla proinflammatorisia välittäjäaineita (mukaan lukien sytokiinit) verenkiertoon. Kohonneet vapaiden rasvahappojen (FFA) tasot lihavilla yksilöillä voivat lisätä verisuonten A-adrenergistä herkkyyttä, estää Na plus, K plus -ATPaasia, ja natriumpumput lisäävät verisuonten sileän lihaksen sävyä ja verisuonten vastustuskykyä, aktivoivat epidermaalisen kasvutekijän reseptoreita, tuottavat reaktiivista happea. lajit ja proteiinikinaasi c. Adiposyyteissä tuotetaan erilaisia bioaktiivisia sytokiinejä, mukaan lukien reaktiiviset happilajit, tulehdusta edistävät molekyylit ja tulehdusmolekyylit (interleukiini -1, interleukiini-6, tuumorinekroositekijä, c-reaktiivinen proteiini), angiogeeniset tekijät (vaskulaarinen endoteelin kasvutekijä), hemostaattiset säätelyyhdisteet (fibrinogeeniaktivaattorin estäjä-1, trombospondiini A2), akuutin faasin vasteproteiinit (seerumin amyloidi A, c-reaktiivinen proteiini), ydintekijä κ -aktivoidun B:n kevytketjun tehostaja solujen (NF-κB) ja IKB-kinaasin (IKK) aktivaatio, mikä edistää endoteelin toimintahäiriötä ja mikrovaskulaarisia sairauksia [33]. Erilaiset patofysiologiset mekanismit voivat edistää CKD:n kehittymistä, kuten ureemisten toksiinien, pääasiassa trimetyyliamiini-n-oksidin (TMAO), tuotanto, ennaltaehkäisevän lyhytketjuisen rasvahapon väheneminen, lisääntyneet tulehdus- ja immuunivasteet, vähentynyt typpioksidi (NO), ja peptidit, jotka salpaavat angiotensiini i:tä konvertoivia entsyymejä [41].
Hormonit
Insuliiniresistenssi indusoi glomerulusten suodatusta, endoteelin toimintahäiriötä, lisääntynyttä verisuonten läpäisevyyttä, verisuonten uudissuonittumista ja muita proteinuriaan liittyviä mikrovaskulaarisia vaurioreittejä [42]. Hyperglykemia aktivoi reittejä, jotka lisäävät edistyneiden glykosylaation lopputuotteiden (AGE:iden) tuotantoa, aktivoivat proteiinikinaasi C -isoformeja ja lisää transformoivaa kasvutekijää, joka edistää solunulkoisen matriisin tuotantoa tylakoidisolujen kautta ja indusoi munuaisfibroosia [43]. Podosyytit estävät proteinurian kohdistamalla aktiinirungon varren. Podosyyttien määrän vähenemistä ja podosyyttivarsien katoamista on raportoitu diabeetikoilla, joilla on varhainen munuaisten vajaatoiminta. Insuliinin rooli podosyyteissä on kriittinen glomerulaariselle toiminnalle ja rakenteelle, mikä vaikuttaa morfologiaan, solun tukirangan uusiutumiseen ja viime kädessä eloonjäämiseen [44].
Leptiini on pieni peptidihormoni, jota tuotetaan rasvakudoksessa ja jonka määrä lisääntyy liikalihavien potilaiden veressä. Kierrettävä leptiini sitoutuu rasvakudokseen ja säätelee ravinnon saantia vapauttamalla muita välittäjäaineita hypotalamuksesta. Leptiini muuttaa insuliinin toimintaa, indusoi angiogeneesiä, vähentää endoteelin NO-syntaasia ja on vuorovaikutuksessa immuunijärjestelmän kanssa. Leptiini poistuu munuaisten kautta ja lisääntyy ESKD-potilailla, joilla on krooninen munuaisten vajaatoiminta, johon liittyy anoreksia ja painonpudotus. Leptiini laukaisee TGF:n erittymisen - glomerulaaristen endoteelisolujen toimesta, ja herkistyneet tylakoidisolut voivat reagoida TGF:ään - indusoidakseen fokaalisen glomeruloskleroosin ja proteinurian kehittymisen [45]. Muita leptiinin vaikutuksia munuaisiin ovat natriureesi, lisääntynyt sympaattinen aktiivisuus ja reaktiivisten happilajien stimulaatio [33].
Lipokaliini, rasvakudoksesta peräisin oleva peptidihormoni, jonka määrä vähenee lihavilla henkilöillä, toimii lipolyyttisenä tekijänä ja säätelee insuliiniherkkyyttä. Lipokaliini estää ateroskleroottista prosessia estämällä vaahtosolujen muodostumista. Liikalihavuudelle on ominaista lipokaliinin puute. Plasman lipokaliinitasot korreloivat negatiivisesti insuliinitasojen kanssa. Lipocalin knockout -hiirillä on ruokavaliosta riippuvainen insuliiniresistenssi ja ateroskleroosi [33]. Lipokaliini lisää AMPK-aktiivisuutta ja vähentää jalkasolujen läpäisevyyttä [46,47]. Lopuksi resistiini, monosyyttien-makrofagien tuottama tulehduksellinen adipokiini, lisääntyy potilailla, joilla on matala GFR [48]. Verenpainetautia ja diabetesta sairastavilla aikuisilla verenkierron resistiinitasot liittyvät glomerulusten suodatusnopeuteen ja proteinuriaan [49].
Cistanche tubulosa
Viitteet
1. Mene, AS; Chertow, GM; Fan, D.; McCulloch, CE; Hsu, C.-Y. Krooninen munuaissairaus ja kuoleman riskit, sydän- ja verisuonitapahtumat ja sairaalahoito. N. Engl. J. Med. 2004, 351, 1296–1305.
2. Matsushita, K.; Van Der Velde, M.; Astor, BC; Woodward, M.; Levey, AS; De Jong, PE; Coresh, J.; Gansevoort, RT Arvioidun munuaiskerästen suodatusnopeuden ja albuminurian yhdistäminen kaikkiin syihin ja sydän- ja verisuoniperäiseen kuolleisuuteen yleisväestökohorteissa: Yhteistyöllinen meta-analyysi. Lancet 2010, 375, 2073–2081.
3. Nitsch, D.; Grams, M.; Sang, Y.; Black, C.; Cirillo, M.; Djurdjev, O.; Iseki, K.; Jassal, SK; Kimm, H.; Kronenberg, F.; et ai. Arvioidun glomerulussuodatusnopeuden ja albuminurian yhteydet kuolleisuuteen ja munuaisten vajaatoimintaan sukupuolen mukaan: meta-analyysi. BMJ 2013, 346, f324.
4. Murphy, D.; McCulloch, CE; Lin, F.; Banerjee, T.; Bragg-Gresham, JL; Eberhardt, MS; Morgenstern, H.; Pavkov, ME; Saran, R.; Powe, NR; et ai. Kroonisen munuaissairauden esiintyvyyden suuntaukset Yhdysvalloissa. Ann. Harjoittelija. Med. 2016, 165, 473–481.
5. Hounkpatin, HO; Harris, S.; Fraser, SDS; Day, J.; Mindell, JS; Taal, MW; O'Donoghue, D.; Roderick, PJ Kroonisen munuaissairauden esiintyvyys aikuisilla Englannissa: kansallisesti edustavien poikkileikkaustutkimusten vertailu vuosina 2003–2016. BMJ Open 2020, 10, e038423.
6. Iseki, K.; Ikemiya, Y.; Kinjo, K.; Inoue, T.; Iseki, C.; Takishita, S. Painoindeksi ja loppuvaiheen munuaissairauden kehittymisen riski seulotussa kohortissa. Kidney Int. 2004, 65, 1870–1876.
7. Polemiti, E.; Baudry, J.; Kuxhaus, O.; Jäger, S.; Bergmann, MM; Weikert, C.; Schulze, MB BMI ja BMI muuttuvat tyypin 2 diabeteksen sattuessa ja mikrovaskulaaristen ja makrovaskulaaristen komplikaatioiden riski: EPIC-Potsdamin tutkimus. Diabetologia 2021, 64, 814–825.
8. Stengel, B.; Tarver-Carr, ME; Powe, NR; Eberhardt, MS; Brancati, FL Lifestyle Factors, Lihavuus ja kroonisen munuaissairauden riski. Epidemiology 2003, 14, 479–487.
9. Othman, M.; Kawar, B.; El Nahas, AM Liikalihavuuden vaikutus ei-diabeettisen kroonisen munuaissairauden etenemiseen: Retrospektiivinen kohorttitutkimus. Nephron 2009, 113, c16–c23.
10. Nowak, KL; Sinä, Z.; Gitomer, B.; Brosnahan, G.; Torres, VE; Chapman, AB; Perrone, RD; Steinman, TI; Abebe, KZ; Rahbari-Oskoui, FF; et ai. Ylipaino ja liikalihavuus ennustavat varhaisen autosomaalisen hallitsevan polykystisen munuaistaudin etenemistä. J. Am. Soc. Nephrol. 2017, 29, 571–578.
11. Brown, RN; Mohsen, A.; Green, D.; Hoefifield, RA; Summers, LK; Middleton, RJ; O'Donoghue, DJ; Kalra, PA; Uusi, DI-painoindeksi ei vaikuta kroonisen munuaissairauden etenemisnopeuteen ei-diabeettisilla henkilöillä. Nephrol. Soita. Elinsiirto. 2012, 27, 2776–2780.
12. Garofalo, C.; Borrelli, S.; Minutolo, R.; Chiodini, P.; De Nicola, L.; Conte, G. Järjestelmällinen katsaus ja meta-analyysi viittaavat siihen, että liikalihavuus ennustaa kroonisen munuaissairauden puhkeamisen väestössä. Kidney Int. 2017, 91, 1224–1235.
13. Chen, J.; Muntner, P.; Hamm, LL; Jones, DW; Batuman, V.; Fonseca, V.; Whelton, PK; Hän, J. Metabolinen oireyhtymä ja krooninen munuaissairaus yhdysvaltalaisilla aikuisilla. Ann. Harjoittelija. Med. 2004, 140, 167–174.
14. Palaniappan, L.; Carnethon, M.; Fortmann, SP Mikroalbuminurian ja metabolisen oireyhtymän välinen yhteys: NHANES III. Olen. J. Hypertens. 2003, 16, 952–958.
15. Chen, J.; Gu, D.; Chen, C.-S.; Wu, X.; Hamm, LL; Muntner, P.; Batuman, V.; Lee, C.-H.; Whelton, PK; Hän, J. Assosiaatio metabolisen oireyhtymän ja kroonisen munuaissairauden välillä kiinalaisilla aikuisilla. Nephrol. Soita. Elinsiirto. 2007, 22, 1100–1106.
16. Tanaka, H.; Shinohara, Y.; Uezu, Y.; Higa, A.; Iseki, K. Metabolinen oireyhtymä ja krooninen munuaissairaus Okinawassa, Japanissa. Kidney Int. 2006, 69, 369–374.
17. Chang, I.; Han, JH; Myung, SC; Kwak, KW; Kim, T.-H.; Park, SW; Choi, NY; Chung, WH; Ahn, SH Yhteys metabolisen oireyhtymän ja kroonisen munuaissairauden välillä Korean väestössä. Nephrology 2009, 14, 321–326.
18. Ryu, S.; Chang, Y.; Woo, H.-Y.; Lee, K.-B.; Kim, S.-G.; Kim, D.-I.; Kim, WS; Suh, B.-S.; Jeong, C.; Yoon, K. Metabolisen oireyhtymän ja CKD:n riskin välinen aikariippuvainen yhteys korealaisilla miehillä, joilla ei ole hypertensiota tai diabetesta. Olen. J. Kidney Dis. 2009, 53, 59–69.
19. Kurella, M.; Lo, JC; Chertow, GM-metabolinen oireyhtymä ja kroonisen munuaissairauden riski ei-diabeettisten aikuisten keskuudessa. J. Am. Soc. Nephrol. 2005, 16, 2134–2140.
20. Yang, T.; Chu, C.-H.; Hsu, C.-H.; Hsieh, P.-C.; Chung, T.-C.; Bai, C.-H.; S.-L.; Hwang, L.-C.; Lin, C.-M.; Sun, C.-A. Metabolisen oireyhtymän vaikutus kroonisen munuaissairauden ilmaantuvuuteen: Kiinalainen kohorttitutkimus. Nephrology 2012, 17, 532–538.
21. Ninomiya, T.; Kiyohara, Y.; Kubo, M.; Yonemoto, K.; Tanizaki, Y.; Doi, Y.; Hirakata, H.; Iida, M. Metabolinen oireyhtymä ja CKD yleisessä japanilaisessa väestössä: Hisayama-tutkimus. Olen. J. Kidney Dis. 2006, 48, 383–391.
22. Lucove, J.; Vupputuri, S.; Heiss, G.; North, K.; Russell, M. Metabolinen oireyhtymä ja CKD:n kehittyminen Amerikan intiaaneilla: The Strong Heart Study. Olen. J. Kidney Dis. 2008, 51, 21–28.
23. Sun, F.; Tao, Q.; Zhan, S. Metabolinen oireyhtymä ja kroonisen munuaissairauden kehittyminen 118 924 ei-diabeettisten taiwanilaisten keskuudessa retrospektiivisessä kohortissa. Nephrology 2010, 15, 84–92.
24. Thomas, G.; Sehgal, AR; Kashyap, SR; Srinivas, TR; Kirwan, JP; Navaneethan, SD Metabolinen oireyhtymä ja munuaistauti: Systemaattinen katsaus ja meta-analyysi. Clin. J. Am. Soc. Nephrol. 2011, 6, 2364–2373.
25. Rashidbeygi, E.; Safabakhsh, M.; Aghdam, SD; Mohammed, SH; Alizadeh, S. Metabolinen oireyhtymä ja sen komponentit liittyvät suurempaan albuminuria- ja proteinurian riskiin: todisteita meta-analyysistä 10 603 067 koehenkilöllä 57 tutkimuksesta. Diabetes Metab. Syndr. Clin. Res. Rev. 2018, 13, 830–843.
26. França, AKTDC; Dos Santos, AM; Salgado, JV; Hortegal, EV; Da Silva, AAM; Filho, NS Arvioitu viskeraalinen rasvakudos, mutta ei kehon massaindeksi, liittyy kystatiini C:hen perustuvaan glomerulaarisen suodatusnopeuden vähenemiseen kroonisen munuaissairauden varhaisissa vaiheissa. Int. J. Nephrol. 2014, 2014, 574267.
27. Kittiskulnam, P.; Thokanit, NS; Katavetin, P.; Susanthitaphong, P.; Srisawat, N.; Praditpornsilpa, K.; Tungsanga, K.; Eiam-Ong, S. Liikalihavuuden ja metabolisen oireyhtymän suuruus diabeettisen kroonisen munuaissairauden väestössä: valtakunnallinen tutkimus. PLoS ONE 2018, 13, e0196332.
28. Zammit, AR; Katz, MJ; Derby, C.; Bitzer, M.; Lipton, RB Krooninen munuaissairaus ei-diabeettisilla iäkkäillä aikuisilla: Metabolisen oireyhtymän, tulehduksen ja insuliiniresistenssin liittyvät roolit. PLoS ONE 2015, 10, e0139369.
29. Yun, H.-R.; Kim, H.; Park, JT; Chang, TI; Yoo, T.-H.; Kang, S.-W.; Choi, KH; Sung, S.; Kim, SW; Lee, J.; et ai. Liikalihavuus, aineenvaihduntahäiriöt ja kroonisen taudin eteneminen. Olen. J. Kidney Dis. 2018, 72, 400–410.
30. Chen, H.-Y.; Lu, F.-H.; Chang, C.-J.; Wang, R.-S.; Yang, Y.-C.; Chang, Y.-F.; Wu, J.-S. Aineenvaihduntahäiriöt, mutta ei liikalihavuus sinänsä, jotka liittyvät krooniseen munuaissairauteen taiwanilaisessa väestössä. Nutr. Metab. Cardiovasc. Dis. 2020, 30, 418–425.
31. Adair, KE; Bowden, RG; Funderburk, LK; Forsse, JS; Ylitalo, KR Aineenvaihdunta, liikalihavuus ja munuaisten toiminta: 2013–2018 Kansalliset terveys- ja ravitsemustutkimustutkimukset. Elämä 2021, 11, 888.
32. Rocchini, AP Liikalihavuus hypertensio*1. Olen. J. Hypertens. 2002, 15, S50–S52.
33. Kotsis, V.; Stabouli, S.; Papakatsika, S.; Rizos, Z.; Parati, G. Lihavuuden aiheuttaman hypertension mekanismit. Hypertensistä. Res. 2010, 33, 386–393.
34. Hall, JE; Crook, ED; Jones, DW; Wofford, MR; Dubbert, PM Liikalihavuuteen liittyvien sydän- ja munuaissairauksien mekanismit. Olen. J. Med. Sci. 2002, 324, 127–137.
35. Kambham, N.; Markowitz, GS; Valeri, AM; Lin, J.; D'Agati, VD Liikalihavuuteen liittyvä glomerulopatia: nouseva epidemia. Kidney Int. 2001, 59, 1498–1509.
36. Deji, N.; Kume, S.; Araki, S.-I.; Soumura, M.; Sugimoto, T.; Isshiki, K.; Chin-Kanasaki, M.; Sakaguchi, M.; Koya, D.; Haneda, M.; et ai. Rakenteelliset ja toiminnalliset muutokset runsasrasvaisen ruokavalion aiheuttamien liikalihavien hiirten munuaisissa. Olen. J. Physiol. Munuaiset. Physiol. 2009, 296, F118–F126.
37. Serra, A.; Romero, R.; Lopez, D.; Navarro, M.; Esteve, A.; Perez, N.; Alastrue, A.; Ariza, A. Munuaisvaurio erittäin lihavilla potilailla, joilla on normaali munuaisten toiminta. Kidney Int. 2008, 73, 947–955.
38. Alexander, kansanedustaja; Patel, TV; Farag, YM; Florez, A.; Rennke, HG; Singh, AK Munuaisten patologiset muutokset metabolisessa oireyhtymässä: poikkileikkaustutkimus. Olen. J. Kidney Dis. 2009, 53, 751–759.
39. Redon, J.; Lurbe, E. Munuaiset lihavuudessa. Curr. Hypertensistä. Tasavalta 2015, 17, 43.
40. Kotsis, V.; Jordan, J.; Micic, D.; Finer, N.; Leitner, DR; Toplak, H.; Tokgozoglu, L.; Athyros, V.; Elisaf, M.; Filippatos, TD; et ai. Liikalihavuus ja sydän- ja verisuoniriski. J. Hypertens. 2018, 36, 1427–1440.
41. Antza, C.; Stabouli, S.; Kotsis, V. Suoliston mikrobisto munuaissairauksissa ja verenpainetaudissa. Pharmacol. Res. 2018, 130, 198–203.
42. Groop, P.-H.; Forsblom, C.; Thomas, MC Taudin mekanismit: Reittiselektiivinen insuliiniresistenssi ja diabeteksen mikrovaskulaariset komplikaatiot. Nat. Clin. Harjoittele. Endokrinol. Metab. 2005, 1, 100–110.
43. Dronavalli, S.; Duka, I.; Bakris, GL Diabeettisen nefropatian patogeneesi. Nat. Clin. Harjoittele. Endokrinol. Metab. 2008, 4, 444–452.
44. De Cosmo, S.; Menzaghi, C.; Prudente, S.; Trischitta, V. Insuliiniresistenssin rooli munuaisten vajaatoiminnassa: näkemyksiä mekanismista ja epidemiologisista todisteista. Nephrol. Soita. Elinsiirto. 2012, 28, 29–36.
45. Wolf, G.; Chen, S.; Han, DC; Ziyadeh, FN Leptiini ja munuaissairaus. Olen. J. Kidney Dis. 2002, 39, 1–11.
46. Rutkowski, JM; Wang, ZV; Park, ASD; Zhang, J.; Zhang, D.; Hu, MC; Moe, OW; Susztak, K.; Scherer, PE Adiponektiini edistää toiminnallista palautumista podosyyttiablaation jälkeen. J. Am. Soc. Nephrol. 2013, 24, 268–282.
47. Przybyci ´nski, J.; Dziedziejko, V.; Puchałowicz, K.; Doma ´nski, L.; Pawlik, A. Adiponektiini kroonisessa munuaissairaudessa. Int. J. Mol. Sci. 2020, 21, 9375.
48. Axelsson, J.; Bergsten, A.; Qureshi, A.; Heimbürger, O.; Bárány, P.; Lönnqvist, F.; Lindholm, B.; Nordfors, L.; Alvestrand, A.; Stenvinkel, P. Kroonisen munuaissairauden kohonneet resistiinitasot liittyvät glomerulusten suodatusnopeuteen ja tulehdukseen, mutta eivät insuliiniresistenssiin. Kidney Int. 2006, 69, 596–604.
49. Ellington, AA; Malik, AR; Klee, GG; Turner, ST; Sääntö, AD; Mosley, JTH; Kullo, IJ Plasmaresistiinin ja glomerulusten suodatusnopeuteen ja albuminuriaan yhdistäminen hypertensiivisillä aikuisilla. Hypertension 2007, 50, 708–714.
50. Seliger, SL; Salimi, S.; Pierre, V.; Giffuni, J.; Katzel, L.; Parsa, A. Mikrovaskulaarinen endoteelin toimintahäiriö liittyy albuminuriaan ja CKD:hen vanhemmilla aikuisilla. BMC Nephrol. 2016, 17, 82.
51. Rajapakse, NW; Karim, F.; Straznicky, NE; Fernandez, S.; Evans, R.; Head, G.; Kaye, DM Lisätty endoteelispesifinen L-arginiinikuljetus estää liikalihavuuden aiheuttamaa verenpainetautia. Acta Physiol. 2014, 212, 39–48.
52. Gruber, H.-J.; Mayer, C.; Mangge, H.; Fauler, G.; Grandits, N.; Wilders-Truschnig, M. Liikalihavuus vähentää typpioksidin biologista hyötyosuutta nuorilla. Int. J. Obes. 2008, 32, 826–831.
53. Rajapakse, N.; Head, G.; Kaye, DM Sano EI liikalihavuuteen liittyvälle verenpaineelle: L-arginiini-typpioksidireitin rooli. Hypertensio 2016, 67, 813–819.
Vasilios Kotsis1, Fernando Martinez2, Christina Trakatelli1ja Josep Redon2,3,4,
1. 3. sisätautien osasto, hypertensio-24h ABPM ESH:n huippuyksikkö, Papageorgiou-sairaala, Thessalonikin Aristoteles-yliopisto, 564 29 Pavlos Melas, Kreikka; vkotsis@auth.gr (VK); ctrak@auth.gr (CT)
2. Internal Medicine Hospital Clínico de Valencia, 46010 Valencia, Espanja; fernandoctor@hotmail.com
3. Cardiovascular and Renal Research Group, INCLIVA Research Institute, Valencian yliopisto, 46010 Valencia, Espanja
4. CIBERObn Carlos III Institute, 28029 Madrid, Espanja
