Osa 1: Nykyaikaiset neurosuojausstrategiat sydänkirurgian aikana: Huippuluokan katsaus
Mar 26, 2022
ali.ma@wecistanche.com
Palesa Motshabi-Chakane 1, Palesa Mogane 1 , Jacob Moutlana 1, Gontse Leballo-Mothibi 1, Sithandiwe Dingezweni 1 , Dineo Mpanya 2 ja Nqoba Tsabedze2,*
Anestesiologian laitos, Terveystieteiden tiedekunta, Kliinisen lääketieteen korkeakoulu,
Witwatersrandin yliopisto, Johannesburg 2193, Etelä-Afrikka; Palesa.Motshabi@wits.ac.za (P.M.-C.); moganep@gmail.com (P.M.); drhlamatsi@gmail.com (J.M.); gleballomothibi@gmail.com (G.L.-M.); sdingezweni@ymail.com (SD)
Sisätautien laitos, kardiologian osasto, terveystieteiden tiedekunta,
Kliinisen lääketieteen korkeakoulu, Witwatersrandin yliopisto, Johannesburg 2193, Etelä-Afrikka;
Dineo.Mpanya@wits.ac.za
Kirjeenvaihto: Nqoba.Tsabedze@wits.ac.za
Lainaus: Motshabi-Chakane, P.; Mogane, P.; Moutlana, J.;
Leballo-Mothibi, G.; Dingezweni, S.; Mpanya, D.; Tsabedze, N. NykyaikainenNeurosuojausStrategiat sydänleikkauksen aikana: Huippuluokan katsaus. Int. J. Environ. Kansanterveys 2021, 18, 12747. https://doi.org/10.3390/ ijerph182312747
Akateeminen toimittaja: Paul B. Tchounwou

Cistanche tubulosa -jauheella on erittäin hyvä neuroprotektiivinen vaikutus
Abstrakti: Avosydänleikkaus on johtava syy hermosolujen vammoihin perioperatiivisessa tilassa, ja jotkut potilaat vaikeuttavat aivoverenkiertohäiriöitä ja deliriumia. Neurologiset seuraukset aiheuttavat valtavan taakan sairastuneen henkilön, hänen perheensä ja terveydenhuoltojärjestelmänsä psykologiselle hyvinvoinnille. Useat satunnaistetut kontrollitutkimukset (RCT) ovat yrittäneet tunnistaa terapeuttisia ja interventiostrategioita, jotka vähentävät sairastuvuutta ja kuolleisuutta potilailla, joilla on perioperatiivisia neurologisia komplikaatioita. Ei kuitenkaan ole vielä yksimielisyyttä parhaasta strategiasta, joka tuottaa parempia potilastuloksia, niin että standardoituneuroprotektioprotokollia ei ole olemassa merkittävässä määrässä anestesiaosastoja. Tämän katsauksen tarkoituksena on keskustella nykyaikaisesta näytöstä hermosolujen vammojen riskitekijöiden, loukkaantumismekanismien janeuroprotektiotoimenpiteet, jotka johtavat parempiin potilastuloksiin. Lisäksi tarkastellaan yhteenvetoa olemassa olevista RCT:istä ja suurista havainnointitutkimuksista sen määrittämiseksi, mitä strategioita tiede tukee ja mistä puuttuu lopullisia todisteita. Olemme todenneet, että farmakologista kokonaisnäyttöäneuroprotektioon heikko. Useimmat neuroprotektiiviset strategiat perustuvat eläinkokeisiin, joita ei voida täysin ekstrapoloida ihmispopulaatioon, eikä optimaalisesta optimaalisuudesta ole vielä yksimielisyyttäneuroprotektiivinenstrategiat potilaille, joille tehdään sydänleikkaus. Suuria monikeskustutkimuksia, joissa käytetään yleisiä standardoituja neurologisia laskeumamääritelmiä, tarvitaan edelleen olemassa olevien hyödyllisten vaikutusten arvioimiseksineuroprotektiivinenTekniikoita.
Avainsanat: neuroprotektio; aivoverenkiertohäiriö; delirium; sydänkirurgia; sydämen anestesia
1. Esittely
Neurosuojauskattaa strategiat, jotka säilyttävät hermosolujen rakenteen ja toiminnan. Neurologiset laskeumat on estettävä kaikilta potilailta, joille tehdään jonkinlainen leikkaus, erityisesti niillä, jotka on tarkoitettu sydänleikkaukseen. Esimerkiksi tutkimuksessa, johon osallistui 10 250 sydänleikkauksen kohteena ollutta potilasta, 221 (2 %) sai leikkauksen jälkeisen aivohalvauksen, ja sairaalahoidon kesto oli huomattavasti pidempi näillä potilailla verrattuna niihin, joilla ei ollut leikkauksen jälkeistä aivohalvausta (10 vs. 16 päivää, p.< 0.001)="" [1].="" numerous="" randomized="" controlled="" trials="" (rcts)="" have="" investigated="" the="" efficacy="" of="" pharmacological="" and="" non-pharmacological="" interventions="" that="" reduce="" neurological="" injury="" during="" and="" after="" cardiac="" surgery="" [2–4].="" however,="" there="" is="" still="" controversy="" on="" the="" optimal="">neuroprotektiostrategia, joka johtaa parempiin potilastuloksiin.
Tämän katsauksen tarkoituksena on keskustella nykyaikaisesta näytöstä hermosolujen vammojen riskitekijöiden, loukkaantumismekanismien janeuroprotektiotoimenpiteet, jotka johtavat parempiin potilastuloksiin.
2. Materiaalit ja menetelmät
Rct-tietojen tiedot, joissa käytetään erilaisianeuroprotektiivinenagentit saatiin sen jälkeen, kun he olivat suorittaneet järjestelmällisen kirjallisuushaun PUBMED:ssä, Scopusissa ja Google scholarissa. Käytettiin seuraavaa hakumerkkijonoa: (neuroprotektiostrategiat TAIneuroprotektioTAI farmakologinen hoito TAI ei-farmakologinen hoito) JA (sydänkirurgia TAI kardiopulmonaalinen ohitusleikkaus) JA (leikkauksen jälkeinen kognitiivinen toimintahäiriö TAI aivohalvaus TAI delirium TAI kohtaus) JA aikuiset potilaat. Mukanamme oli satunnaistettuja kontrollikokeita, systemaattisia katsauksia ja meta-analyysejä, jotka on julkaistu viimeisten 15 vuoden aikana. Kirjallisuushaun painopiste oli farmakologisessa ja ei-farmakologisessaneuroprotektiivinenstrategiat (taulukko 1). Jos käytettävissä oli järjestelmällisiä tarkasteluja tai meta-analyyseja tukitoimien rct-ohjelmista, niistä raportoitiin mieluummin kuin yksittäisistä rct-sopimuksista.
Taulukko 1. Yhteenveto satunnaistetuista kontrollikokeista, joissa verrattiin interventioita tavanomaiseen hoitoonneuroprotektiosydänkirurgiassa.
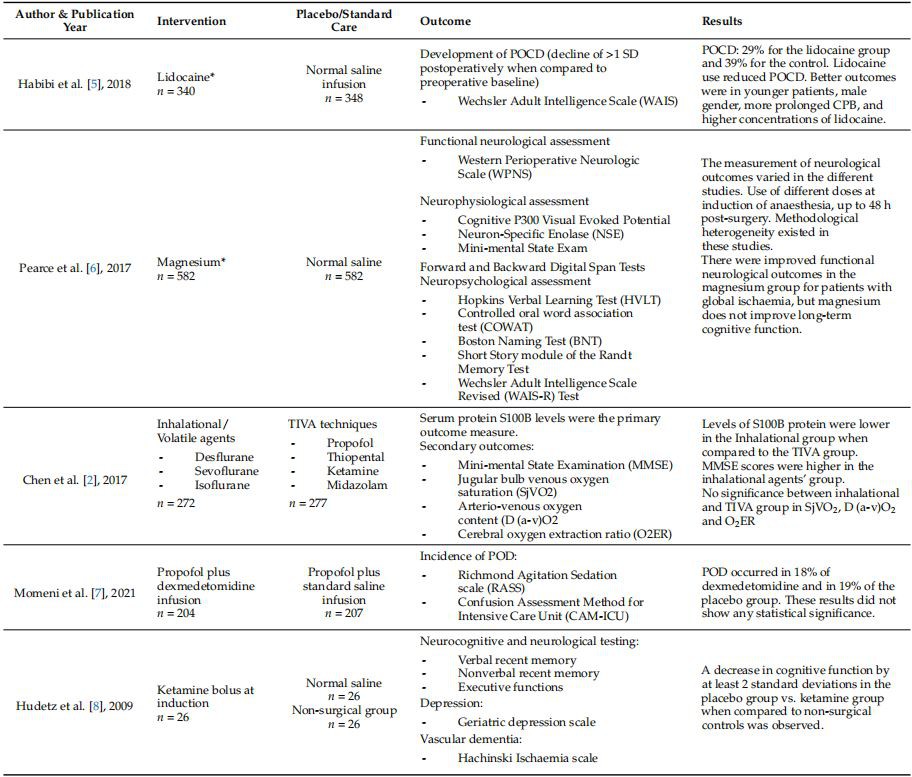

Lyhenteet: RCT, satunnaistettu kontrollikoe; CPB, kardiopulmonaalinen ohitus; POCD, leikkauksen jälkeinen kognitiivinen toimintahäiriö; MM-RR, Manteli–Haenszel-riskisuhde; CI, luottamusvälit; TAI, kerroinsuhde; TIVA, laskimonsisäinen anestesia yhteensä; Joukkotuhoase, painotettu keskiarvoero; POD, postoperatiivinen delirium; CABG, sepelvaltimon ohitusleikkaus; MAP, keskimääräinen valtimopaine; SD, keskihajonta. Lidokaiini* bolus 1–1,5 mg/kg. Infuusio 2–4 mg/kg/tunti: riippuu keskuksen protokollasta. Lidokaiinin pitoisuus plasmassa vaihteli välillä 7-30 μmol/l. Magnesium* -annokset, jotka olivat vähintään 2 g 24 tunnin sisällä sydänpysähdyksestä tai sydänleikkauksesta. Rivastigmiini*, 1,5 mg annos 8 tuntia, illasta ennen leikkausta; yhteensä 22 annosta (päivään 6 asti postoperatiivisesti). Syvä hypoterminen verenkiertohäiriö (DHCA) taaksepäin suuntautuvalla aivoperfuusiolla (RCP)*, jäähdytetään nenänielun lämpötiloihin 14,1 o C - 20 o C. Etäiskeerinen sepelvaltimon esivakautus (RIPC)* käyttämällä BP-mansettia yläraajassa kolmella vuorottelevalla inflaatiojaksolla (200 mmHg 5 min) ja deflaatio 5 minuutin ajan (reperfuusio). Aivojen hapetuksen seuranta*: Aivojen deoksigenaatiojaksot< 60%="" for="">60 sivua.
3. Neurologisen alijäämän esiintyvyys ja esiintyvyys sydänleikkauksen jälkeen
Kansainvälinen nimikkeistökoodi suosittelee termiä "perioperatiiviset neurokognitiiviset häiriöt" kuvaamaan sekä leikkauksen jälkeistä deliriumia (POD) että leikkauksen jälkeistä kognitiivista toimintahäiriötä/heikkenemistä (POCD), joista jälkimmäisellä ei ole diagnostista ja tilastollista mielenterveyshäiriöiden käsikirjaa 5 (DSM5) diagnoosia varten [14,15]. Toinen käytetty laaja terminologia on "neurologinen vamma sydänleikkauksen jälkeen". Perioperatiivinen aivohalvaus, delirium ja enkefalopatia ovat joitain sydänkirurgian neurologisia seurauksia [16]. Aivohalvauksen riski vaihtelee suoritetun leikkauksen tyypin mukaan [17]. Esimerkiksi kaksois- tai kolminkertaisen venttiilin leikkaukseen liittyy 10%: n aivohalvauksen riski, kun taas riski on pienempi potilailla, jotka on tarkoitettu "sydämen lyömiseen", joka tunnetaan myös nimellä "off-pump", sepelvaltimon ohitussiirteen (CABG) leikkaus [17].
Meta-analyysissä, johon osallistui 174 969 sydänleikkaukseen lähetettyä potilasta, varhaisten ja viivästyneiden aivohalvausten yhdistetty tapahtumamäärä oli kukin alle 1% [18]. Lisäksi delirium on yleistä vanhuksilla, ja sen esiintyvyys on suurempi, 12% [19]. On vain vähän tutkimuksia, joissa raportoidaan neurologisista komplikaatioista sydänleikkauksen jälkeen potilailla, jotka asuvat matalan ja keskitulotason maissa (LMIC). Retrospektiivisessä kaavioanalyysissä, johon osallistui 1218 peräkkäistä potilasta, jotka oli lähetetty CABG-leikkaukseen Johannesburgissa, perioperatiivisen aivohalvauksen määrä oli 1,2% [20]. Lisäksi vuosi aivohalvauksen alkamisen jälkeen ison-Britannian punnan vuosikustannuksiksi henkeä kohti arvioidaan 18 081 puntaa, mikä nousee 22 961 puntaan yli 84-vuotiailla potilailla [21]. Nämä korkeat terveydenhuollon kustannukset edellyttävät kiireellistä tarvetta strategioille, jotka vähentävät aivohalvauksen sydänleikkauksen jälkeistä taakkaa.

4. Neurologiseen laskuun liittyvät riskitekijät
Leikkaustyypin lisäksi aivohalvausriski kasvaa potilailla, joilla on olemassa oleva aivoverenkiertosairaus, perifeerinen verisuonisairaus, diabetes, verenpainetauti, aiempi sydänleikkaus, preoperatiivinen infektio, kiireellinen leikkaus, yli 2 tunnin sydän-keuhkojen ohitusaika (CPB), leikkauksensisäisen verenvuodon tarve ja korkeat verensiirtovaatimukset [18]. Kognitiivisen heikkenemisen riskitekijät sydänkirurgian jälkeen ovat monitekijäisiä (kuva 1). Neurologiset tulokset ovat moninaisia, ja ne on aiemmin luokiteltu tyypiksi I (sisältää kuolemaan johtaneen tai ei-kuolemaan johtavan aivohalvauksen, stuporin tai kooman purkauksen yhteydessä) ja tyypin II, joka sisältää kognitiivisen toiminnan heikkenemisen, muistivajeen tai kohtaukset [22].

Kuvio 1. Hermosolujen vamman riskitekijät ennen sydänleikkausta, sen aikana ja sen jälkeen.
Kognitiivisen toiminnon arviointi on tehtävä ennen leikkausta ja leikkauksen jälkeen käyttäen validoitua kognitiivisen testin arviointityökalua. Lisäksi testauksen ajoitus vaikuttaa neurologisten vammojen diagnosointinopeuteen sydänleikkauksen jälkeen [23]. 30 päivän kuluessa leikkauksen jälkeen tehdyissä diagnostisissa testeissä on sekavia tekijöitä, kuten leikkauksen jälkeistä kipua, ja lääkkeiden käyttö voi vaikuttaa arviointipisteisiin [15]. Emergence delirium tapahtuu ennen anestesiasta heräämistä, sen aikana tai sen jälkeen, kun taas postoperatiivinen delirium tapahtuu 24–72 tuntia sen jälkeen, ja leikkauksen jälkeinen kognitiivinen heikkeneminen tapahtuu viikoista kuukausiin leikkauksen jälkeen [15,24]. Suurin osa POCD: n riskitekijöistä liittyy niiden mahdollisuuteen häiritä elinsuojelun perusperiaatteita, kuten hapen toimitusta, elinten perfuusiota, elinten ravitsemusvaatimuksia, olemassa olevia elinvarastoja ja myrkyllistä altistumista leikkauksen aikana [25]. POCD: n ehkäisy sydänleikkauksen jälkeen on suunnattu näiden riskitekijöiden ymmärtämiseen ja hallintaan.

5. Aivovamman mekanismi
Sydänkirurgiaan liittyvän aivovamman mekanismi on monimutkainen ja monitekijäinen. Yleisin mekanismi johtuu sepelemisistä syistä, jotka johtavat aivojen hypoperfuusioon ja emboliaan [26,27]. Sepeleemisten syiden lisäksi on liittynyt myös tulehdusvaste, aivojen hypertermia, hyperglykemia, perioperatiivinen anemia ja eteisvärinä (kuva 2) [27].

Kuvio 2. Aivovamman mekanismit.
5.1. Muuttunut aivoperfuusio
Sydänleikkauksen ja CPB: n vaikutukset aivoperfuusioon voidaan luokitella aivojen hypoperfuusioon ja reperfuusioon. Aivojen hypoperfuusio, joka johtuu aivoverenvirtauksen (CBF) vähenemisestä CPB: n aikana, on ensisijainen syy sepelemiseen aivovammaan. Tätä vamman muotoa voi pahentaa entisestään mikroembolien heikentynyt puhdistuma CBF:n pienentyessä. Pitkälle edennyt ikä, laaja aivoverenkiertohäiriö ja aivohalvauksen historia lisäävät aivojen hypoperfuusion riskiä [26]. CPB: n varhainen jakso liittyy yleensä alhaisen keskimääräisen valtimopaineen (MAP) jaksoihin kanyylien asettamisen ja sydämen suurten astioiden käsittelyn aikana. Tämän seurauksena voi esiintyä aivojen hypoperfuusiota, ja verenkierto aivojen vesistöalueilla voi vähentyä kriittisesti. CPB: n loppupuolella tapahtuu aivojen reperfuusio, mikä johtaa vapaiden happiradikaalien muodostumiseen [28]. Iskemia-/reperfuusiovamman aikana aloitetaan erilaisia sekundaarisia mekanismeja, jotka lopulta johtavat hermosolujen kuolemaan.
5.2. Hypoksiaan liittyvä aivovamma
Aivojen hypoperfuusiojaksojen aikana esiintyvät hypoksiset olosuhteet johtavat eri molekyylien, kuten hypoksiaa indusoivan tekijän (HIF) ja sulfonyyliureareseptorin 2A (SUR2A) proteiinin, säätelyyn, jotka sitten käynnistävät tapahtumia, jotka voivat johtaa hermosolujen vammoihin [28]. Happitasojen lasku johtaa HIF:n siirtymiseen hermosolujen ytimeen. HIF koostuu α ja β alayksiköstä. α-alayksikkö ilmaistaan konstitutiivisesti. Se kuitenkin hajoaa nopeasti normaaleissa happipitoisuuksissa. Lisäksi hypoksia liittyy adenosiinitrifosfaatti (ATP) -tasojen laskuun, mikä johtaa ATP-riippuvaisten ionipumppujen vikaantumiseen, solunsisäisen natrium- ja kalsiumpitoisuuden nousuun ja lopulta sytoplasmiseen ja mitokondrioiden turvotukseen, mikä voi johtaa solukuolemaan [28].
5.3 Reperfuusioon liittyvä aivovamma
Reperfuusiovaihe liittyy reaktiivisten happilajien (ROS) tuotantoon, pääasiassa mitokondrioissa. ROS reagoi typpioksidin (NO) kanssa muodostaen peroksinitriittiä. Tämä molekyyli on erittäin reaktiivinen ja nitrosylaattiproteiinit, mikä johtaa hermosolujen toimintahäiriöön ja aivovaurioihin [28].
5.4. Aivojen makro- ja mikroembolia
Sydänkirurgia johtaa usein erilaisten embolisten materiaalien tuotantoon. Koon mukaan kytkettynä embolit voidaan erottaa makroemboleiksi, jotka tukkivat virtauksen valtimoissa, joiden halkaisija on vähintään 200 μm, ja mikroemboleiksi, jotka tukkivat pienempiä valtimoita, arterioleja ja kapillaareja. Ateroskleroottiset plakit, jotka johtuvat pääasiassa aortasta, muodostavat makroembolit [26], kun taas mikroembrolit koostuvat kaasumaisista emboleista ja biologisista aggregaateista, kuten trombista, verihiutaleiden aggregaateista ja rasvasta [26,28,29]. Epäorgaanisista roskista, kuten polyvinyylikloridiletkun ja silikonin vaahdonestoaineen fragmenteista, peräisin olevia emboleja on raportoitu aiemmin [29].
Vaikka CPB-koneessa on suojamekanismeja, kuten kupla-ansoja [28], kaasumaisia emboleja voidaan silti viedä CPB-piiriin laskimokanyloituksen, lääkkeiden antamisen ja vasemman sydämen avoimista sydänkammioista [26]. Lisäksi aortan manipulointi leikkauksen aikana lisää embolisaatioriskiä valtimosuodattimien sijoittelusta huolimatta [28,30]. Aivojen mikroemboliaa kognitiivisen toimintahäiriön mekanismina tukee aivojen makro-/mikroembolikuormituksen välinen suhde CPB:n aikana ja kognitiivinen toimintahäiriö eri tutkimuksissa [26,31–34]. Lisäksi makro-/mikroembolia voi esiintyä myös aortan dekannaulaation aikana, varsinkin kun potilas ei ole saanut riittävästi antikoagulaatiohoitoa.

5.5 Tulehdusvaste
CPB:hen liittyvät tulehdusprosessit pahentavat entisestään hermosolujen sisäistä tuomaristoa [27]. Potilaan veren vuorovaikutus CPB-komponenttien, kuten letkun, säiliöiden, hapettimen ja liitosten, kanssa johtaa komplementtijärjestelmän aktivoitumiseen, mikä johtaa tulehdusta edistävien sytokiinien, kuten interleukiini (IL)-6, IL-8, IL-10 ja kasvaimen nekroositekijä-alfa (TNFα) [28,35], vapautumiseen. Tämä systeeminen tulehdusvaste johtaa veri-aivoesteen vuotamiseen, aivoedeemaan ja lopulta aivojen häiriöihin [28].
5.6. Aivojen hypertermia
Hypertermian on myös raportoitu aiheuttavan aivovaurioita erilaisissa kliinisissä olosuhteissa, ja sen on osoitettu pahentavan hermosolujen kuolemaa iskemian jälkeen. Hypertermian haitalliset vaikutukset aivoissa liittyvät hypertermian aiheuttamaan solujen turvotukseen ja nekroottiseen kuolemaan erittäin korkeiden lämpötilojen tapauksessa [36]. CPB:n sydänleikkauksen aikana aivojen hypertermiaa voi esiintyä johtuen aortan kanyylin läheisyydestä aivosuoniin tai aivojen lämpötilan aliarvioinnista tavanomaisella seurannalla [27].
5.7. Hyperglykemia
CPB: n ja hypotermian aiheuttama stressivaste sydänleikkauksen aikana johtaa kohonneisiin seerumin glukoositasoihin jopa ei-diabeetikoilla [27]. Hyperglykemian aiheuttaman aivovamman patofysiologia on monitekijäinen. Hyperglykemia lisää reaktiivisten happilajien tuotantoa proteiinikinaasi C-välitteisen reitin ja nikotiiniamidi-adeniini-dinukleotidifosfaatin (NADPH) lisääntyneen tuotannon kautta [37]. Reaktiiviset happilajit voivat johtaa hermosolujen kuolemaan, kuten aiemmin on kuvattu. Hyperglykemian ja ydintekijä-kappa B:n lisääntyneen ilmentymisen välillä on myös hyvin kuvattu yhteys [38]. Hyperglykemian metaboliset vaikutukset, kuten lisääntynyt maitohapon tuotanto ja sitä seurannut asidoosi ja mitokondrioiden toimintahäiriöt, ovat toinen ehdotettu hyperglykemiaan liittyvän aivovamman mekanismi [39].
