DBL-katekolin, mahdollisen melanosyyttien sytotoksisen yhdisteen, oksidatiivinen oligomerointi paljastaa uusien ionisten diels-alder-tyyppisten lisäysten esiintymisen, osa 2
May 18, 2023
Dimeeristä muodostui myös yhdisteitä, joissa hävisi kaksi protonia. Nämä yhdisteet eluoituivat 17 minuutin, 18 minuutin, 20 minuutin ja 21 minuutin kohdalla molekyylimassalla 353,1021, joka on 1,5 ppm:n sisällä C20H16O6:n teoreettisesta massasta (353,1013 amu). Näiden yhdisteiden CID-spektri oli merkittävästi erilainen, mikä viittaa siihen, että reaktioseoksessa muodostuu useita isomeerejä (kuvat 8-11).
Asiaankuuluvien tutkimusten mukaan kista on yleinen yrtti, joka tunnetaan nimellä "ihmeyrtti, joka pidentää elämää". Sen pääkomponentti on cistanosidi, jolla on erilaisia vaikutuksia, kuten antioksidantteja, tulehdusta ehkäiseviä ja immuunitoimintoja edistäviä vaikutuksia. Cistanchen ja ihon valkaisun välinen mekanismi piilee cistanche-glykosidien antioksidanttisessa vaikutuksessa. Ihmisen ihon melaniinia syntyy tyrosiinin katalysoiman tyrosiinin hapettumisen seurauksena, ja hapetusreaktio vaatii hapen osallistumista, joten kehon happivapaista radikaaleista tulee tärkeä melaniinin tuotantoon vaikuttava tekijä. Cistanche sisältää cistanosidia, joka on antioksidantti ja voi vähentää vapaiden radikaalien muodostumista kehossa, mikä estää melaniinin tuotantoa.

Napsauta Cistanche Tubulosaa valkaisua varten
Lisätietoja:
david.deng@wecistanche.com/WhatApp:86 13632399501
20 minuutin kohdalla eluoituva piikki osoitti vain vesihäviön päätuotantona (m/z 335 ioni kuvassa 10). 21 minuutin kohdalla eluoituva piikki osoitti pääpiikin COCH2-ryhmän häviämisen kanssa (m/z 311 ionia). Tämän yhdisteen on oltava DBL-kinonidimeerin hapetettu muoto. Toisaalta 18 minuutin kohdalla eluoituva piikki osoitti suuria hajoamisioneja 335:ssä (vesihäviö), 311:ssä (COCH2-häviö) ja vähäisen ionin m/z:ssä 293 (vesi- ja COCH2-häviö). Huomaa, että viimeinen hajoamisioni ei ole mahdollinen DBL-kinonidimeerille ja on mahdollista vain bentsodioksaanidimeerin hapettuneelle muodolle. Näistä tuloksista pääteltiin, että reaktiossa muodostuu kahta erilaista dimeeriä - bentsodioksaanidimeeriä ja DBL-kinonidimeeriä.


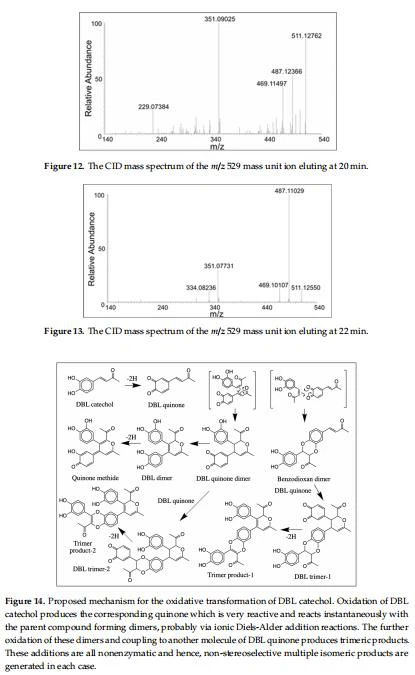
Dimeeristen tuotteiden lisäksi reaktioseoksen massaspektrissä voitiin havaita myös trimeerisiä yhdisteitä. Jälleen on läsnä kahden emo-ionin m/z 529,1486, joista toinen eluoituu 20 minuutin kohdalla ja toinen 22 minuutin kohdalla (kuvio 5 paneeli C). Niiden massa on 3 ppm:n sisällä teoreettisen protonoidun trimeeriyhdisteen (C30H26O9) massasta. Niiden CID-spektrit on esitetty kuvissa 12 ja 13. Yhden isomeerin CID antoi pää-ionin 351:ssä, mikä vastaa dimeerin täysin hapettunutta muotoa. Toinen isomeeri antoi huomattavasti vähemmän tätä tuotantoa. Trimeerien rakennetta ei voitu erottaa pirstoutumiskuvion perusteella. Siitä huolimatta oli selvää, että reaktioseoksessa muodostuu myös erilaisia trimeerisiä tuotteita. Näin ollen tässä artikkelissa esitetyt tulokset vahvistavat, että DBL-katekoli on erittäin herkkä oksidatiiviselle polymeroitumiselle, kuten eräs ryhmämme aiemmassa työssä ehdotti [11].

Dimeerien ja trimeerien muodostuminen voidaan selittää reaktiossa muodostuneiden kinonoidituotteiden reaktiivisuuksilla (kuva 14). DBL-katekolin hapettuminen tuottaa vastaavan kinoninsa, joka on erittäin hydrofobinen ja voi helposti osoittaa sykloadditioreaktion emokatekolin kanssa. DBL-kinonin ioninen Diels-Alder-lisäys emokatekoliin tuottaa kahden tyyppisiä additiotuotteita, kuten kuvassa 14 on esitetty. Kinonoidikarbonyyliryhmien reaktio desaturoidun sivuketjun kanssa tuottaa bentsodioksaanidimeerin. Sitä vastoin dienonin sivuketjun lisäys desaturoidun sivuketjun kanssa tuottaa pyraanityyppisen adduktin, joka on yksinkertaisesti nimetty DBL-kinonidimeeriksi. Molemmat näistä yhdisteistä voivat käydä läpi helpon hapettumisen ja lisäreaktion muodostaen trimeerisiä yhdisteitä samanlaisilla Diels-Alder-reaktioilla. Vaikka Diels-Alder-reaktion biologinen esiintyminen on hyvin harvinaista, sen on raportoitu etenevän muutamissa olosuhteissa [20–23]. Esimerkiksi yksi ryhmistämme on äskettäin osoittanut, että N-asetyylidopa-metyyliesterin kinoni käy läpi nopeaa sykloadditiota, luultavasti ionisen Diels-Alder-reaktion kautta, jolloin syntyy samanlainen bentsodioksaanidimeeri [20]. Nykyiset tutkimukset tukevat myös tällaisten ionisten Diels-Alder-lisäysten esiintyvyyttä sivuketjujen desaturoituneiden katekolien kinonoidikemiassa. Nämä syklisointireaktiot ovat kaikki ei-entsymaattisia ja siten ei-stereoselektiivisiä, mikä johtaa useiden isomeeristen tuotteiden tuotantoon. Tällaisten useiden tuotteiden tuotanto entsymaattisesti tuotettujen kinonoidilajien ei-entsymaattisen syklisoinnin aikana on dokumentoitu hyvin tässä laboratoriossa useille dehydrodopa- ja dehydrodopamiinijohdannaisille [16–20].
RK:n ja sen pelkistyneen tuotteen, rododendronin, voimakas melanotoksisuus on nyt vakiintunut [1–8,24]. Vaikka jotkin reaktioista, kuten tiolien väheneminen ja solun nukleofiileihin lisääminen, ovat yhteisiä myös muille sytotoksisille kinoneille, RK:n ja rododendronin ainutlaatuinen genotoksisuus voidaan selittää niiden kyvyllä osoittaa useita redox-reaktioita, jotka eivät tuota vain vastaavia kinonoidijohdannaisia. mutta myös useita sivuketjun desaturoituneita kinonoidilajeja. Lisäksi tuotetaan lukuisia dimeerisiä ja trimeerisiä yhdisteitä, joilla kaikilla on kyky aiheuttaa reaktiivisten happilajien tuotantoa, solutiolien ehtymistä ja reaktiota solun makromolekyylien kanssa, mukaan lukien proteiinit ja DNA [11,24]. Yhdisteet, joissa esiintyy tällaisia useita redox-reaktioita, ovat siksi myrkyllisempiä kuin yksinkertaiset kinonoidiyhdisteet. On melko vaikeaa paikantaa yhtä tai muuta RK:n tai rhododendronin tuotetta leukoderman ja muiden myelotoksisten vaikutusten aiheuttajaksi. Nämä tulokset huomioon ottaen varomme käyttämästä näitä yhdisteitä ja muita samankaltaisia katekoleja, jotka voivat aiheuttaa useita redox-reaktioita minkä tahansa melaniiniin liittyvien häiriöiden hoidossa.
3. Materiaalit ja menetelmät


Lyhenteet
Viitteet
1. Beekwilder, J.; van der Meer, I.; Sibbesen, O.; Broekgaarden, M.; Qvist, I.; Mikkelsen, JD; Hall, RD Luonnollisen vadelmaketonin mikrobituotanto. Biotechnol. J. 2007, 2, 1270–1279. [CrossRef] [PubMed]
2. Fukuda, Y.; Nagano, M.; Futatsuka, M. Ammatillinen leukoderma työntekijöillä, jotka osallistuvat 4-(p-hydroksifenyyli)-2-butanonin valmistukseen. J. Occup. Health 1998, 40, 118–122. [CrossRef]
3. Nishigori, C.; Aoyama, Y.; Ito, A.; Suzuki, K.; Suzuki, T.; Tanemura, A.; Ito, M.; Katayama, I.; Oiso, N.; Kagohashi, Y.; et ai. Opas lääketieteen ammattilaisille (eli ihotautilääkäreille) rododenolin aiheuttaman leukoderman hoitoon. J. Dermatol. 2015, 42, 113–128. [CrossRef] [PubMed]
4. Sasaki, M.; Konda, M.; Sato, K.; Umeda, M.; Kawabata, K.; Takahashi, Y.; Suzuki, T.; Matsunaga, K.; Inoue, S. Rhododendron, depigmentaatiota indusoiva fenoliyhdiste, aiheuttaa melanosyyttien sytotoksisuutta tyrosinaasista riippuvaisen mekanismin kautta. Pigment Cell Melanoma Res. 2014, 27, 754–763. [CrossRef] [PubMed]
5. Kasamatsu, S.; Hachiya, A.; Nakamura, S.; Nakamura, S.; Yasuda, Y.; Fujimori, T.; Takano, K.; Moriwaki, S.; Hase, T.; Suzuki, T.; et ai. Aktiivisen kirkastusaineen, rododendronin, levittämisen aiheuttama pigmenttimuutos liittyy tyrosinaasiaktiivisuuteen tietyllä kynnysarvolla. J. Dermatol. Sci. 2014, 76, 16–24. [CrossRef] [PubMed]
6. Ito, S.; Yamashita, T.; Ojika, M.; Wakamatsu, K. Rhododendronin tyrosinaasin katalysoima hapetus tuottaa 2-metyylikromaania-6,7-dionia, oletettua lopullista myrkyllistä metaboliittia: Vaikutukset melanosyyttitoksisuuteen. Pigment Cell Melanoma Res. 2014, 27, 744–753. [CrossRef] [PubMed]
7. Ito, S.; Gerwat, W.; Kolbe, L.; Yamashita, T.; Ojika, M.; Wakamatsu, K. Ihmisen tyrosinaasi voi hapettaa molemmat rododendronin enantiomeerit. Pigment Cell Melanoma Res. 2014, 27, 1149–1153. [CrossRef]
8. Ito, S.; Okura, M.; Wakamatsu, K.; Yamashita, T. Rododendroli-eumelaniinin voimakas prooksidanttiaktiivisuus indusoi kysteiinin ehtymistä B16-melanoomasoluissa. Pigment Cell Melanoma Res. 2017, 30, 63–67. [CrossRef]
9. Ito, S.; Okura, M.; Nakanishi, Y.; Ojika, M.; Wakamatsu, K.; Yamashita, T. Rhododendronin (RD) tyrosinaasitalysoitu aineenvaihdunta B16-melanoomasoluissa: RD-feomelaniinin tuotanto ja kovalenttinen sitoutuminen tioliproteiinien kanssa. Pigment Cell Melanoma Res. 2015, 28, 295–306. [CrossRef]
10. Ito, S.; Wakamatsu, K. Rhododendronin aiheuttaman leukoderman biokemiallinen mekanismi. Int. J. Mol. Sci. 2018, 19, 552. [CrossRef]
11. Ito, S.; Hinoshita, M.; Suzuki, E.; Ojika, M.; Wakamatsu, K. Leukodermaa aiheuttavan vadelmaketonin tyrosinaasin katalysoima hapetus tuottaa (E)-4-(3-okso-1-butenyyli)-1,2- bentsokinoni: Vaikutus melanosyyttitoksisuuteen. Chem. Res. Toxicol. 2017, 30, 859–868. [CrossRef]
12. Sugumaran, M.; Dali, H.; Kundzicz, H.; Semensi, V. Karboksietyyli-o-bentsokinonijohdannaisten epätavallinen molekyylinsisäinen syklisaatio ja sivuketjun desaturaatio. Bioorg. Chem. 1989, 17, 443-453. [CrossRef]
13. Sugumaran, M.; Ricketts, D. Mallin sklerotisaatiotutkimukset. 3. Peptyylimallin tyrosiinin ja dopajohdannaisten ihon entsyymien katalysoima hapetus. Kaari. Insect Biochem. Physiol. 1995, 28, 17–32. [CrossRef]
14. Sugumaran, M. Kinonimetidejen reaktiivisuus o-kinoneja vastaan katekoliamiinin metaboliassa ja eumelaniinin biosynteesissä. Int. J. Mol. Sci. 2016, 17, 1576. [CrossRef]
15. Ito, S.; Sugumaran, M.; Wakamatsu, K. Elävissä organismeissa tuotettujen ortokinonien kemialliset reaktiivisuudet: tyrosinaasin ja fenoloksidaasin vaikutuksesta fenoleihin ja katekoleihin muodostuvien kinonoidituotteiden kohtalo. Int. J. Mol. Sci. 2020, 21, 6080. [CrossRef]
16. Abele, A.; Zheng, D.; Evans, J.; Sugumaran, M. Hyönteisten kutikulaarisen sklerotisoivan esiasteen, 1,2-dehydro-N-asetyylidopamiinin oksidatiivisen muutoksen mekanismien uudelleentarkastelu. Insect Biochem. Mol. Biol. 2010, 40, 650–659.
17. Abebe, A.; Kuang, QF; Evans, J.; Robinson, WE; Sugumaran, M. Trikromin malliyhdisteen oksidatiivinen transformaatio tarjoaa uuden käsityksen tunikromien silloittumis- ja puolustusreaktiosta. Bioorg. Chem. 2017, 71, 219–229. [CrossRef]
18. Kuang, QF; Abebe, A.; Evans, J.; Sugumaran, M. Tunikromien oksidatiivinen transformaatio – mallitutkimukset 1,2-dehydro-N-asetyylidopamiinilla ja N-asetyylikysteiinillä. Bioorg. Chem. 2017, 73, 53–62. [CrossRef]
19. Abebe, A.; Kuang, QF; Evans, J.; Sugumaran, M. Massaspektrometriset tutkimukset valaisevat 1,2-dehydro-N-asetyylidopan epätavallisia oksidatiivisia muutoksia. Rapid Comm. Massaspektri. 2013, 27, 1785–1793. [CrossRef]
20. Abebe, A.; Zheng, D.; Evans, J.; Sugumaran, M. Peptidyylidehydrodopa-malliyhdisteen, 1,2-dehydro-N-asetyylidopametyyliesterin, uusi translaation jälkeinen oligomerointi. Bioorg. Chem. 2016, 66, 33–40. [CrossRef]
21. Takao, KI; Munakata, R.; Tadano, KI Viimeaikaiset edistysaskeleet luonnontuotteiden synteesissä käyttämällä molekyylinsisäisiä Diels-Alder-reaktioita. Chem. Rev. 2005, 105, 4779–4807. [CrossRef] [PubMed]
22. Ose, T.; Watanabe, K.; Mie, T.; Honma, M.; Watanabe, H.; Yao, M.; Oikawa, H.; Tanaka, I. Näkemys luonnollisesta Diels-Alder-reaktiosta makrofagisyntaasin rakenteesta. Nature 2003, 422, 185–189. [CrossRef] [PubMed]
23. Sukat, EM; Williams, RM Biosynteettisten Diels-Alder-reaktioiden kemia ja biologia. Angew. Chem. Int. Ed. Eng. 2003, 42, 3078–3115. [CrossRef] [PubMed]
24. Ito, S.; Agata, M.; Okochi, K.; Wakamatsu, K. Rhododendrol-eumelaniinin voimakasta prooksidanttiaktiivisuutta tehostaa ultravioletti-A-säteily. Pigment Cell Melanoma Res. 2018, 31, 523–528. [CrossRef]
Lisätietoja: david.deng@wecistanche.com / WhatApp:86 13632399501
