Neutrofiiligelatinaasiin liittyvän lipokaliinin tunnistaminen uudeksi varhaisen virtsan biomarkkeriksi iskeemiselle munuaisvauriolle
Mar 22, 2022
Ottaa yhteyttä:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
JAYA MISHRA,* QING MA,* ANNE PRADA,* MARK MITSNEFES,* KAMYAR ZAHEDI,* JUN YANG,† JONATHAN BARASCH,† ja PRASAD DEVARAJAN*
*Nephrology & Hypertension, Cincinnati Children's Hospital Medical Center, Cincinnati, Ohio; ja † Nefrologia, College of Physicians and Surgeons, Columbia University, New York, New York
Abstrakti.
Akuuttimunuaisteniskeemisen vamman aiheuttama epäonnistuminen (ARF) on edelleen yleinen ja mahdollisesti tuhoisa ongelma. Transkriptominlaajuista kyselystrategiaa käytettiin tunnistamaan munuaisgeenit, jotka indusoituvat hyvin varhain munuaisiskemian jälkeen ja joiden proteiinituotteet voisivat toimia uusina biomarkkereina ARF:lle. Seitsemän geeniä, jotka ovat lisääntynyt ja - 10--kertaisia, tunnistettiin, joista yhden (Cyr61) on äskettäin raportoitu indusoituneen munuaisiskemian jälkeen. Yllättäen kuuden muun transkription induktio oli uutta ARF-kentässä. Tässä tutkimuksessa yksi näistä aiemmin tunnistamattomista geeneistä karakterisoitiin edelleen, nimittäin neutrofiiligelatinaasiin liittyvä lipokaliini (NGAL), koska se on pieni erittyvä polypeptidi, joka on proteaasiresistentti ja sen vuoksi voidaan helposti havaita virtsasta. Merkittävä NGAL-mRNA- ja proteiinitasojen noususäätely varhaisessa postskeemisessa hiiressämunuainenvahvistettiin. NGAL-proteiinin ilmentyminen havaittiin pääasiassa lisääntyvien solujen tuman antigeenipositiivisissa proksimaalisissa tubulussoluissa, pisteellisessä sytoplasmisessa jakaumassa, joka lokalisoitui yhdessä myöhäisten endosomien markkerien kanssa. NGAL havaittiin helposti virtsasta heti ensimmäisellä virtsan erityksellä iskemian jälkeen sekä ARF:n hiiri- että rottamalleissa. NGAL:n esiintyminen virtsassa liittyi annokseen ja kestoonmunuaisteniskemia ja edelsi muiden virtsan merkkiaineiden, kuten N-asetyyli- -D-glukosaminidaasin ja 2-mikroglobuliinin, ilmaantumista. NGAL:n alkuperä tubulussoluista varmistettiin viljellyissä ihmisen proksimaalisissa tubulussoluissa, jotka altistettiin in vitro iskeemiselle vauriolle, missä NGAL-mRNA indusoitui nopeasti soluissa ja NGAL-proteiini oli helposti havaittavissa viljelyväliaineessa 1 tunnin sisällä lievästä ATP:n ehtymisestä. NGAL oli myös helposti havaittavissa sisplatiinin aiheuttaman munuaistoksisuuden omaavien hiirten virtsasta, mikä taas edelsi N-asetyyli- -D-glukosaminidaasin ja 2-mikroglobuliinin ilmaantumista. Tulokset osoittavat, että NGAL voi edustaa varhaista, herkkää, ei-invasiivista virtsan biomarkkeria iskeemiselle ja nefrotoksisellemunuaistenvahinkoa.

Cistanche herbavoi hoitaa munuaisvaurioita
Saat lisätietoja Cistancheen liittyvistä tuotteista
Akuuttimunuaistenepäonnistuminen(ARF) iskeemisen tai nefrotoksisen vaurion seurauksena on edelleen yleinen ja mahdollisesti tuhoisa ongelma kliinisessä nefrologiassa, ja kuolleisuus on jatkuvasti korkea tukihoidon merkittävästä edistymisestä huolimatta (1–4). Uraauurtavat tutkimukset useiden vuosikymmenien ajan ovat valaisseet jatkuvan verisuonten supistumisen, tubulustukoksen, solujen rakenteellisten ja aineenvaihdunnan muutosten sekä tulehdusvasteen roolit ARF:n patogeneesissä (4–7). Vaikka nämä tutkimukset ovat tasoittaneet tietä onnistuneille terapeuttisille lähestymistavoille eläinmalleissa, ihmisillä tehdyt translaatiotutkimukset ovat tuottaneet pettymyksen tuloksia (2–4). Syitä tähän voivat olla munuaisten monitahoinen vaste iskemialle ja nefrotoksiineille sekä ARF:n varhaisten merkkiaineiden niukkuus, mikä johtaa hoidon aloittamisen viivästymiseen (4–8).
Yrittää selvittää näiden lukemattomien molekyyliperustan aikaisessa vaiheessamunuaistenVastauksia ovat helpottaneet viimeaikaiset toiminnallisen genomiikan edistykset, jotka ovat tuottaneet uusia työkaluja monimutkaisten biologisten prosessien, kuten iskeemisen ARF:n, genominlaajuiseen analysointiin (8–11). cDNA-mikrosirumenetelmät tarjoavat rinnakkaisia ja kvantitatiivisia ilmentymisprofiileja tuhansista geeneistä, jotka yhdistettynä bioinformatiikan työkaluihin voivat tunnistaa geenejä biologisella reitillä, karakterisoida uusien geenien toimintaa ja havaita sairauden alaluokkia (9). Tätä seulontatekniikkaa käyttämällä olemme tunnistaneet seitsemän geenin alajoukon, joiden ilmentyminen on 0--kertaistunut muutaman ensimmäisen tunnin aikana iskeemisenmunuaistenvahinkoahiiren mallissa. Yksi näistä transkripteistä, kysteiinirikas proteiini 61 (Cyr61), on aivan hiljattain vahvistettu munuaisiskemian indusoimaksi (8), mutta muiden kuuden erilaisesti ilmentyvän geenin käyttäytyminen on uutta ARF-kirjallisuudessa. Tässä tutkimuksessa päätimme karakterisoida lisää yhtä näistä aiemmin tuntemattomista geeneistä, nimittäin neutrofiiligelatinaasiin liittyvää lipokaliinia (NGAL), koska se on pieni erittyvä polypeptidi, joka voi olla havaittavissa virtsasta, erityisesti koska se on proteaasiresistentti. Tuloksemme osoittavat, että NGAL voi edustaa uutta varhaista virtsan biomarkkeria iskeemiselle ja nefrotoksisellemunuaistenvahinkoa.
Materiaalit ja menetelmät
Munuaisiskemia-reperfuusiovaurion hiirimallit
Käytimme vakiintuneita hiiren malleja, joissa lyhyiden ajanjaksojen rakenteelliset ja toiminnalliset seurauksetmunuaisteniskemia on dokumentoitu aiemmin (11–15). Lyhyesti sanottuna urospuolisia Swiss-Webster-hiiriä (Taconic Farms, Germantown, NY), jotka painoivat 25-35 g, pidettiin 12:12-h valo:pimeä-syklissä ja niille annettiin vapaa pääsy ruokaan ja veteen. Eläimet nukutettiin natriumpentobarbitaalilla (50 mg/kg intraperitoneaalisesti) ja asetettiin lämmityspöydälle peräsuolen lämpötilan pitämiseksi 37 asteessa. Käytettiin kolmea erillistä protokollaa: (1) yksipuolinen iskemia ilman ARF:ää, (2) kahdenvälinen iskemia ARF:n kanssa ja (3) kahdenvälinen lievä subkliininen iskemia. Yksipuolisia iskemiakokeita varten vasen munuaisen pedicle suljettiin ei-traumaattisella verisuonipuristimella 45 minuutin ajaksi, jona aikana munuainen pidettiin lämpimänä ja kosteana. Sitten puristin poistettiin, munuaisesta tarkkailtiin verenkierron palautumista ja viilto ommeltiin. Hiirten annettiin toipua lämmitetyssä häkissä, ja ajoitettuja virtsakeräyksiä saatiin. 0, 3, 12 tai 24 tunnin reperfuusion jälkeen eläimet nukutettiin uudelleen, vatsaontelo avattiin ja verta otettiin puhkaisun kautta alemman onttolaskimon kautta seerumin kreatiniinin mittaamiseksi kvantitatiivisella kolorimetrisellä määrityssarjalla (Sigma, St. Louis, MO). Hiiret tapettiin, munuaiset perfuusiokiinnitettiin in situ 4-prosenttisella paraformaldehydillä PBS:ssä ja molemmat munuaiset otettiin talteen (oikea munuainen toimi kunkin eläimen kontrollina). Ainakin kolme erillistä eläintä tutkittiin kullakin uudelleenvirtausjaksolla. Puolet kustakin munuaisesta pikapakastettiin nestetypessä ja säilytettiin 70 asteessa jatkokäsittelyyn asti; näyte kiinnitettiin formaliiniin, upotettiin parafiiniin ja leikattiin (4 m). Parafiinileikkeet värjättiin hematoksyliini-eosiinilla ja tutkittiin histologisesti. Puristetut munuaiset osoittivat iskemia-reperfuusiovauriosta johtuvia tyypillisiä morfologisia muutoksia, kuten muut (12–14) ja me (11) ovat aiemmin julkaisseet. Toinen puolikas kustakin munuaisesta upotettiin OCT-yhdisteeseen (Tissue-Tek), ja pakastetut leikkeet (4 m) saatiin immunohistokemiaa varten. Kahdenvälistä iskemiaa varten ARF-kokeissa molempia munuaisia puristettiin 30 minuutiksi ja niitä tutkittiin eri reflow-jaksoilla, kuten edellä on kuvattu. Tämä kahdeksan eläimen ryhmä suunniteltiin edustamaan kliinistä ARF:ää ja osoitti merkittävän seerumin kreatiniinin nousun 24 tuntia vamman jälkeen. Kahdenvälisiä lieviä subkliinisiä iskemiakokeita varten molemmat munuaiset puristettiin vain 5, 10 tai 20 minuutiksi ja niitä tutkittiin eri reperfuusiojaksoilla, kuten edellä. Tämä lievä vaurion aste suunniteltiin simuloimaan subkliinistä munuaisiskemiaa, ja tämän ryhmän hiirillä ei havaittu seerumin kreatiniinin nousua mitattuna 24 tuntia vaurion jälkeen.
Munuaisiskemia-reperfuusiovaurion rotan malli
Käytimme vakiintuneita jyrsijämallejamunuaisteniskemia-reperfuusiovaurio (10). Lyhyesti sanottuna urospuoliset Sprague-Dawley-rotat, jotka painoivat 200-250 g (Taconic Farms), nukutettiin ketamiinilla (150 g/g) ja ksylatsiinilla (3 g/g) ja niille tehtiin molemminpuolinen munuaisvaltimotukkeus mikrovaskulaarisilla puristimilla 30 minuutin ajan, kuten kohdassa on kuvattu. hiiren protokolla. Ajastetut virtsan keräykset saatiin 3, 6, 9, 12 ja 24 tunnin reperfuusion kohdalla, ja veri kerättiin kreatiniinin mittaamista varten tappamishetkellä (24 tuntia).
Sisplatiinin aiheuttaman munuaisvaurion hiirimalli
Käytimme vakiintuneita hiiren malleja, joissa sisplatiinin antamisen rakenteelliset ja toiminnalliset seuraukset on dokumentoitu aiemmin (16–18). Lyhyesti, hiirille annettiin yksi intraperitoneaalinen injektio sisplatiinia (20 mg/kg ruumiinpainoa). Tämä johtaa tubulussolunekroosiin ja apoptoosiin sekä kohonneeseen veren ureatyppipitoisuuteen 3 päivän kuluessa sisplatiiniinjektion jälkeen (16–18). Eläimiä pidettiin metabolisissa häkeissä, ja virtsakeräyksiä otettiin päivittäin.
RNA:n eristäminen
Hiiren kokonaiset munuaiskudokset (tai viljellyt ihmisen proksimaaliset tubulussolut; katso alla) rikottiin Tissue Terrorilla (Biospec Products, Racine, WI). Kokonais-RNA kontrolli- ja iskeemisistä munuaisista eristettiin käyttämällä RNeasy Mini Kit -sarjaa (Qiagen, Valencia, CA) ja kvantifioitiin spektrofotometrialla.
Microarray-menettelyt
Yksityiskohtaiset kuvaukset microarray-laitteistoista ja -menetelmistä on julkaistu aiemmin (11). Lyhyesti sanottuna jokaisessa kokeessa 100 g puhdistettua hiiren munuaisten kokonais-RNA:ta käänteistranskriptoitiin Superscript II -käänteiskopioijaentsyymillä (Life Technologies, Rockville, MD) Cy3-dUTP:n (Amersham, Piscataway, NJ) kontrolleille ja Cy5-dUTP iskeemisille näytteille. cDNA-näytteet puhdistettiin käyttämällä Microcon YM-50 -suodatinta (Millipore, Madison, WI) ja hybridisoitiin mikrosirulevyille, jotka sisälsivät 8979 ainutlaatuista sekvenssivarmennettua hiiren koetinta (11). Kolme erillistä eläintä tutkittiin kullekin uudelleenvirtausjaksolle, ja kullekin eläimelle suoritettiin vähintään kaksi riippumatonta mikrosirukoetta. Diat skannattiin käyttämällä microarray-skanneria (GenePix 4000B; Axon Instruments, Foster City, CA) erillisten TIFF-kuvien saamiseksi Cy3- ja Cy5-fluoresenssia varten. Signaalin intensiteetit Cy3:lle ja Cy5:lle määritettiin yksittäisille geeneille käyttämällä GenePix Pro 3.0 -tietojen erotusohjelmistoa (Axon Instruments). Laadunvalvonta ja tietojen analysointi suoritettiin aiemmin kuvatulla tavalla (11).

cistanche-kasvi munuaisille
Semikvantitatiivinen käänteistranskriptio-PCR
Sama määrä (1 plus - g) kokonais-RNA:ta kontrolli- ja kokeellisista hiiren munuaisista käänteistranskriptoitiin Superscript II -käänteistranskriptaasilla (Life Technologies) satunnaisten heksameerien läsnä ollessa valmistajan ohjeiden mukaisesti. PCR suoritettiin käyttämällä pakkausta (Roche, Indianapolis, IN) ja seuraavia alukkeita: hiiren NGAL sense 5'-CACCACGGACTACAACCAGT TCGC-3', hiiren NGAL antisense 5'-TCAGTTGTCAATGCATTG GTCGGTG-3}', ihmisen sense 5'-TCAGCCGTCGATACACT GGTC-3' ja Human NGAL antisense 5'-CCTCGTCCGAGTGG TGAGCAC-3'. Alukeparit hiiren ja ihmisen -aktiinille ja glyseraldehydi-3--fosfaattidehydrogenaasille (GAPDH) saatiin Clontechilta (La Jolla, CA). Valereaktiot, joissa ei ollut cDNA:ta, toimivat negatiivisina kontrolleina. PCR-tuotteet analysoitiin agaroosigeelielektroforeesilla, jota seurasi värjäys etidiumbromidilla, ja kvantifioitiin densitometrisesti. Taittomuutokset NGAL-mRNA-ilmentymisessä iskeemisissä ja verrokkimunuaisissa ilmentyivät -aktiini- tai GAPDH-monistuksen normalisoinnin jälkeen.
Mikroskooppi
NGAL:n havaitsemista varten pakasteleikkeet permeabilisoitiin {{0}},2 prosentin Triton X-100:lla PBS:ssä 10 minuutin ajan, blokattiin vuohen seerumilla 1 tunnin ajan ja inkuboitiin primaarisen NGAL-vasta-aineen kanssa ( 1:500 laimennus) 1 tunnin ajan. Objektilasit altistettiin sitten 30 minuutin ajan pimeässä sekundaarisille vasta-aineille, jotka oli konjugoitu Cy5:llä (Amersham, Arlington Heights, IL) ja visualisoitiin fluoresenssimikroskoopilla (Zeiss Axiophot), joka oli varustettu rodamiinisuodattimilla. NGAL:n lokalisoimiseksi Rab11:n kanssa sarjaleikkeitä inkuboitiin ensin NGAL-vasta-aineen tai Rab11-vasta-aineen monoklonaalisen vasta-aineen kanssa (1:500 laimennus; Transduction Laboratories), sitten sekundaaristen vasta-aineiden kanssa, jotka oli konjugoitu joko Cy5:n (NGAL) tai Cy3:n (Rab11) kanssa. ) ja visualisoidaan rodamiini- tai fluoreseiinisuodattimilla, vastaavasti. NGAL:n lokalisoimiseksi yhdessä proliferoivan solun ydinantigeenin (PCNA) kanssa leikkeitä inkuboitiin yhdessä NGAL-vasta-aineen ja PCNA:n monoklonaalisen vasta-aineen kanssa (1:500 laimennus; Upstate), ja havaitseminen suoritettiin immunoperoksidaasivärjäyksellä (ImmunoCruz Staining System, Santa Cruzin biotekniikka). TUNEL-määritykseen käytimme ApoAlert DNA Fragmentation Assay Kit -sarjaa (Clontech). Parafiinileikkeistä deparafiini tehtiin ksyleenillä ja laskevilla etanolilla, kiinnitettiin 4 prosentilla formaldehydillä/PBS:llä 30 minuuttia 4 asteessa, permeabilisoitiin proteinaasi K:lla huoneenlämpötilassa 15 minuutin ajan ja 0,2 prosentin Triton X-100/PBS:llä 15 minuutin ajan. min 4 asteessa ja inkuboitiin nukleotidien ja TdT-entsyymin seoksen kanssa 60 min 37 asteessa. Reaktio lopetettiin kahdella SSC:llä ja leikkeet pestiin PBS:llä ja kiinnitettiin Crystal/mountilla (Biomed, Foster City, CA). TUNEL-positiiviset apoptoottiset ytimet havaittiin visualisoimalla fluoresenssimikroskoopilla.
Virtsan kokoelma
Hiiret tai rotat sijoitettiin aineenvaihduntahäkkeihin (Nalgene, Rochester, NY), ja virtsa kerättiin ennen ja joka tunti sen jälkeen.munuaistenvaltimon tukos. Virtsanäytteet sentrifugoitiin nopeudella 5 000 g roskien poistamiseksi, ja supernatantti analysoitiin Western blot -menetelmällä. Virtsan kreatiniini mitattiin kvantitatiivisella kolorimetrisellä määrityssarjalla (Sigma) näytteiden normalisoimiseksi virtsan NGAL-määritystä varten. Kolorimetrinen määrityssarja N-asetyyli-D-glukosaminidaasin (NAG) määrittämiseksi virtsasta hankittiin Rochelta.
Soluviljely
Ihmisenmunuaistenproksimaaliset tubulaariset epiteelisolut (RPTEC) saatiin Cloneticsilta (San Diego, CA). Soluja kasvatettiinmunuaistenepiteelisolujen tyviväliaine täydennettynäMunuaisetEpiteelisolujen kasvualusta (REGM) -kompleksi ({{0}},5 l/ml hydrokortisonia, 10 pg/ml hEGF, 0.5 - g/ml epinefriiniä, 6,5 pg/ml trijodityroniinia, 10 plus - g/ml transferriinia, 5 - g/ml insuliinia, 1 -g/ml gentamysiinisulfaattia ja 2 % FBS:ää), valmistajan suosittelemalla tavalla.
Viljeltyjen solujen lievä ATP-häviö
Muokkasimme aiemmin kuvattuja in vitro iskemian protokollia ATP-vajauksella oksidatiivisen fosforylaation estäjillä (19, 20). Toisena päivänä konfluenssin jälkeen RPTEC-soluja inkuboitiin 1 m:n kanssa antimysiini A:ta (Sigma) vaihtelevien ajanjaksojen ajan aina 6 tuntiin asti. Olemme aiemmin osoittaneet, että tämä johtaa lievään osittaiseen palautuvaan ATP:n ehtymiseen eikä solujen elinkelpoisuuden menetystä muun tyyppisissä viljellyissä munuaisepiteelisoluissa, kuten MDCK (19) ja 786-O (20) soluissa. ATP-tasoja tarkkailtiin käyttämällä lusiferaasipohjaista määrityspakkausta (Sigma) ja ilmaistiin prosentteina kontrolliarvoista. Solut kerättiin eri ajankohtina ATP:n ehtymisestä ja analysoitiin NGAL-mRNA:n ilmentymisen suhteen käänteistranskriptio-PCR:llä (RT-PCR) ja NGAL-proteiinin ilmentymisen suhteen Western-analyysillä. NGAL:n erittymistä elatusaineeseen seurattiin myös.
Muut materiaalit ja menetelmät
Kaikki kemikaalit ostettiin Sigmalta, ellei toisin mainita. Western blottausta varten proteiinipitoisuudet määritettiin Bradford-määrityksellä (Bio-Rad, Hercules, CA), ja jokaiseen kaistaan ladattiin yhtä suuret määrät kokonaisproteiinia. Monoklonaalista vasta-ainetta - -tubuliinille (Sigma) käytettiin laimennoksena 1:10,000 tasaisen proteiinikuormituksen varmistamiseksi, ja polyklonaalista vasta-ainetta NGAL:lle käytettiin suhteessa 1:500 (21). Monoklonaalista vasta-ainetta 2-mikroglobuliinille käytettiin suhteessa 1:500 (Sigma). Siirrettyjen proteiinien immunodetektio saavutettiin käyttämällä tehostettua kemiluminesenssia (Amersham).
Tulokset
Varhaisen munuaisiskemia-reperfuusiovaurion eläinmallien karakterisointi
Käytimme hiiren malleja, joissa lyhytkestoisten munuaisiskemian rakenteelliset ja toiminnalliset seuraukset on dokumentoitu (11–15). Iskeemisen vaurion tyypilliset histopatologiset piirteet ilmenivät helposti 24-h-reperfuusionäytteissä sekä toispuolisen (45 min) että kahdenvälisen (30 min) iskemian jälkeen. Näitä olivat harjan reunakalvojen menetys, putkien laajentuminen, litistynyt putkimainen epiteeli, luminaaliset jätteet ja interstitiaaliset infiltraatit (kuva 1). Dokumentoimme apoptoottisten solujen läsnäolon käyttämällä TUNEL-määritystä. Apoptoosi sijoittui pääasiassa distaalisiin tubulaarisiin soluihin ja Henlen silmukan nouseviin raajoihin, sekä irtautuneissa soluissa ontelon sisällä että kiinnittyneissä soluissa. Satunnaiset proksimaaliset tubulussolut olivat myös apoptoottisia, mutta glomerulukset olivat olennaisesti vailla apoptoosia. TUNEL-positiivisia soluja ei havaittu kontrollimunuaisissa tai iskeemisissä näytteissä, joista TdT jätettiin pois (ei esitetty). Yllä mainitut histologiset ja apoptoottiset muutokset puuttuivat munuaisista, jotka oli altistettu lievemmille iskemia-asteille (5, 10 tai 20 minuuttia kahdenvälistä iskemiaa; ei esitetty). Seerumin kreatiniinitasot heijastivat havaittuja histopatologisia muutoksia. Siten hiirillä, joilla oli yksipuolinen munuaisiskemia tai lievä subkliininen bilateraalinen iskemia, havaittiin seerumin kreatiniinitasoja, joita ei voitu erottaa kontrollieläimistä, kun taas hiiret, joilla oli molemminpuolinen iskemia 30 minuutin ajan, osoittivat seerumin kreatiniinin merkittävää nousua (kuvio 1).

Kuva 1. Iskeemisen hiirimallin karakterisointimunuaistenvahinkoa. Vasemmanpuoleiset paneelit näyttävät tulokset hematoksyliini- ja eosiinivärjäyksestä (ylhäällä) ja TUNEL-värjäyksestä (alhaalla) kontrollihiirten munuaisleikkeistä tai 24 tunnin iskemia-reperfuusion (IRI) jälkeen. (Oikealla) Seerumin kreatiniinimääritysten tulokset kontrollihiirillä (Con), yksipuolisen iskemian jälkeen 45 minuutin ajan (U45) tai kahdenvälisen iskemian jälkeen eri ajanjaksoina, kuten on esitetty. *P 0.05 vs. kontrolli. Palkkien sisällä olevat numerot osoittavat eläinten lukumäärän.
NGAL-mRNA indusoituu merkittävästi varhaisessa postskeemisessa munuaisessa
Mikrosiruanalyysillä hiiristä, joilla on yksipuolinenmunuaisteniskemia, NGAL:n havaittiin indusoituvan jatkuvasti (3,2 plus - 0.5-kertainen, 11,1 plus - 1.2-kertainen ja 4,3 plus {{1{{30} }}}.6-kertainen 3, 12 ja 24 tunnin reperfuusion kohdalla) iskeemisessä hiiren munuaisessa verrattuna saman eläimen kontrollimunuaisiin (keskiarvo plus - SD kolmelta eläimeltä kullakin aikapisteellä). Tämä havainto vahvistettiin semikvantitatiivisella RT-PCR:llä käyttäen normalisointiprotokollaa sekä plus-aktiinilla että GAPDH:lla. Mitään merkittäviä muutoksia plus-aktiinin tai GAPDH:n mRNA-ilmentymisessä ei havaittu millään tutkituista reperfuusiojaksoista, kuten aiemmin on kuvattu (11). Hiirispesifisiä alukkeita käyttämällä havaitsimme kuitenkin merkittävän NGAL-mRNA-ekspression lisääntymisen (4,1 plus -0.5-kertainen, 9 plus -0.6-kertainen ja 4,2 plus 0.{31}}kertaiseksi 3, 12 ja 24 tunnin reperfuusion kohdalla, missä arvot edustavat kolmen erillisen eläimen keskiarvoa plus -SD). Nämä tulokset on havainnollistettu kuvassa 2 ja ne ovat yleisesti ottaen yhtäpitäviä transkriptioanalyysillä havaittujen muutosten kanssa.

Kuvio 2. Hiiren munuaisen neutrofiiligelatinaaseihin liittyvän lipokaliinin (NGAL) mRNA:n induktio iskemian jälkeen. (Yläosa) Edustava käänteistranskriptio-PCR (RT-PCR) alukkeilla hiiren aktiinille ja NGAL:lle, käyttämällä kontrollihiirten (C) munuaisista uutettua RNA:ta tai erilaisten reperfuusiojaksojen jälkeen kuvan mukaisesti (tunteja). Kaista M sisältää 100-emäsparin DNA-tikkaat. (Alhaalla) Taittuu NGAL-mRNA-ilmentymisen lisääntyminen eri ajankohtina kontrollista (CON). Arvot, jotka on saatu mikrosirulla (yhtenäinen viiva) verrattuna RT-PCR:ään (katkoviiva), ovat keskiarvoja SD kolmesta kokeesta kullakin aikapisteellä.
NGAL-proteiini on selvästi yli-ilmentynyt varhaisten iskeemisten hiiren munuaisten proksimaalisissa tubuluksissa
Seuraavaksi oli mielenkiintoista määrittää, onko NGAL-proteiinin postskeeminen ilmentyminen munuaisissa rinnakkainen mRNA:n kanssa. Western-analyysin mukaan NGAL oli juuri havaittavissa 25-kD-immunoreaktiivisena peptidinä kontrollihiiren munuaisissa. Tämän vyöhykkeen identiteetti NGAL:na määritettiin erillisessä koesarjassa, jossa primaarisen vasta-aineen esi-inkubointi rekombinantin hiiren lipokaliinin kanssa esti täysin tämän immunoreaktiivisuuden (ei esitetty). Yksipuolisissa iskemiakokeissa NGAL:n ilmentyminen indusoitiin 3-4-kertaisesti densitometrialla iskeemisessä munuaisessa viidestä erillisestä eläimestä 3 tunnin sisällä vauriosta, kuten kuvassa 3 esitetään. Tämä vaste parani dramaattisesti kahdeksasta erillisestä eläimestä tehdyissä kahdenvälisissä iskemiakokeissa. . Näissä hiirissä NGAL indusoitiin kolminkertaisesti 3 tunnin reperfuusion jälkeen, huippu oli 12--kertainen 24- tunnin näytteissä ja laski normaalille tasolle 72- tunnin palautumisjakson aikana (kuva 3). .
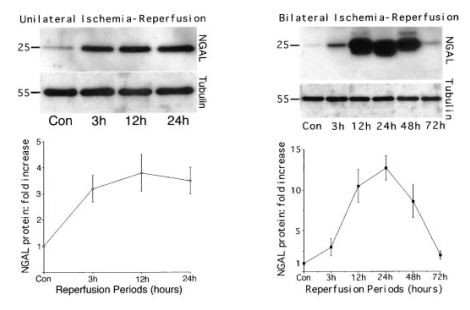
Kuva 3. Hiiren munuaisen NGAL-proteiinin induktio toispuolisen tai kahdenvälisen iskemian jälkeen. (Yläosa) Edustavat Western blot -näytteet kokonaisista munuaisnäytteistä, jotka on saatu kontrollihiiristä (Con) tai reperfuusiojaksojen jälkeen, kuten on esitetty (tunteja), tutkittu polyklonaalisella vasta-aineella NGAL:lle tai monoklonaalisella vasta-aineella tubuliinia vastaan (saman proteiinikuormituksen osoittamiseksi). Molekyylipainomerkit ovat vasemmalla. (Alhaalla) Taittuu NGAL-proteiinin ilmentymisen lisääntyminen eri ajankohtina kontrollista (CON). Densitometrisesti saadut arvot ovat keskiarvoja SD viideltä eläimeltä toispuolisen iskemian ja kahdeksan eläimen kahdenvälisen iskemian osalta
Immunohistokemiallisia tekniikoita käyttäen osoitimme seuraavaksi, että NGAL-proteiini oli tuskin havaittavissa kontrollihiiren munuaisissa, mutta se säätelee pääasiassa proksimaalisissa tubuluksissa 3 tunnin sisällä iskemiasta, kuten kuvassa 4. Proksimaalisten tubulusten tunnistaminen näissä osissa perustui harjan läsnäoloon. rajakalvo, tuman suhde solukoon ja solun morfologia. Indusoitu NGAL esiintyi pisteittynä sytoplasmisessa jakautumisessa proksimaalisissa tubulussoluissa, muistuttaen erittyvää proteiinia. Tämä ilmentymismalli oli identtinen sekä yksi- että kahdenvälisissä iskemia-reperfuusiovaurion malleissa ja se oli johdonmukaisesti ilmeinen jokaisessa tutkitussa eläimessä. Munakeräsistä puuttui NGAL:n ilmentyminen, eikä NGAL:ia ekspressoivia neutrofiilejä ollut havaittavissa. Koska NGAL:n on osoitettu viljellyissä Wilmsin kasvainmunuaissoluissa lokalisoituvan ainakin osittain endosomien kanssa (21), tutkimme sarjaosissa NGAL:n ja Rab11:n (myöhään kierrättyvien endosomien merkkiaine) jakautumista. Yhdistetyt kuvat osoittivat NGAL:n merkittävän samanaikaistumisen Rab11:n kanssa (kuva 4). Tutkiaksemme tehostuneen NGAL-ilmentymisen toiminnallista merkitystä iskemian jälkeen, tutkimme sarja munuaisleikkeitä NGAL-ilmentymisen, TUNEL-positiivisten ytimien tai PCNA-positiivisten ytimien varalta. Vaikka NGAL:ia yliekspressoivat tubulussolut eivät olleet TUNEL-positiivisia (ei esitetty), NGAL:n ja PCNA:n merkittävä samanaikainen lokalisoituminen oli ilmeistä lisääntyvissä ja regeneroituvissa soluissa 48-h-reflow-jaksolla (kuva 4).

Kuva 4. Hiiren munuaisen NGAL-proteiinin induktio iskemian jälkeen. (Yläosa) Edustavia immunohistokemiallisia tuloksia hiiren munuaisten jäädytetyistä leikkeistä, jotka on saatu kontrollihiiristä tai vaihtelevien uudelleenvirtausjaksojen jälkeen, kuten on esitetty (tunteja), jotka on tutkittu polyklonaalisella NGAL-vasta-aineella. G, glomerulus. Paneeli, jossa on merkintä HP, on suuritehoinen 100 plus -suurennus, ja muut paneelit ovat 20:ssä. (Alhaalla) Kahdessa vasemmassa paneelissa näkyy tubulus 3 tunnin reperfuusion jälkeen, joka ilmaisee NGAL:ia (punainen) tai Rab11:tä (vihreä). Kolmannessa paneelissa näkyy yhdistetty kuva, joka ilmaisee yhteispaikannusta keltaisella. Oikealla äärimmäisessä paneelissa näkyy NGAL:n ja proliferoivan solun ydinantigeenin samanaikainen lokalisointi tubuluksissa 48 tunnin uudelleenvirtauksen jälkeen.
NGAL-proteiini havaitaan helposti virtsasta heti ARF:n induktion jälkeen hiirillä
Seuraavaksi oli huomattavan mielenkiintoista määrittää, voidaanko NGAL-proteiinin postskeeminen ilmentyminen havaita virtsasta, mikä viittaa sen käyttökelpoisuuteen iskeemisen varhaisena ei-invasiivisena biomarkkerina.munuaistenvahinkoa. Kun virtsan kreatiniinipitoisuuksia käytettiin tasaamaan näytteen lataamista varten, NGAL puuttui virtsasta ennen iskemiaa. Silmiinpistävä vastakohtana NGAL ilmeni 25-kD-vyöhykkeenä 2 tunnin sisällä vauriosta (ensimmäisessä virtsan erittyessä iskemian jälkeen) kaikissa tutkituissa eläimissä (viidellä yksipuolisella ja kahdeksalla kahdenvälisellä iskemialla), kuten Kuvio 5. Tämän vyöhykkeen identiteetti NGAL:na määritettiin erillisessä koesarjassa, jossa primaarisen vasta-aineen esi-inkubointi rekombinantin hiiren lipokaliinin kanssa esti täysin tämän immunoreaktiivisuuden (ei esitetty). On huomattava, että NGAL oli helposti havaittavissa vain 1 litrassa käsittelemätöntä virtsaa Western-analyysillä ja säilyi koko tutkitun ajan (24 tunnin reperfuusio). Tämän jälkeen vertailimme virtsan NGAL-eritystä aiemmin vahvistettuihin vauriomarkkereihin, kuten 2-mikroglobuliiniin ja NAG:hen. Kun virtsan NGAL havaittiin 2 tunnin sisällä iskemiasta, 2-mikroglobuliini havaittiin samoissa virtsanäytteissä vasta 12 tunnin toispuoleisen ja 8 tunnin kahdenvälisen iskemian jälkeen (kuva 5). Samoin virtsan NAG-eritys lisääntyi merkitsevästi vasta 12 tunnin yksipuolisen ja 8 tunnin kahdenvälisen iskemian jälkeen verrattuna ei-iskeemisiin kontrollieläimiin (kuvio 5).
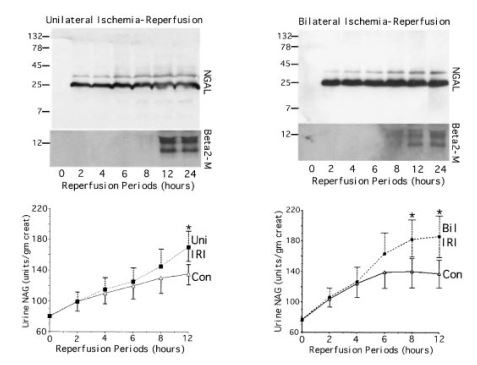
Kuva 5. NGAL-proteiinin varhainen havaitseminen virtsasta hiirillä, joilla on iskeeminen akuuttimunuaistenvika (ARF). (Yläosa) Käsittelemättömien virtsanäytteiden edustavat Western blot -näytteet (1 - 2 plus - l kaistaa kohti, normalisoitu kreatiniinipitoisuuden suhteen) saatiin kuvan mukaisilla reperfuusiojaksoilla (tunteja) toispuolisen tai kahdenvälisenmunuaistenvaltimon kiristys. Molekyylipainomerkit näkyvät vasemmalla. Blotit tutkittiin NGAL:lla (ylhäällä) tai {{0}}mikroglobuliinilla (Beta2-M; keskellä). (Alhaalla) Virtsan N-asetyyli-D-glukosaminidaasi (NAG) -määritykset eri reperfuusiojaksoilla, kuten on osoitettu, viideltä eläimeltä toispuoleisen iskemian ja kahdeksan eläimen kahdenvälisen iskemian osalta. Arvot ovat keskimääräisiä SD. *P 0,05 verrattuna kontrolliin kullakin aikapisteellä, ANOVA.
NGAL-proteiini havaitaan helposti virtsasta jopa lievän munuaisiskemian jälkeen hiirillä
Virtsan NGAL-ilmaisun herkkyyden määrittämiseksi ilman ilmeistä ARF:ää käytimme protokollia, joissa erilliset hiiret altistettiin vain 5, 10 tai 20 minuutin kahdenvälisille tutkimuksille.munuaistenvaltimon tukos. Nämä tutkimukset suunniteltiin arvioimaan NGAL:n erittymistä virtsaan lievän subkliinisen munuaisiskemian jälkeen. Seerumin kreatiniini, joka mitattiin 24 tunnin uudelleenvirtauksen jälkeen, oli normaaleissa rajoissa kaikissa näissä hiirissä (kuva 1). Hämmästyttävää, NGAL havaittiin helposti vain 1 litrassa käsittelemätöntä virtsaa näissä eläimissä (kuva 6), vaikka sen ilmaantuminen oli jonkin verran viivästynyt verrattuna eläimiin, joilla oli selvä ARF. Siten, kun 30 minuutin kahdenvälinen iskemia johti virtsaan NGAL:n erittymiseen 2 tunnissa (kuva 5), hiirillä, joilla oli 20 tai 10 minuuttia molemminpuolista iskemiaa, virtsan NGAL ilmeni 4 tunnin kuluttua ja ne, joilla oli 5 minuutin iskemia, erittivät NGAL:n vasta 6 tunnin kuluttua ( kuva 6). Siten NGAL:n esiintyminen virtsassa korreloi munuaisiskemian annoksen ja keston kanssa.
NGAL-proteiini havaitaan helposti virtsasta heti ARF:n induktion jälkeen rotilla

Kuva 6. NGAL-proteiinin havaitseminen virtsasta hiirillä, joilla on subkliininen munuaisiskemia. Edustava Western blot käsittelemättömistä virtsanäytteistä (1-2 l per kaista, normalisoitu kreatiniinipitoisuuden suhteen), joka on saatu kuvan mukaisilla reperfuusiojaksoilla (tunteja) 5, 10 tai 20 minuutin molemminpuolisen munuaisvaltimoiden puristamisen jälkeen. Molekyylipainomerkit näkyvät vasemmalla. Näillä eläimillä oli normaali seerumin kreatiniini 24 tunnin kuluttua uudelleenvirtauksesta.
Koska keskustelua käydään lajieroista munuaisvaltimoiden tukoksen aiheuttamissa reaktioissa (22), tutkimme seuraavaksi NGAL:n käyttäytymistä eri eläinmallissa, nimittäin vakiintuneessa munuaisiskemia-reperfuusiovaurion rottamallissa. Kun virtsan kreatiniinipitoisuuksia käytettiin tasaamaan näytteen lataamista varten, NGAL puuttui virtsasta ennen iskemiaa. Sitä vastoin NGAL ilmeni 25-kD immunoreaktiivisena peptidinä 3 tunnin sisällä vauriosta (ensimmäisenä virtsan erittyessä iskemian jälkeen), kuten kuvassa 7 on esitetty. Vertailun vuoksi seerumin kreatiniini tässä mallissa iskeeminen vaurio lisääntyi vasta 24 tunnin reperfuusion jälkeen (ei esitetty). Jälleen kerran NGAL havaittiin 1 litrassa käsittelemätöntä virtsaa ja säilyi koko tutkitun ajan (24 h reperfuusio).

Kuva 7. NGAL-proteiinin varhainen havaitseminen virtsasta rotilla, joilla on iskeeminen ARF. Edustava Western blot -analyysi käsittelemättömistä virtsanäytteistä (1-2 l per kaista, normalisoitu kreatiniinipitoisuuden suhteen), joka on saatu kuvan mukaisilla reperfuusiojaksoilla (tunteja), 30 minuutin kahdenvälisen munuaisvaltimon puristuksen jälkeen rotilla. Molekyylipainomerkit näkyvät vasemmalla. Näillä eläimillä oli merkittävä seerumin kreatiniinin nousu 24 tunnin kuluttua uudelleenvirtauksesta.
NGAL-mRNA indusoituu viljellyissä ihmisen proksimaalisissa tubulussoluissa varhaisen lievän iskemian jälkeen
Vahvistaaksemme NGAL:n alkuperän iskeemisistä proksimaalisista tubulussoluista modifioimme aiemmin kuvattuja in vitro iskemian protokollia ATP-depletiolla viljellyissä ihmisen proksimaalisissa tubulussoluissa (RPTEC). Inkubaatio on 1-m antimysiiniä, mikä johti lievään osittaiseen ATP-vajautumiseen noin 83 plus 3 prosenttiin kontrollista 1 tunnin sisällä, ja asteittainen lasku noin 75 plus - 3 prosenttiin kontrollista 6 tunnissa ( keskimääräinen SD neljästä kokeesta). Tämän lievän ATP-vajeen morfologisia seurauksia ei havaittu. NGAL-mRNA oli juuri havaittavissa lepäävissä soluissa. Kuitenkin ATP:n osittaisen ehtymisen jälkeen nopea ja kestosta riippuvainen NGAL-mRNA:n induktio oli ilmeistä RT-PCR:llä, kuten kuvassa 8 esitetään.
NGAL-proteiini havaitaan helposti väliaineesta varhaisen iskemian jälkeen in vitro
Seuraavaksi tutkimme NGAL-proteiinin ilmentymistä RPTEC-soluissa ja elatusaineessa lievän ATP-vajeen jälkeen. NGAL-proteiini oli havaittavissa kontrolli-RPTEC-soluissa, ja sen ilmentyminen lisääntyi ATP:n ehtymisen jälkeen kestosta riippuvalla tavalla, kuten kuvassa 8 on esitetty. NGAL-immunoreaktiivista proteiinia ei löydetty kontrollisolujen viljelyväliaineesta, mutta NGAL oli helposti havaittavissa 1:n sisällä. h lievää ATP-vajetta (kuvio 8). NGAL-proteiinin runsauden lisäntymistä havaittiin liittyen ATP:n ehtymisen kestoon. Nämä tulokset viittaavat siihen, että indusoitu NGAL-proteiini erittyy nopeasti elatusaineeseen, analogisesti NGAL:n nopean ilmaantumisen kanssa virtsaan munuaisiskemian jälkeen in vivo.
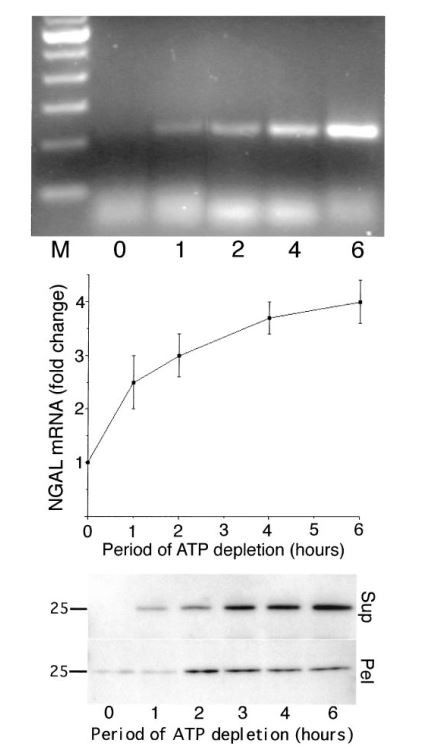
Kuvio 8. NGAL-mRNA:n induktio iskemian jälkeen in vitro. (Yläosa) Edustava RT-PCR alukkeilla ihmisen NGAL:lle, käyttäen RNA:ta, joka on uutettu munuaisten proksimaalisista tubulaarisista epiteelisoluista (RPTEC) eri jaksojen osittaisen ATP:n ehtymisen jälkeen kuvan mukaisesti (tunteja). Kaista M sisältää 100-emäsparin DNA-tikkaat. (Keski) NGAL-mRNA:n ilmentymisen kertainen lisääntyminen eri ajankohtina kontrollista (0), normalisoitu glyseraldehydi-3-fosfaattidehydrogenaasin ilmentymiselle. Esitetyt arvot ovat keskiarvoja kolmen kokeen keskiarvosta kullakin aikapisteellä. (Alhaalla) Edustava Western blot RPTEC-näytteillä eri jaksojen osittaisen ATP:n ehtymisen jälkeen, kuten on esitetty (tunteja), saatu yhtä suuresta määrästä solupellettejä (Pel) tai viljelyalustaa (Sup), tutkittu polyklonaalisella NGAL-vasta-aineella. Molekyylipainomerkit ovat vasemmalla. Kuva edustaa kolmea erillistä koetta.
NGAL-proteiini havaitaan helposti virtsasta varhain sisplatiinin aiheuttaman munuaistoksisuuden indusoinnin jälkeen
Seuraavaksi halusimme määrittää, voidaanko NGAL:ia havaita virtsasta muiden tubulussoluvaurioiden jälkeen. Vakiintuneessa sisplatiinin nefrotoksisuuden hiirimallissa NGAL havaittiin helposti virtsasta 1 päivän sisällä sisplatiinin antamisesta (kuva 9). Sitä vastoin virtsan 2-mikroglobuliini oli tuskin havaittavissa 2 vuorokauden kuluttua, ja se voitiin havaita luotettavasti vasta päivänä 4–5 sisplatiinin jälkeen. Vastaavasti lisääntynyt NAG:n erittyminen virtsaan oli ilmeistä vasta 4. ja 5. päivänä sisplatiinin annon jälkeen (kuvio 9).
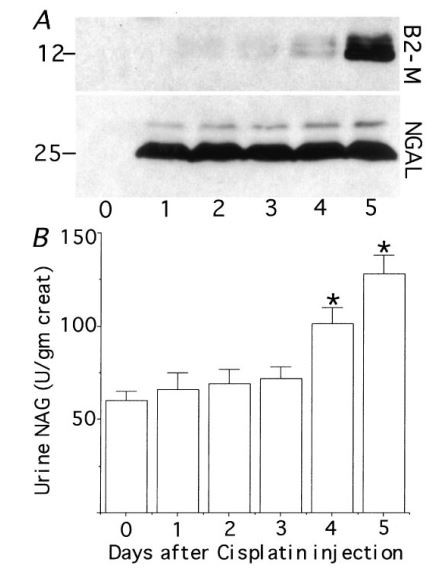
Kuva 9. NGAL-proteiinin varhainen havaitseminen virtsasta hiirillä, joilla on sisplatiinin aiheuttama vaurio. (A) Edustavat Western blot -tutkimukset käsittelemättömistä virtsanäytteistä (1-2 l per kaista, normalisoitu kreatiniinipitoisuuden suhteen), jotka on saatu päivinä sisplatiinin annon jälkeen, ja jotka on tutkittu 2-mikroglobuliinin tai NGAL:n vasta-aineella. Molekyylipainomerkit näkyvät vasemmalla. (B) Virtsan NAG-määritykset eri päivinä sisplatiinin annon jälkeen (n 4). Arvot ovat keskiarvo plus -SD. *P 0.05 vs. päivä 0.
Keskustelu
Käytimme transkriptionlaajuista kyselystrategiaa tunnistaaksemme munuaisgeenit, jotka indusoituvat varhain munuaisiskemian jälkeen ja joiden proteiinituotteet voisivat toimia uusina biomarkkereina ARF:lle. Tunnistamme seitsemän geeniä, jotka ovat 10--kertaisesti säädeltyjä, joista yhden (Cyr61) on äskettäin raportoitu indusoituneen munuaisiskemian jälkeen (8). Yllättäen kuuden muun transkription induktio oli uutta ARF-kentässä. Tässä tutkimuksessa päätimme karakterisoida lisää yhtä näistä aiemmin tunnistamattomista geeneistä, nimittäin NGAL:ia.
NGAL kuuluu lipokaliinien superperheeseen - 20 rakenteellisesti samankaltaisista erittyneistä proteiineista, joiden uskotaan kuljettavan erilaisia ligandeja verhiön sisällä (23). Ihmisen NGAL tunnistettiin alun perin 25-kD-proteiiniksi, joka on kovalenttisesti sitoutunut ihmisen neutrofiilien gelatinaasiin, missä se edustaa yhtä neutrofiilien sekundaarisista raeproteiineista (24, 25). Molekyylikloonaustutkimukset ovat paljastaneet ihmisen NGAL:n olevan samanlainen kuin hiiren 24p3-geeni, joka tunnistettiin ensin hiiren munuaisten primääriviljelmissä, jotka indusoitiin lisääntymään (26). NGAL ekspressoituu erittäin alhaisina määrinä muissa ihmisen kudoksissa, mukaan lukien munuaiset, henkitorvi, keuhkot, mahalaukku ja paksusuolen (27). NGAL-ilmentyminen indusoituu merkittävästi stimuloidussa epiteelissä. Se on esimerkiksi lisääntynyt paksusuolen epiteelisoluissa tulehdus- tai neoplasia-alueilla, mutta se puuttuu välissä olevilta alueilta tai metastaattisilta vaurioilta (28). NGAL-pitoisuudet ovat kohonneet potilaiden seerumissa, joilla on akuutti bakteeri-infektio (29), astmaa tai kroonista obstruktiivista keuhkosairautta sairastavien potilaiden ysköksessä (30) ja keuhkoputken nesteessä keuhkolaajentuneesta keuhkoista (31). Kaikissa näissä tapauksissa NGAL-induktion oletetaan olevan seurausta tulehdussolujen ja epiteelisolujen välisistä vuorovaikutuksista, ja NGAL-ilmentymisen lisääntyminen on ilmeistä sekä neutrofiileissä että epiteelissä (28–32).
NGAL:n lisääntymistä kypsässä munuaisessa ei ole tähän mennessä kuvattu. Useat tutkimuksestamme kerätyt todisteet viittaavat siihen, että havaittu NGAL-induktio edustaa munuaisten proksimaalisten tubulussolujen uutta luontaista vastetta iskeemiselle vauriolle, eikä se johdu pelkästään aktivoiduista neutrofiileistä. Ensinnäkin vaste on erittäin nopea, ja NGAL ilmaantuu virtsaan 2 tunnin sisällä vauriosta (ensimmäisenä virtsan erittyessä munuaisvaltimon tukkeutumisen jälkeen), ja munuaisten neutrofiilien kerääntyminen tässä iskeemisen ARF:n mallissa havaitaan yleensä ensimmäisen kerran 4 tunnin kuluttua. loukkaantumisen jälkeen (33-35). Toiseksi NGAL-induktion ja neutrofiilien kertymisen ajalliset mallit ovat erilaisia. NGAL-mRNA:n ja proteiinin ilmentyminen havaittiin maksimissaan 12 tunnin kuluttua uudelleenvirtauksesta, kun taas neutrofiilien kertymisen huippu on 24 tunnin kohdalla (33–35), johon mennessä NGAL:n ilmentyminen on vähentynyt merkittävästi. Kolmanneksi tutkituissa munuaisnäytteissä ei ollut havaittavissa NGAL-proteiinia ilmentäviä neutrofiilejä immunofluoresenssilla (kuvio 4). Neljäs ja vakuuttavin, NGAL-mRNA:n ja proteiinin induktion dokumentoitiin tapahtuvan viljellyissä ihmisen proksimaalisissa tubulussoluissa in vitro iskemian jälkeen, jolloin NGAL erittyi viljelyalustaan 1 tunnin sisällä ATP:n ehtymisestä järjestelmässä, jossa neutrofiilit puuttuvat kokonaan. In vivo -tutkimuksemme eivät kuitenkaan anna meidän sulkea kokonaan pois jotakin vaikutusta aktivoituneiden neutrofiilien tunkeutumisesta havaittuun NGAL-ylössääntelyyn. Todellakin, on mahdollista, että NGAL:n voimistuminen munuaisten tubulussoluissa voi indusoitua sytokiinien paikallisella vapautumisella mikroverenkiertoon jääneistä neutrofiileistä aikaisin iskeemisen vaurion jälkeen.

Mikä on cistanche? Cistanchevoi hoitaamunuaistenvahinkoa
Riittävä selitys NGAL:n induktiolle stimuloidun epiteelin vaikutuksesta on puuttunut, ja on epäselvää, onko NGAL suojaava tai lähellä vammoja tai jopa viatonta sivustakatsojaa. Viimeaikaiset todisteet viittaavat siihen, että ainakin osassa solutyyppejä NGAL voi edustaa proapoptoottista molekyyliä (36–38). Hiiren pro-B-lymfosyyttisolulinjassa sytokiinien poisto johti huomattavaan NGAL:n induktioon sekä apoptoosin alkamiseen (36, 37). NGAL on myös yhdistetty lisääntymiskudosten apoptoosiin. Kiertyvän maitorauhasen ja kohdun epiteelisolut ilmentävät korkeita NGAL-tasoja, mikä ajallisesti osuu yhteen maksimaalisen apoptoosin ajanjakson kanssa (38). On todennäköistä, että NGAL säätelee solupopulaatioiden alajoukkoa indusoimalla apoptoosia. Stimuloitu epiteeli voi lisätä NGAL:n säätelyä indusoimaan tunkeutuvien neutrofiilien apoptoosia, jolloin solut voivat selviytyä tulehdusvasteen tuhoista. Vaihtoehtoisesti epiteelisolut voivat käyttää tätä mekanismia säätelemään omaa kuolemaansa. On kuitenkin mielenkiintoista huomata tutkimuksissamme, että NGAL:n induktio varhaisen munuaisiskemia-reperfuusiovaurion jälkeen tapahtuu pääasiassa proksimaalisissa tubulussoluissa, joissa ei ollut TUNEL-positiivisia ytimiä.
Muut viimeaikaiset tutkimukset ovat paljastaneet, että NGAL parantaa epiteelin fenotyyppiä. NGAL ilmentyy tunkeutuvassa virtsaputken silmussa ja laukaisee nefrogeneesin stimuloimalla mesenkymaalisten solujen muuttumista munuaisepiteeliksi (21). Toisen lipokaliinin, glykodeliinin, on osoitettu indusoivan epiteelifenotyyppiä, kun sitä ilmennetään ihmisen rintasyöpäsoluissa (40). Nämä löydökset koskevat erityisesti kypsää munuaista, jossa yksi hyvin dokumentoiduista reaktioista iskeemiseen vaurioon on proksimaalisia tubuluksia ympäröivien dedifferentioituneiden epiteelisolujen huomattava esiintyminen (41). Tärkeä näkökohta munuaisten regeneraatiossa ja korjaamisessa iskeemisen vaurion jälkeen sisältää epiteelin fenotyypin uudelleen hankkimisen, prosessi, joka toistaa useita normaalin kehityksen näkökohtia (42). Tämä viittaa siihen, että vaurioitunut tubulus voi ilmentää NGAL:ia uudelleen epitelisoitumisen indusoimiseksi. Tuki tälle käsitteelle perustuu äskettäin tunnistettuun NGAL:n rautaa kuljettavaksi proteiiniksi, joka on komplementaarinen transferriinille nefrogeneesin aikana (21). On hyvin tunnettua, että raudan kuljettaminen soluihin on ratkaisevan tärkeää solujen kasvulle ja kehitykselle, ja tämä on oletettavasti kriittistä postskeemiiselle munuaisten regeneraatiolle aivan kuten se on ontogenian aikana. Koska NGAL näyttää sitovan ja kuljettavan rautaa (21), on myös todennäköistä, että NGAL voi toimia vaurioituneiden proksimaalisten tubulusepiteelisolujen raudan nieluna. Koska NGAL voidaan endosytoosia proksimaalisella tubuluksella (K. Mori ja J. Barasch, julkaisemattomat havainnot), proteiini voisi mahdollisesti kierrättää rautaa eläviin soluihin. Tämä saattaa stimuloida kasvua ja kehitystä sekä poistaa raudan, reaktiivisen molekyylin, kudosvauriopaikalta, mikä rajoittaa raudan välittämää sytotoksisuutta. Tuloksemme osoittavat, että NGAL:n samanaikainen lokalisointi PCNA-positiivisissa uusiutuvissa ja lisääntyvissä tubulussoluissa antaa lisätukea tälle hypoteesille.
Löytöjemme suuri merkitys liittyy mahdollisuuteen, että NGAL on uusi virtsan biomarkkeri iskeemiselle sairaudelle.munuaistenvahinkoajoka on suotuisa verrattuna muihin kuvattuihin biomarkkereihin. Ehkä parhaiten tutkittu esimerkki on munuaisvauriomolekyyli-1 (KIM-1), oletettu adheesiomolekyyli, joka osallistuu munuaisten regeneraatioon (43,44). Ikemia-reperfuusiovaurion rottamallissa KIM{6}}:n todettiin lisääntyneen 24–48 tuntia ensimmäisen loukkauksen jälkeen, mikä teki siitä luotettavan mutta hieman myöhäisen tubulussoluvaurion merkkiaineen. Viimeaikaiset tyylikkäät tutkimukset ovat osoittaneet, että KIM-1 voidaan havaita munuaisbiopsiasta ja virtsasta potilailla, joilla on iskeeminen akuutti tubulusnekroosi (45). Tämä havaitseminen dokumentoitiin kuitenkin potilailla, joilla on todettu iskeeminen munuaisvaurio, eikä virtsan KIM{11}}-mittauksen käyttökelpoisuutta varhaisen subkliinisen vaurion havaitsemiseksi ole toistaiseksi validoitu. Toisessa tuoreessa esimerkissä Cyr61:n havaittiin olevan erittyvä kysteiinirikas proteiini, joka on havaittavissa virtsasta 3-6 tuntia iskeemisen munuaisvaurion jälkeen (8). Tämä havaitseminen vaati kuitenkin bioafiniteettipuhdistusvaiheen hepariini-Sepharose-helmillä, ja jopa tällaisen puhdistuksen jälkeen havaittiin useita ristiin reagoivia peptidejä. Sitä vastoin tutkimuksemme osoittaa, että NGAL havaittiin helposti ja nopeasti suhteellisen puhtaina immunoreaktiivisina peptideinä Western blot -testeissä vain 1 litralla ensimmäisestä käsittelemättömästä virtsasta munuaisiskemian jälkeen sekä hiirillä että rotilla. Lisäksi virtsan NGAL oli ilmeinen jopa erittäin lievän "subkliinisen" munuaisiskemian jälkeen, huolimatta normaaleista seerumin kreatiniinitasoista. Lisäksi virtsan NGAL:n havaitseminen edelsi huomattavasti perinteisten merkkiaineiden, mukaan lukien 2- mikroglobuliinin ja NAG:n, ilmestymistä virtsaan.
Lopuksi on syytä huomata, että NGAL oli havaittavissa myös virtsasta varhain sisplatiinin annon jälkeen, jolloin muut morfologiset ja biokemialliset indikaattoritmunuaistenvahinkoaolivat poissa. Siten NGAL:n lisääntynyt säätely ja erittyminen virtsaan voi edustaa munuaisten tubulussolujen nopeaa vastetta erilaisiin loukkauksiin, ja NGAL:n havaitseminen virtsasta voi edustaa laajasti sovellettavaa ei-invasiivista kliinistä työkalua tubulussoluvaurion varhaiseen diagnosointiin.
Yhteenvetona tietomme osoittavat, että NGAL edustaa uutta, herkkää, ei-invasiivista virtsan biomarkkeria munuaisiskemialle. Tulevassa translaatiotyössä on tärkeää tutkia NGAL:n ilmentymistä virtsassa potilailla, joilla on lievä ja varhainen iskeeminen muoto.munuaistenvahinkoa. Toivotaan, että tällainen varhainen havaitseminen voi antaa kliinikoille mahdollisuuden aloittaa oikea-aikaiset interventiotoimet ARF:ssä, joka on edelleen huono ennuste, johon uusia hoitoja tarvitaan kipeästi. Lisäksi toivotaan, että näin nopea ja yksinkertainen virtsan NGAL:n havaitseminen potilailla, joilla on hienovarainen, subkliininen iskeeminenmunuaistenvahinkoa(esim. elämään liittyvät munuaisensiirrot, verisuonikirurgia, sydän- ja verisuonitapahtumat) tai subkliiniset munuaistoksiset vauriot (esim. varjoaineiden ja aminoglykosidien käyttö) varoittavat lääkäriä ryhtymään toimenpiteisiin, joilla pyritään estämään eteneminen selväksi ARF:ksi.
Kiitokset
Tätä työtä tuki National Institutes of Health / National Institute of Diabetes and Digestive and Kidney Diseases PD (DK53289, DK52612) ja JB (DK55388 ja DK58872) apurahoilla.

Cistanche tubulosavoi hoitaamunuaisvaurio
Viitteet
1. Thadani R, Pascual M, Bonventre JV: Akuutti munuaisten vajaatoiminta. N Engl J Med 334: 1448-1460, 1996
2. Star RA: Akuutin hoitoonmunuaistenepäonnistuminen. Kidney Int 54: 1817–1831, 1998
3. Liaño F, Pascual J: Ennustavat tekijät ja pisteytys. Teoksessa: Acute Renal Failure, toimittaja Molitoris BA ja Finn WF, Philadelphia, WB Saunders, 2001, s. 507–518
4. Molitoris BA: Siirtyminen hoitoon iskeemisessä akuutissa munuaisten vajaatoiminnassa. J Am Soc Nephrol 14: 265–267, 2003
5. Brady HR, Brenner BM, Clarkson MR, Lieberthal W: Akuutti munuaisten vajaatoiminta. Julkaisussa: The Kidney, 6. painos, toimittanut Brenner BM, Philadelphia, WB Saunders, 2000, s. 1201–1262
6. Sutton TA, Molitoris BA: Soluvaurion mekanismit iskeemisessä akuutissa munuaisten vajaatoiminnassa. Semin Nephrol 18: 490-497, 1998
7. Sheridan AM, Bonventre JV: Solubiologia ja vaurion molekyylimekanismit iskeemisessä akuutissamunuaistenepäonnistuminen. Curr Opin Nephrol Hypertens 9: 327-334, 2000
8. Muramatsu Y, Tsujie M, Kohda Y, Pham B, Perantoni AO, Zhao H, Jo SK, Yuen PST, Craig L, Hu X, Star RA: Kysteiinirikkaan proteiinin 61 (CYR61, CCN1) varhainen havaitseminen virtsasta munuaisten iskemia-reperfuusiovaurion jälkeen. Kidney Int 62: 1601–1610, 2002
9. Kurella M, Hsiao LL, Yishida T, Randall JD, Chow G, Sarang SS, Jensen RV, Gullans SR: Monimutkaisten biologisten prosessien DNA-mikrosiruanalyysi. J Am Soc Nephrol 12: 1072-1078, 2001
10. Yoshida T, Kurelia M, Beato F, Min H, Ingelfinger JR, Stears RL, Swinford RD, Gullans SR, Tang SS: Geeniekspression muutosten seuranta munuaisiskemia-reperfuusiossa rotalla. Kidney Int 61: 1646–1654, 2002
11. Supavekin S, Zhanh W, Kucherlapati R, Kaskel FJ, Moore LC, Devarajan P: Differentiaalinen geeniekspressio aikaisen munuaisiskemian/reperfuusion jälkeen. Kidney Int 63: 1714–1724, 2003
12. Nogae S, Miyazaki M, Kobayashi N, Saito T, Abe K, Saito H, Nakane PK, Nakanishi Y, Koji T: Apoptoosin induktio hiiren munuaisen iskemia-reperfuusiomallissa: Fasin mahdollinen osallistuminen. J Am Soc Nephrol 9: 620-631, 1998
13. Daemen MARC, Van de Ven MWCM, Heineman E, Buurman WA: Endogeenisen interleukiinin-10 ja tuumorinekroositekijän osallisuus munuaisiskemia-reperfuusiovauriossa. Transplantation 67: 792–800, 1999
14. Kelly KJ, Plotkin Z, Dagher PC: Guanosiinilisäys vähentää apoptoosia ja suojaamunuaisteniskeemisen vaurion taustalla. J Clin Invest 108: 1291–1298, 2001
15. Burne NJ, Rabb H: Fukosyylitransferaasien patofysiologiset vaikutukset munuaisiskemia-reperfuusiovauriossa. J Immunol 169: 2648-2652, 2002
16. Megyesi J, Safirstein RL, Price PM: p21WAF1/CIP/SD1:n induktio munuaistubulussoluissa vaikuttaa sisplatiinin aiheuttaman akuutinmunuaistenepäonnistuminen. J Clin Invest 101: 777–782, 1998
17. Shiraishi F, Curtis LM, Truong L, Poss K, Visner GA, Madsen K, Nick HS, Agarwal A: Heme-oksygenaasi-1-geenin ablaatio tai ilmentyminen moduloi sisplatiinin aiheuttamaa munuaistiehyiden apoptoosia. Am J Physiol 278: F726-F736, 2000
18. Ramesh G, Reeves WB: TNF- välittää kemokiinien ja sytokiinien ilmentymistä jamunuaistenvahinkoasisplatiinin munuaistoksisuus. J Clin Invest 110: 835-842, 2002
19. Feldenberg LR, Thevananther S, del Rio M, De Leon M, Devarajan P: Osittainen ATP:n ehtyminen indusoi Fas- ja kaspaasivälitteisen apoptoosin MDCK-soluissa. Am J Physiol 276: F837-F846, 1999
20. Devarajan P, De Leon M, Talasazan F, Schoenfeld AR, Davidowitz EJ, Burk RD: Von Hippel-Lindau -geenituote estää munuaissolujen apoptoosia Bcl-2--riippuvaisten reittien kautta. J Biol Chem 276: 40599-40605, 2001
21. Yang J, Goetz D, Li JY, Wand W, Mori K, Setlik D, Du T, ErdjumentBromage H, Tempst P, Strong R, Barasch J: Lipokaliinin välittämä raudan toimitusreitti. Mol Cell 10: 1045-1056, 2002
22. Molitoris BA, Weinberg JM, Venkatachalam MA, Zager RA, Nath KA, Goligorsky MS: Akuutti munuaisten vajaatoiminta II. Akuutin munuaisten vajaatoiminnan kokeelliset mallit: epätäydellinen mutta välttämätön. Am J Physiol 278: F1–F12, 2000
23. Flower DR, North AC, Sansom CE: Lipokaliiniproteiiniperhe: rakenne- ja sekvenssikatsaus. Biochim Biophys Acta 1482: 9–24, 2000
24. Kjeldsen L, Cowland JB, Borregaard N: Ihmisen neutrofiiligelatinaaseihin liittyvä lipokaliini ja homologiset proteiinit rotassa ja hiiressä. Biochim Biophys Acta 1482: 272–283, 2000
25. Xu S, Venge P: Lipokaliinit sairauden biokemiallisina merkkiaineina. Biochim Biophys Acta 1482: 298–307, 2000
26. Hraba-Renevey S, Turler H, Kress M, Salomon C, Weil R: SV40-hiiren geenin 24p3:n indusoima ilmentyminen sisältää transkription jälkeisen mekanismin. Oncogene 4: 601-608, 1989
27. Cowland JB, Borregaard N: Ihmisistä peräisin olevan neutrofiiligelatinaaseihin liittyvän lipokaliinin geenin molekyylien karakterisointi ja kudosilmentymisen malli. Genomics 45: 17-23, 1997
28. Nielson BS, Borregaard N, Bundgaard JR, Timshel S, Sehested M, Kjeldsen L: NGAL-synteesin induktio ihmisen kolorektaalisen neoplasian ja tulehduksellisten suolistosairauksien epiteelisoluissa. Gut 38: 414-420, 1996
29. Xu SY, Pauksen K, Venge P: Ihmisen neutrofiililipokaliinin (HNL) seerumimittaukset tekevät eron akuuttien bakteeri- ja virusinfektioiden välillä. Scand J Clin Lab Invest 55: 125–131, 1995
30. Keatings VM, Barnes PJ: Granulosyyttiaktivaatiomarkkerit indusoidussa ysköksessä verrattuna krooniseen obstruktiiviseen keuhkosairauteen, astmaan ja normaaleihin koehenkilöihin. Am J Respir Crit Care Med 155: 449–453, 1997
31. Betsuyaky T, Nishimura M, Takeyabu K, Tanino M, Venge P, Xu S, Kawakami Y: Neutrofiilien jyväproteiinit bronkoalveolaarisessa huuhtelunesteessä potilailta, joilla on subkliininen emfyseema. Am J Respir Crit Care Med 159: 1985–1991, 1999
32. Carlson M, Raab Y, Severus L, Xu S, Hallgren R, Venge P: Ihmisen neutrofiililipokaliini on ainutlaatuinen neutrofiilitulehduksen merkkiaine haavaisessa paksusuolitulehduksessa ja proktiitissa. Gut 50: 501–506, 2002
33. Chiao H, Kohda Y, McLeroy P, Craig L, Housing I, Star RA: -Melanosyyttejä stimuloiva hormoni suojaamunuaistenvahinkoaiskemian jälkeen hiirillä ja rotilla. J Clin Invest 99: 1165-1172, 1997
34. Rabb H, Ramirez G, Saba SR, Reynolds D, Xu J, Flavell R, Antonia S: Munuaisten iskeeminen reperfuusiovaurio L-selektiinipuutteisilla hiirillä. Am J Physiol 271: F408-F13, 1996
35. Rabb H, Star R: Tulehdusvaste ja sen seuraukset akuutissamunuaistenepäonnistuminen. Teoksessa: Acute Renal Failure, toimittaja Molitoris BA ja Finn WF, Philadelphia, WB Saunders, 2001, s. 89–100
36. Devireddy LR, Teodoro JG, Richard FA, Green MR: Apoptoosin induktio eritetyllä lipokaliinilla, jota transkriptionaalisesti säätelee IL-3-deprivaatio. Science 293: 829–834, 2001
37. Persengiev SP, Devireddy LR, Green MR: ATFx:n apoptoosin esto: Uusi rooli nisäkkään bZIP-transkriptiotekijöiden ATF/CREB-perheen jäsenelle. Genes Dev 16: 1806–1814, 2002
38. Ryon J, Bendickson L, Nilsen-Hamilton M: Uterokaliinin/24p3:n, lipokaliinin ja akuutin vaiheen proteiinin korkea ekspressio involutioning lisääntymiskudoksissa. Biochem J 367: 271-277, 2002
39. Poistettu todisteesta.
40. Kamarainen M, Seppala M, Virtanen I, Andersson LC: Glykodeliinin ilmentyminen MCF-7-rintasyöpäsoluissa indusoi erilaistumista organisoituneeksi akinaariseksi epiteeliksi. Lab Invest 77: 565–573, 1997
41. Witzgall R, Brown D, Schwarz C, Bonventre JV: Proliferoivan solun ydinantigeenin, vimentiinin, c-fos:n ja klusteriinin lokalisointi postskeemisessa munuaisessa: todisteita heterogeenisestä geneettisestä vasteesta nefronisegmenttien välillä ja suuri joukko mitoottisia aktiiviset ja erilaistumattomat solut. J Clin Invest 93: 2175–2188, 1994
42. Hammerman MR: Fylogenian yhteenveto ontogenian avulla nefrologiassa. Kidney Int 57: 742–755, 2000
43. Ichimura T, Bonventre JV, Bailly V, Wei H, Hession CA, Cate RL, Sanicola M: Munuaisvauriomolekyyli-1 (KIM-1), oletettu epiteelisolujen adheesiomolekyyli, joka sisältää uuden immunoglobuliinin domeenia, on ylössäädelty munuaissoluissa vaurion jälkeen. J Biol Chem 271: 4135-4142, 1998
44. Bailly V, Zhang Z, Meier W, Cate R, Sanicola M, Bonventre JV: Munuaisvauriomolekyylin irtoaminen-1, oletettu adheesioproteiini, joka osallistuu munuaisten regeneraatioon. J Biol Chem 277: 39739-39748, 2002
45. Han WK, Bailly V, Abichandani R, Thadani R, Bonventre JV: Munuaisvauriomolekyyli-1 (KIM-1): Uusi biomarkkeri ihmisen munuaisten proksimaalisen tubuluksen vauriolle. Kidney Int 62: 237–244, 2002
