Perfluorooktaanihapon vaikutukset suoliston mikrobiotaan ja mikrobien aineenvaihduntaan C57BL/6J-hiirissäⅢ
Nov 28, 2023
3. Tulokset
3.1. PFOAMuutti suolen mikrobiston koostumusta
Tutkimuksessamme havaittiin yhteensä 78 bakteerisukua, kuten 16S rRNA-sekvensointi paljasti. Yleisimmät suvut on esitetty kuvassa 1A. LEfSe-analyysi osoitti, että viisi bakteerisukua rikastui PFOA-käsitellyissä hiirissä, nimittäin Alistipes, LachnospiraceaeUCG 004, Clostridiales, Clostridium ASF356 ja Incertae sedis (kuva 1B). Sillä välin kuusi bakteerisuvua väheni PFOA-käsitellyssä ryhmässä, nimittäin Tyzzerella, Eubacteriumcoprostanoligenes, Intestinimonas, Clostridium septum, Roseburia ja Turicibacter (kuva 1B).

3.2. Suoliston mikrobiston ja ulosteen aineenvaihduntatuotteiden välinen korrelaatio
Suoritimme integroivan analyysin suoliston mikrobiotosta ja ulosteen metaboliitteista MixOmicsilla. Suoliston mikrobiotan ja ulosteen metaboliittien välinen yleinen korrelaatio oli 0,74 (kuva 2A). Sekä ulosteen metaboliittien että bakteerisukujen osalta PFOA-käsitelty ryhmä erotettiin kontrolliryhmästä (kuva 2B, täydentävä kuva S1). Yhteys ulosteen metaboliittien ja bakteerisukujen välillä on esitetty kuvassa 2C. Kolme bakteerisukua osoitti korrelaatioita kahdeksan ulosteen metaboliitin kanssa (kuva 2D).

3.3. PFOA:n aiheuttamat muutokset ulosteen aineenvaihdunnassa
PFOA-altistuksen jälkeen yhteensä 12 0 metaboliittia osoitti p-arvon < 0,05, joista viidellä metaboliitilla oli väärä havaitsemisprosentti (FDR) < 0,05 (kuva 3A). Merkittävien metaboliittien hierarkkinen klusteri on esitetty kuvassa 3B. Reitin rikastusanalyysi paljasti, että PFOA-altistus muutti kysteiinin ja metioniinin metaboliaa (kuva 3C). Erityisesti kolme ulosteen sappihappoa vähentyivät merkittävästi PFOA-altistumisesta, nimittäin glykodeoksikoolihappo, beeta-hyodeoksikoolihappo ja gamma-murikolihappo (kuva 3D).

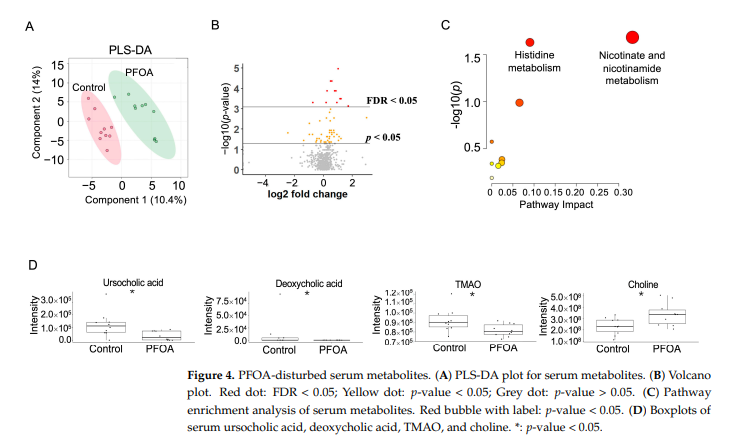
3.4. PFOA:n aiheuttamat muutokset seerumin aineenvaihdunnassa
PFOA:lla käsitelty ryhmä ja kontrolliryhmä erottuivat hyvin PLS-DA-käyrässä (kuvio 4A). Yhteensä 59 seerumin metaboliitin p-arvo oli < 0.05, joista 10 metaboliitin FDR oli < 0,05 (kuvio 4B). Reitin rikastusanalyysi paljasti, että PFOA-altistus muutti nikotiini- ja nikotiiniamidiaineenvaihduntaa ja histidiinimetaboliaa (kuvio 4C). Kaksi sappihappoa, taurokolihappo ja deoksikoolihappo, vähenivät merkittävästi PFOA:lla hoidetussa ryhmässä, linjassa TMAO:n laskun ja PFOA-altistuksen aiheuttaman koliinin lisääntymisen kanssa (kuva 4D).

3.5. PFOA:n aiheuttamat muutokset maksan metaboliitteissa
Maksan metaboliittien PLS-DA-analyysi osoitti, että PFOA:lla käsitelty ryhmä erotettiin kontrolliryhmästä (kuvio 5A). Yhteensä 94 maksan metaboliittia osoitti p-arvoja < 0,05 PFOA-altistuksen jälkeen (kuva 5B). Reitin rikastusanalyysi osoitti, että arginiinibiosynteesi muuttui merkittävästi (kuvio 5C). Kolmen metaboliitin havaittiin olevan merkittäviä maksassa, seerumissa ja ulosteessa, nimittäin 1-(1Z-heksadekyyli)-sn-glysero-3-fosfokoliini, dekanoyyli-L-karnitiini ja 1- heksadekyyli-sn-glysero-3-fosfokoliini (kuva 5D). PFOA-altistuminen vähensi kahta sappihappoa, tauroursodeoksikoolihappoa ja taurokenodeoksikoolihappoa, samoin kuin kahden tryptofaanimetaboliitin, 3-indoliakryylihapon ja 3-indolietikkahapon, määrä väheni ja tauriinin määrä lisääntyi (kuva 5E).

4. Keskustelu
Hiili-fluori-sidos tekee PFOA:sta vastustuskykyisen fotolyysille ja hydrolyysille, mikä johtaa PFOA:n pysymiseen ympäristössä. Plasman PFAS-pitoisuuksien ja makean veden kalojen, merikalojen, rapujen ja katkarapujen ravinnonsaannin välillä havaittiin positiivinen korrelaatio 933 lisääntymisikäisellä naisella Shanghaissa, Kiinassa [32]. Varhainen altistuminen PFOA:lle on keskeinen tekijä lasten seerumipitoisuuksissa [33]. Tutkimuksessa, jossa tutkittiin PFAS:n ja kroonisen tulehduksen sekä oksidatiivisen stressin välistä suhdetta National Health and Nutrition Examination Surveyssa (NHANES) vuosina 2005–2012 (n=6652), PFOA:n prosentuaalinen muutos liittyi merkittävästi lymfosyyttien prosenttiosuuteen. määrät, seerumin rauta ja seerumin kokonaisbilirubiini [34]. Munuais- ja kivessyöpäriski kasvaa 10 ng/ml nousua kohti seerumin PFOA-pitoisuudessa [35].
Lisäksi seerumin PFOA-pitoisuus liittyi positiivisesti maksasoluvauriomarkkerin alaniiniaminotransferaasiin (ALT) 47 092 aikuisella C8 Health Projectissa [36]. Seerumin PFOA liittyi myös positiivisesti immunoglobuliiniin, antisyklisiin sitrullinoituihin peptidivasta-aineisiin ja reumatekijöihin [37]. Vakavana ja laajalle levinneenä ympäristöongelmana on raportoitu PFOA:n aiheuttamia metabolisia muutoksia ihmisen ääreisveren lymfosyyteissä [38] ja lapset, joilla on lääkärin diagnosoima alkoholiton rasvamaksatauti (NAFLD) [39].
Integratiivista analyysiä PFOA-altistuksen aiheuttamasta metabolomin ja suoliston mikrobiotan häiriöistä ei kuitenkaan ole tehty. Tässä tutkimuksessa emme ainoastaan paljastaneet seerumin metaboliitteissa tapahtuvia muutoksia, vaan myös metabolisia muutoksia ulosteessa ja maksassa. Lisäksi suoritimme integroivan analyysin ulosteen metaboliitteista ja suoliston mikrobiotosta ja paljastimme niiden välisen yhteyden PFOA-altistuksen vaikutuksesta. PFOA-altistus häiritsi sekä ulosteen metaboliittien että suoliston mikrobiston profiileja.

PFOA-altistus vähensi Roseburian, Tyzzerellan, Eubacterium coprostanoligenesin ja Intestinimonasin suhteellista runsautta. Roseburiaa pidetään kommensaalina bakteerina, jolla on anti-inflammatorisia ominaisuuksia ja joka voi palauttaa hyödyllisiä suoliston mikro-organismeja [40].
Roseburia intestinalis voi ylläpitää energiahomeostaasia ja ehkäistä suoliston tulehdusta [41]. Tyzzerellaa havaittiin alemmilla tasoilla potilailla, joilla oli akuutti sydäninfarkti ja sairaalapotilailla, joilla oli ruokatorven syöpä [42,43]. Mozzarellan on raportoitu liittyvän rasvahappojen saantiin ravinnosta [44]. Tyzzerellan kasvua esti brownien ja runsassokerisen ruokavalion yhdistelmälisäys [45]. E. coprostanoligenes korreloi diasyyliglyserolien tason kanssa [46]. E. coprostanoligenesin väheneminen liittyi käänteisesti seerumin aspartaattitransferaasin (AST) ja ALT:n tasoihin runsasrasvaisella ruokavaliolla ruokituilla hiirillä [47].
Intestinimonas spp. on havaittu lysiinillä rikastetuissa ulosteen laimennoksissa, ja intestinimonasin kaltaiset bakteerit tunnetaan butyraatin tuottajina, jotka hyödyntävät lysiiniä ja Nεfruktosyllysiiniä korvikkeilla ja aikuisilla [48]. Näiden mikro-organismien väheneminen saattaa vaikuttaa isännän immuunivasteeseen ja metaboliseen aktiivisuuteen. Alistipes-, Clostridium ASF 356-, Clostridiales- ja LachnospiraceaeUCG 004 -bakteerien suhteellinen runsaus rikastui merkittävästi PFOA-altistuminen. Alistipes on ehdollinen patogeeninen bakteeri, ja sitä lisääntyivät runsasrasvaiset ja sakkaroosipitoiset ruokavaliot [49].
Alistipesiä pidettiin suoliston mikrobiotan markkerina, joka jaettiin lihavilla potilailla, joilla oli erilaisia aineenvaihduntahäiriöitä [50]. Suurempi Alistipesin määrä havaittiin potilailla, joilla oli erilaisia aivoihin liittyviä sairauksia, mukaan lukien Alzheimerin tauti, tarkkaavaisuus-hyperaktiivisuushäiriö, skitsofrenia, autismikirjon häiriö, vakava masennushäiriö, Parkinsonin tauti ja kaksisuuntainen mielialahäiriö [51]. Lisäksi Alistipes eristettiin potilaista, joilla oli vatsan ja peräsuolen paiseita, ja se yhdistettiin masennukseen ja paksusuolensyöpään [52]. Sappia sietävänä mikro-organismina Alistipesin runsautta voitaisiin lisätä eläinperäisellä ruokavaliolla [53].
Alistipesin rikastuminen johtui myös kastalagiinin ravinnosta, joka on aktiivinen yhdiste polyfenolirikkaissa marjoissa camu-camu [54]. In vitro -tutkimus ehdotti, että Clostridium ASF 356 kulutti disoleusiinia, valiinia, alaniinia, treoniinia, laktaattia ja muita metaboliitteja, ja se osallistui myös ristiruokinnassa. Jotkut Clostridiumin lajit, kuten C. difficile, ovat patogeenisiä.PFOA-altistus häiritsi sappihappoaineenvaihduntaa tässä tutkimuksessa. Sappihapot syntetisoidaan maksassa kolesterolista ja varastoituvat sappirakkoon, ja ne vapautuvat suolistossa aterian seurauksena ja kulkevat sitten enterohepaattisen verenkierron läpi.
Ennen erittymistä primaariset sappihapot konjugoidaan tyypillisesti tauriiniin ja glysiiniin. Primaariset sappihapot, koolihappo ja kenodeoksikoolihappo voidaan muuntaa sekundäärisiksi sappihapoiksi sappihapon dekonjugaation ja 7-alfa-hydroksylaation avulla. Suoliston mikrobitakaani säätelee sappihapon aineenvaihduntaa alentamalla tauro- -murikolihappotasoja, joka on tumareseptorin farnesoidi-X-reseptorin (FXR) antagonisti [55]. Sappihappojen synteesi on negatiivisen palautekontrollin alaisena maksassa ja sykkyräsuolessa FXR-aktivaation kautta [55]. Yhteys seerumin sappihappojen ja sekä seerumin PFOA:n että sikiön kasvun päätepisteiden välillä havaittiin 313 raskaana olevan afroamerikkalaisen naisen kohortissa [56].

C57BL/6J-hiirillä havaittiin lisääntynyttä verenkierrossa olevaa sappihappoa, joka johtuu viiden PFAS:n seoksesta, jotka koostuivat PFOA:sta, PFOS:sta, PFNA:sta, PFHxS:stä ja GenX:stä [57]. Ikään liittyvää vuotavaa suolitulehdusta voitaisiin lievittää probioottisten cocktailien lisäyksellä lisäämällä sappisuolan hydrolaasin aktiivisuutta, mikä johtaa tauriinin lisääntymiseen, mikä stimuloi tiiviitä liitoksia [58]. Dysbioosin aiheuttama sekundääristen sappihappojen puute voi edistää suoliston tulehdusta, joka voi olla helpottaa täydentämällä sekundaarisia sappihappoja hiirimalleissa [59].
PFOA:n aiheuttaman sappihappometaboliaan liittyvän geeniekspression heikkeneminen raportoitiin ihmisen HepaRG-hepatoomasoluissa. Erityisesti CYP7A1, avainentsyymi, joka katalysoi sappihapposynteesin nopeutta rajoittavaa vaihetta, väheni [60].
Sappihappobiosynteesiin osallistuvien entsyymien lisäksi PFOA alensi myös sappihapon kuljetukseen liittyvien geenien, Bsep:n ja Mrp2:n, ilmentymistasoja 3D-hiiren primaarisessa maksasferoidimallissa [61]. Lisäksi PFOA:n on raportoitu olevan vuorovaikutuksessa ihmisen sappihappoa kuljettavan Na+/taurokolaattia kuljettavan polypeptidin kanssa [62]. PFOA vähensi niiden RNA- ja proteiiniekspressiota orgaanisten anionien kuljettavien polypeptidien 1a1, 1a4 ja 1b2 avulla hiirimallissa aktivoimalla peroksisomiproliferaattori-aktivoitua reseptoria (PPAR) alfa; nämä ovat tärkeimpiä kuljettajia, jotka ovat vastuussa sappihappojen imeytymisestä maksaan [63].
Tryptofaanin aineenvaihdunnan muutokset olivat eniten raportoitu PFAS:iin liittyvä metabolinen tunnus ihmistutkimuksissa [64]. Suoliston mikrobit voivat muuttaa tryptofaanin indoliksi ja sen johdannaisiksi, kuten 3-indoliakryylihapoksi ja 3-indolietikkahapoksi, joiden tasoa alensi PFOA-altistus tässä tutkimuksessa. Erityisesti 3-indolietikkahapon on raportoitu edistävän suoliston epiteelin estetoimintoa ja tukahduttavan tulehdusvasteita [65]. Musiineja hyödyntävien ja tryptofaania metaboloivien suoliston mikro-organismien geneettinen kapasiteetti on heikentynyt potilailla, joilla on tulehduksellinen suolistosairaus [65].
Sytoplastisreseptorina AhR on tärkeä tekijä kudosten homeostaasissa ja immuniteetissa, mikä mahdollistaa immuunisolujen sopeutumisen ympäristöolosuhteisiin [66]. Lisäksi 3-indolietikkahapon raportoitiin yhdeksi AhR:n hallitsevista aktivaattoreista ihmisen osallistujien hiiri- ja ulostenäytteissä [67]. Lisäksi 3-indolietikkahappo voi edistää suoliston esteen eheyttä ja tukahduttaa tulehdusvasteita aktivoimalla AhR-transkriptiotekijää, mikä edelleen edisti AhR-riippuvaista IL-22-transkriptiota [68]; 3-indolietikkahappo on myös pregnane X -reseptorin (PXR) aktivaattori, joka indusoi IL-35+ B-solujen muodostumista yhdessä lipopolysakkaridin kanssa PXRand Toll -reseptorin 4 kautta [69]. Lisäksi 3-indolietikkahapolla on hyödyllisiä vaikutuksia, kuten selkärankareumaa lievittävä [70]; 3-indolietikkahappo väheni merkittävästi hiirillä, joita ruokittiin runsasrasvaisella ruokavaliolla [71].
3-indolietikkahapon täydentäminen voisi lievittää alkoholin aiheuttamaa rasvamaksasairauksia heikentämällä tulehdusvastetta, oksidatiivista stressiä ja maksan lipogeneesiä [72]. Lisäksi 3-indolietikkahappo vaikutti kemoterapian tehokkuuteen haimasyöpäpotilailla kahdessa riippumattomassa haimajohdon adenokarsinoomakohortissa [73]. Haiman duktaalisen adenokarsinooman hiirimallissa ulosteen mikrobiotan siirto ja 3-indolietikkahapon lisäys voivat myös parantaa kemoterapeuttista tehoa humanisoiduilla gnotobioottisilla hiirillä [73]. Kanssa3-indoliakryylihapon ja 3-indolietikkahapon vähentäminen PFOA:lla, nämä hyödylliset vaikutukset saattavat vaarantua.
Tällä tutkimuksella oli useita rajoituksia. Ensinnäkin tämä tutkimus sisälsi vain uroshiiriä, kun taas naarashiiriä ei otettu mukaan. Sukupuolittain tasapainotettu tutkimussuunnitelma, joka sisältää sekä uros- että naarashiiriä, voisi parantaa tätä tutkimusaluetta. Toiseksi, PFOA-tasoa juomavedestä, jonka kontrollihiiret saivat, ei havaittu. Kun otetaan huomioon PFOA:n laaja levinneisyys, oli todennäköistä, että kontrollihiiren saama juomavesi sisälsi vähän PFOA:ta. Juomaveden PFOA-tason ilmoitettiin olevan 20-70 ng/l Georgiassa, Yhdysvalloissa [74]. PFOA:n myrkyllisen vaikutuksen testaamiseksi suoliston mikrobiotaan liittyviin metaboliitteihin altistustasoksi asetettiin tässä tutkimuksessa 1 ppm, mikä on korkeampi kuin ympäristön kannalta merkityksellinen taso. Annosta on alennettava tulevissa tutkimuksissa PFOA:n terveysvaikutusten selvittämiseksi ympäristön kannalta merkityksellisillä tasoilla.
5. Johtopäätökset
PFOA:sta on tullut vakava kansanterveysongelma viime aikoina. Tässä tutkimuksessa PFOA häiritsi sekä suoliston mikrobiston koostumusta että ulosteiden, seerumin ja maksan metabolisia profiileja hiirillä. Suoliston mikrobiston ja erilaisten ulosteen metaboliittien välillä havaittiin korrelaatio. PFOA-altistus aiheutti merkittäviä muutoksia suoliston mikrobiotaan liittyvissä metaboliiteissa, mukaan lukien sappihapot ja tryptofaanimetaboliitit, kuten 3-indoliakryylihappo ja 3-indolietikkahappo. Löytömme voisivat parantaa ymmärrystä suoliston mikrobiotan välittämän PFOA:n terveysvaikutuksista.
Luonnollinen kasviperäinen lääke ummetuksen lievitykseen-Cistanche
Cistanche on loiskasvien suku, joka kuuluu Orobanchaceae-heimoon. Nämä kasvit tunnetaan lääkeominaisuuksistaan, ja niitä on käytetty perinteisessä kiinalaisessa lääketieteessä (TCM) vuosisatojen ajan. Cistanche-lajeja esiintyy pääasiassa kuivilla ja aavikkoalueilla Kiinassa, Mongoliassa ja muissa Keski-Aasian osissa. Cistanche-kasveille on tunnusomaista niiden mehevät, kellertävät varret, ja niitä arvostetaan suuresti niiden mahdollisten terveyshyötyjen vuoksi. TCM:ssä Cistanchella uskotaan olevan tonisoivia ominaisuuksia, ja sitä käytetään yleisesti munuaisten ravitsemiseen, elinvoiman lisäämiseen ja seksuaalisen toiminnan tukemiseen. Sitä käytetään myös ikääntymiseen, väsymykseen ja yleiseen hyvinvointiin liittyvien ongelmien ratkaisemiseen. Vaikka Cistanchella on pitkä käyttöhistoria perinteisessä lääketieteessä, sen tehoa ja turvallisuutta koskeva tieteellinen tutkimus on jatkuvaa ja rajallista. Sen tiedetään kuitenkin sisältävän erilaisia bioaktiivisia yhdisteitä, kuten fenyylietanoidiglykosideja, iridoideja, lignaaneja ja polysakkarideja, jotka voivat myötävaikuttaa sen lääkevaikutuksiin.

Wecistanchencistanche-jauhe, cistanche-tabletit, cistanche-kapselitja muita tuotteita kehitetään käyttämälläaavikkocistancheraaka-aineina, joilla kaikilla on hyvä vaikutus ummetusta lievittämään. Erityinen mekanismi on seuraava: Cistanchen uskotaan olevan potentiaalisia etuja ummetuksen lievittämisessä sen perinteisen käytön ja tiettyjen sen sisältämien yhdisteiden perusteella. Vaikka tieteellinen tutkimus erityisesti Cistanchen vaikutuksesta ummetukseen on rajallista, sillä uskotaan olevan useita mekanismeja, jotka voivat edistää sen potentiaalia lievittää ummetusta. Laksatiivinen vaikutus:CistancheSitä on pitkään käytetty perinteisessä kiinalaisessa lääketieteessä ummetuksen lääkkeenä. Sillä uskotaan olevan lievä laksatiivinen vaikutus, joka voi auttaa edistämään suoliston liikkeitä ja aiheuttamaan ummetusta. Tämä vaikutus voidaan johtua useista Cistanchen yhdisteistä, kuten fenyylietanoidiglykosideista ja polysakkarideista. Suoliston kosteuttaminen: Perinteisen käytön perusteella Cistanchella katsotaan olevan kosteuttavia ominaisuuksia, jotka kohdistuvat erityisesti suolistoon. Suoliston kosteutuksen ja voitelun edistäminen voi auttaa pehmentämään työkaluja ja helpottamaan kulkua, mikä lievittää ummetusta. Tulehdusta ehkäisevä vaikutus: Ummetus voi joskus liittyä ruoansulatuskanavan tulehdukseen. Cistanche sisältää tiettyjä yhdisteitä, mukaan lukien fenyylietanoidiglykosideja ja lignaaneja, joilla uskotaan olevan anti-inflammatorisia ominaisuuksia. Vähentämällä suoliston tulehdusta se voi auttaa parantamaan suoliston säännöllisyyttä ja lievittämään ummetusta.
