Luku 2: Inflammasomien rooli glomerulonefriitissä
Jun 08, 2022
Lisätietoja: ottaa yhteyttätina.xiang@wecistanche.com
7. Tulehduksellinen osallistuminen autoimmuunimunuaissairauksiin
Yhteenveto tärkeimmistä aiheeseen liittyvistä julkaisuistatulehduksellinenGlomerulonefriitin tutkimukset on esitetty taulukossa 1.

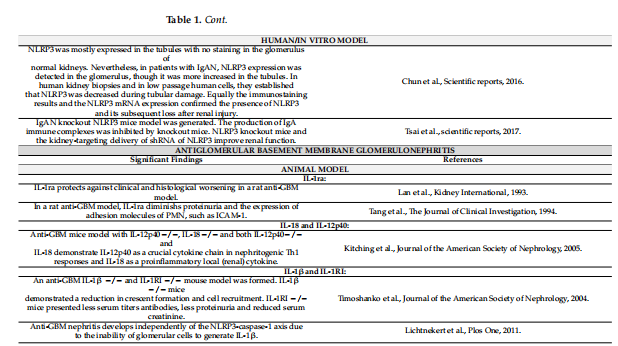
LDG, matalatiheyksiset granulosyytit; NET:t, neutrofiilien ekstrasellulaariset ansat; dsDNA, anti-kaksoisjuosteinen DNA; SLE, systeeminen lupus erythematosus; LN, lupus-nefriitti; NFkB, ydintekijä kappa B; TNF-c, tuumorinekroositekijä; siRNA, pieni häiritsevä RNA; INF, interferoni; HMGB1, korkean liikkuvuuden ryhmän laatikko 1 proteiini; LPS, lipopolysakkaridi; ATP, adenosiinitrifosfaatti; CASP1, kaspaasi-1; ANCA, anti-neutrofiilinen sytoplasminen autovasta-aine; NE, neutrofiilien elastaasi; PR3, proteinaasi 3; MPO, myeloperoksidaasi; NCGN, nekrotisoiva puolikuun muotoinen glomerulonefriitti; Phox, NADPH-oksidaasi; PR3, proteinaasi 3; IgAN, IgA-nefropatia; mRNA, lähetti-RNA; shRNA, lyhyt hiusneula-RNA; Il-1ra, interleukiini-1-reseptorin antagonisti; anti-GBM, anti-glomerulaarinen tyvikalvo; PMN, polymorfonukleaarinen; ICAM-1, solujen välinen adheesiomolekyyli-1; IL-1RI, IL1-tyypin 1 reseptori.
Napsauta tätä saadaksesi tietää cistanchesta, mistä ostaa
7.1.Lupus-nefriitti
SLE on krooninen sairaus, joka vaikuttaa useinmunuainen. Lupus nefriitti (LN) on yleisinmunuaissairaus, johon osallistuu noin 50 prosenttia SLE-potilaista. Tämäautoimmuuni sairausvaikuttaa enimmäkseen lisääntymisiässä oleviin naisiin. Miehillä häiriö voi olla aggressiivisempi. Potilailla on LN yleensä varhaisessa iässä, ja se ilmenee yleensä taudin alkuvaiheessa. Potilaiden, joilla on tämä munuaisten vajaatoiminta, kuolleisuus on lisääntynyt. Yhteensä 10-30 prosenttia LN-potilaista etenee munuaisten vajaatoimintaan, joka vaatii munuaiskorvaushoitoa.
Epäsäännöllisyydet synnynnäisessä ja adaptiivisessa immuniteetissa edistävät SLE:n patogeneesiä. LN esiintyy, kun neutrofiileihin liittyvien geenien transkriptio lisääntyy. IFN:n nousu edeltää neutrofiilien aktivoitumista. IFN:n lisääntyminen aiheuttaa B-solujen erilaistumisen plasmablasteiksi ja tuottaatulehdustiettyjen kudosten neutrofiilien ja aktiivisten myeloidisolujen kautta. Kun nämä neutrofiilit kuolevat, solunulkoiset neutrofiililoukut (NET) ilmestyvät. NETit ovat ristikkokromatiinikuituja, jotka on yhdistetty antimikrobisista peptideistä ja entsyymeistä johdettujen rakeiden kanssa, joilla on tärkeä puolustusrooli [74]. Nämä verkot auttavat ylläpitämään antigeenispesifistä autovasta-ainetuotantoa.
Munakeräsissä kerrostuneiden immuunikompleksien muodostuminen johtuu vasta-aineiden tuotannosta ydin- ja soluantigeeneja vastaan. Immuunikompleksit voivat aktivoida komplementin ja aiheuttaa munuaisvaurioita, erityisesti vaihtoehtoisen reitin kautta. B- ja T-solujen tuottamat plasman interstitiaaliset solut aggregoituvat munuaisten tubulointerstitiumissa ja synnyttävät myös autovasta-aineiden tuotantoa [73].
Inflammasomin komponenttien lisääntyminen havaittiin biopsiasta potilailta, joilla oli LN PICARD(ASC), kaspaasi-1 ja IL-18, mikä osoitti heidän panoksensa sairauteen 75]. Lisäksi IL-18:n lisääntynyt transkriptio tubulointerstitiaalisissa ja glomerulaarisissa osastoissa korreloi LN:n vaikeusasteen ja proteinurian alkamisen kanssa.
7.1.1. In vitro -malli
Inflammasomin aktivoituminen synnynnäisen immuniteetin soluissa voi laukaista tai vahvistaa autoimmuunivasteen. Tulehdukselliselle ärsykkeelle, kuten LPS:lle, altistumisen jälkeen eristetyt tuoreet monosyytit lisäävät tulehduksen aktivoitumista, jolle on ominaista kaspaasin-1, IL-1 ja IL-18 nousu. In vitro -viljelmiin lisätty kaspaasi-1-estäjä vähentää IL-18-tuotantoa.
Kuten aiemmin mainittiin, NEToosi-mekanismi myötävaikuttaa neutrofiilien kuolemaan SLE-potilailla. Tutkijaryhmiltä saadut todisteet viittaavat siihen, että SLE-potilaille on ominaista NET:ien kehittymisen ja poistumisen välinen epätasapaino, mikä aiheuttaa kudosvaurioita. Erityisesti matalatiheyksiset proinflammatoriset granulosyytit, joita esiintyy SLE-potilaiden verenkierrossa, mahdollistavat paljon suuremman kapasiteetin tuottaa NET-soluja[79].
Kahlenbertg ja hänen työtoverinsa [80] osoittivat ensinnäkin, että NET:t ovat osittain tulehduksen aktivoijia LL-37:n ulkoistumisen kautta. NETit ulkoistavat erilaisia antimikrobisia peptidejä. Tarkemmin sanottuna katelisidiini LL-37 on muun muassa neutrofiilien, monosyyttien ja makrofagien syntetisoima peptidi, jolla on aktiivisuutta useita patogeenejä vastaan. LL-37-ulkoistuminen NET:issä on tunnistettu SLE-potilaiden neutrofiileistä [79]. Tässä tutkimuksessa [80] kirjoittajat puhdistivat ja eristivät ihmisen ja hiiren makrofageja. Tulokset osoittivat, että LL-37 aktivoi NLRP3-tulehduksen makrofageissa ja että SLE-potilaat aktivoivat tulehduksen todennäköisemmin vasteena LL-37:lle ja NET:ille verrattuna vertailupotilaiden makrofagiin. Tämä stimulaatio pitää yllä IL-1- ja IL-18-arvojen lisääntymistä, mikä puolestaan edistää NEToosia, mikä johtaa taudin pahenemiseen tai elinvaurioihin, pääasiassa munuaisiin, ihoon ja aivoihin. Lisäksi heidän tietonsa viittaavat siihen, että NLRP3-tulehdusta tarvitaan LL-37:n kaspaasi-1-aktivointiin.
7.1.2. Eläinmalli
On huomionarvoista mainita, että erilaisissa hiiren tutkimuksissa NLRP3 on yhdistetty LN: hen. Kahlenberg et ai. [81], tutki kaspaasin -1 roolia hiiren lupuksen induktiossa. Villityypin hiirimallit altistettiin pristanin kehittämille lupukseen liittyville autovasta-aineille ja aktiiviselle vasteelle INF-tyypin INF:lle. Pristane-altistuksen jälkeen kaspaasi-1 -/- hiirillä ei ollut kohonneita IL-1- tai IL-tasoja -18, mikä viittaa siihen, että kaspaasilla-1 oli rooli näiden sytokiinien transkriptiossa. Lisäksi kaspaasi-1-/-hiiret osoittivat vähemmän glomerulonefriittiin liittyvien autovasta-aineiden ja immuunikompleksien kehittymistä, toisin kuin villityypin hiirissä. P2X7:llä, ekstrasellulaarisella ATP-avainnetulla ionikanavareseptorilla, on myös osoitettu olevan rooli NLRP3-aktivaatiossa ja LN-kehityksessä. Selektiivisen P2X7-antagonistin käyttö briljantinsinisissä Gin MLR/Ipr -hiirissä aiheutti NLRP3/ASC/kaspaasi-1-kompleksin heikkenemisen ja siten IL- :n suppression. Tämä vähensi LN:n vakavuutta, proteinuriaa ja veren ureatyppitasoja hiirillä. Samoin P2X7/NLRP3:n esto vähentää Th17:Treg-suhdetta, mikä vähentää kaksijuosteisten DNA-vasta-aineiden (anti-dsDNA) määrää. NZM2328-hiiret, joille injektoitiin suonensisäisesti adenovirusta ilmentäviä interferoni-c-partikkeleita, vahvistivat nämä tulokset [82]. P2X7:n lisääntynyttä ilmentymistä on havaittu myös SLE-potilaiden munuaiskudoksessa [83]. Neutraloivan monoklivasta-aineen erittäin liikkuvalle box 1 -proteiinille, DNA:han sitoutuvalle ubikvitiinin ydinproteiinille, on myös osoitettu vähentävän IL-, IL-6, IL-17 ja IL{{42} } tasot ja kaspaasi-l BXSB-hiirten munuaisissa. Lisäksi tämä malli heikensi myös proteinuriaa, glomerulonefriittiä, munuaisten immuunikompleksikertymiä ja kiertävää anti-dsDNA:ta.
Toinen LN:iin vaikuttava tulehdusreitti on NF-kB. NF-KB on transkriptiotekijä, joka osallistuu synnynnäiseen ja adaptiiviseen immuniteettiin [85]. Ihmistutkimuksissa on kuvattu korrelaatio NF-kB:n aktivoitumisen ja histologisen ja munuaisten toiminnan heikkenemisen välillä [86]. Zhao et ai. [87] tutki, vähensiko molempien reittien estäminen LN:n etenemistä lupukseen alttiissa MRL/LPR-hiirissä. Tämän kiinnostuksen laukaisi NF-kB:n munuaisten patofysiologinen rooli. Bayn NF-kB:n ja NLRP3:n esto{10}} esti niiden muodostumisen ja aktivoitumisen, mikä johti LN:n todetun munuaisvaurion paranemiseen. Lisäksi Bayl1-7082 vähensi munuaisten immuunikompleksikertymiä ja seerumin anti-dsDNA-tasoja.
AIM2 on myös osallisena SLE:n patogeneesissä. Sen eston on kuitenkin osoitettu olevan kaksitahoinen suhteessa LN:n patofysiologiaan. Zhang ja työtoverit analysoivat korrelaatiota LN:n ja AIM2:n vakavuuden välillä SLE-potilailla ja lupushiirillä. AIM2-ekspressio oli kohonnut SLE-potilaiden PBMC:issä. Lisäksi AIM2 korreloi makrofagien aktivaation kanssa ja lisääntyi lymfosyyteistä peräisin olevan apoptoottisen DNA:n indusoimissa makrofageissa. AIM2:n esto siRNA:lla vähensi makrofagien tunkeutumista munuaiskudokseen ja paransi munuaistulehdusta [88] Muut tutkijat havaitsivat kuitenkin, että AIM2:n esto aiheutti alttiutta SLE:n kehittymiselle. p202 säätelee negatiivisesti AIM2:ta joissakin hiirikannoissa, mikä lisää INF:ää ja alttiutta SLE:lle.
7.1.3. Ihmisen malli
Inflammasomin roolia autoimmuunisairauksissa on kuvattu laajasti. Kirjallisuudessa on raportoitu tutkimuksia erilaisilla SNP:illä, jotka liittyvät inflammasomiin SLE-potilailla. Pontillo et al.[90] analysoi 14 SNP:tä 7 tulehduksellisessa geenissä, kuten NLRP1, NLRP3, NLRC4, AIM2, CARD8, CASP1 ja IL1B. Tutkimus osoitti ensimmäistä kertaa yhteyden SNP:n ja SLE:n välillä Etelä-Brasilian väestössä. NLRP1 rs2670660 SNP, varsinkin yhdistettynä NLRP1-variantin rs12150220 kanssa, lisää riskiä SLE:lle ja kehittää nefriittiä, niveltulehdusta ja ihottumaa. Muut SNP:t, jotka on myös kuvattu autoimmuunisairauksissa, kuten keliakia [91] ja diabetes [21], eivät liittyneet SLE-tautiin heidän populaatiossaan [90]. He eivät myöskään löytäneet yhteyttä SLE:hen AIM2- tai IL1B-polymorfismien suhteen [90]. Lisäksi tulokset da Cruz et ai. havaitsi toiminnan lisääntymisen NLRP3 rs10754558 -variantissa potilailla, joilla on LN.

7.2.ANCA Glomerulonefriitti
Vaskuliittiin liittyvä ANCA (AAV) on henkeä uhkaava autoimmuunisairaus, jolle on tunnusomaista vasta-ainevälitteinen glomerulonefriitti ja nekrotisoiva vaskuliitti. AAV vaikuttaa pieniin ja keskikokoisiin verisuoniin, erityisesti elimiin, kuten munuaisiin ja keuhkoihin. Pauci-immuuni- ja nekrotisoiva glomerulonefriitti liittyy usein potilailla, joilla vaskuliitti on yleisempää yli 50-vuotiailla miehillä. ANCA-vaskuliitti liittyy yleensä ANCA-myeloperoksidaasiin (MPO), ANCA-proteinaasi 3:een (PR3) tai ANCA-negatiiviseen serotyyppipositiivisuuteen. Tämä patologia luokitellaan erilaisiin kliinisiin muunnelmiin, kuten mikroskooppiseen polyangiittiin, granulomatoosiin polyangiitin kanssa (Wegener) ja eosinofiiliseen granulomatoosiin polyangiitin kanssa (Churg-Strauss) tai munuaiskudokseen rajoittuva vaskuliitti [93]. Sekä synnynnäinen että adaptiivinen immuniteetti osallistuvat AAV:n kehittymiseen, vaikka tarkat mekanismit ovat vielä selvittämättä.
Neutrofiileillä on perustavanlaatuinen rooli AAV:n patogeneesissä, joka aiheuttaa kudosvaurioita ANCA-vasta-aineiden aiheuttaman degranulaation jälkeen. Vasta-aineiden lisäksi T-solut osallistuvat myös taudin patogeneesiin. Neutrofiilit erittävät sytokiinejä, jotka rekrytoivat enemmän neutrofiilejä ja muita tulehdussoluja. T-solujen infiltraatio on myös osa granuloomia. Anti-T-soluhoitojen hyöty osoittaa tämän solun osallistumisen AAV:hen. Th1- ja Th17-fenotyypit ovat mukana akuutissa vaiheessa. C5a:n lisääntymistä ja siten vaihtoehtoisen komplementtireitin osallistumista on raportoitu.
7.2.1. In vitro -malli
Tulehduskomponentit, kuten sytokiinit, ovat tärkeitä välittäjiä AAV:ssä. Sekä Il-1 että Il-18 on liitetty AAV:n patogeneesiin, joten tulehduksen osallisuutta tämän taudin tulehduskaskadissa odotetaan.
l-18 vaikuttaa neutrofiilien kemoattraktioon TNFa:n pohjustuksesta [95], toisin kuin muissa tutkimuksissa on raportoitu. Hewins et ai. osoittivat, että anti-TNF-vasta-aineen läsnä ollessa ANCA-indusoitu superoksidituotanto ei vähentynyt. Tämä selittäisi kudosvaurion pysyvyyden anti-TNF-hoidon läsnä ollessa. Lisäksi Hewins ja kollegat osoittivat munuaisten Il{5}}-ilmentymistä potilailla, joilla oli ANCA-vaskuliitti.
7.2.2. Eläinmalli
Useat tutkimukset osoittavat ANCA:n nekrotisoivan puolikuu GN:n (NCGN) eläinmalleissa [97]. Dipeptidyylipeptidaasi (DPPI) on kysteiiniproteaasi, joka vastaa neutrofiilien seriiniproteaasien (NPS), kuten katepsiini G(CG), neutrofiilielastaasin (NE) ja PR3:n, aktivoimisesta. Nämä tulehduksen moduloinnista vastaavat entsyymit on liitetty ANCA-vaskuliitin patofysiologiaan. Anti-MPO-vasta-aine-indusoidussa NCGN:n kokeellisessa mallissa DPPI:n suojaava rooli munuaissairaudessa osoitettiin tulehduksellisten sytokiinien, erityisesti IL-1:n paikallisella vähenemisellä [98]. Itse asiassa PR3:n ja NE:n Il-1 nousu ja käsittely on yhdistetty [99]. Scheiberin et al.[98]ryhmä osoitti, että aktiivinen PR3 tai aktiivinen PR3/NE lisää sytokiinien ja anti-MPO-vasta-aineiden määrää, jolloin syntyy NCGN. He tuottivat NE-/PR{14}}hiiriä, jotka oli suojattu NCGN:ltä. Tämä osoitti NSP:n roolin ANCA-nefropatiassa. Lisäksi he huomasivat, että hoito anakinralla, IL-1-reseptorin antagonistilla, heikentää tulehdussarjaa ja suojaa NCGN:ltä.
Toinen erilainen reitti, joka indusoi Il{0}}-tuotantoa ja aiheuttaa NCGN:n, liittyy fagosyyttien NADPH-oksidaasiin (Phox). Phox on hemiproteiinin heterodimeeri pg91phoxista ja p22phoxista, joka vastaa ROS:n tuottamisesta kudosvaurioita [100]. Jotkut tutkimukset kuitenkin selittävät, että ROS osallistuu myös tulehduksen tyrehtymiseen [101]. Toinen tutkimus saksalaiselta Schreiberin et al. [100] havaitsivat Phoxinin roolin tulehduksen rajoittamisessa alentamalla sen komponentteja, kuten kaspaasia-1 ja siten IL-1. Nämä kirjoittajat loivat vasta-ainevälitteisen anti-MPO-mallin. Siirretyillä hiirillä, joilla oli gp91phox-puutos tai p47phox-puutos luuydintä, havaittiin suurempi histologinen osallistuminen ja enemmän tulehdusta ja nekroosia verrattuna hiiriin, joilla oli villityyppinen luuydin. Lisäksi ne tuottivat myös pg91phox/kaspaasi{16}-puutteellisia luuytimensiirtohiiriä. Tässä tapauksessa hiiret, joilla oli kaksoispuutos, paransivat NCGN:ää verrattuna hiiriin, joilla oli vain pg91phox-puutos. Nämä tulokset olettavat, että Phox rajoittaa kaspaasin{19}} aktiivisuutta ja siten tulehduksen roolia.
7.2.3.Ihmismalli
Kohonneita seerumipitoisuuksia tulehduksellisten komponenttien kaskadissa on havaittu myös potilailla, joilla on ANCA-vaskuliitti. IL-18-tasoja on havaittu potilailla, joilla on ANCA-vaskuliitti MPO- tai PR3-arvoista riippumatta. On yleisesti hyväksytty, että munuaisten interstitiaalinen vaurio on täytynyt liittää munuaiskerästen vaurioon, mutta on olemassa tapausraportteja potilaista, joilla on ANCA-vaskuliitti, jolla oli vain interstitiaalinen vaurio [103,104]. Tashiro et ai. ei osoittanut korrelaatiota glomerulusvaurion ja interstitiaalisen vaurion välillä ANCA-vaskuliittia sairastavien potilaiden biopsioista. He havaitsivat IL-1-tasojen korrelaation tubulointerstitiaalisen vaurion vakavuuteen. Lisäksi tunkeutuvat makrofagit osoittivat positiivista värjäytymistä NLRP3:lle tubulointerstitiumissa havaitsematta tätä positiivisuutta glomeruluksessa. Päinvastoin, Hewins et ai. [95], jotka löysivät munuaisbiopsioista lisääntynyttä IL-18-säätelyä, raportoivat, että podosyyteissä on havaittu positiivisuutta glomeruluksessa, kun taas tubulointerstitiumissa IL-18--positiivisuutta on havaittu tunkeutuvissa makrofageissa, myofibroblasteissa ja tubulusepiteelissä. soluja.
NOD:n kaltaisten reseptorien aktivaatio potilailla, joilla on ANCA-vaskuliitin aktiivinen vaihe, on peräisin Wangista et ai. [106]. NOD2:n, NLRP3:n ja NLRC5:n keskimääräiset optiset tiheydet sekä glomeruluksessa että tubulointerstitiumissa olivat merkittävästi korkeammat potilailla, joilla oli ANCA-vaskuliitti kuin terveillä kontrolleilla, potilailla, joilla oli minimaalinen muutos sairaus, ja potilailla, joilla oli tyypin IV LN. NLR:t ilmentyivät pääasiassa podosyyteissä ja tunkeutuvissa monosyyteissä ja makrofageissa, mutta tuskin ilmentyivät glomeruluksissa, tulokset olivat samanlaisia kuin Tashiro et al. NOD2:n ja NLRC5:n ilmentyminen korreloi kliinisopatologisen osallisuuden kanssa, kun taas NLRP3 ei [106]. Toisin kuin nämä tutkijat, Tashiro ja kollegat korreloivat NLRP3:n munuaisvaurion vakavuuteen.

7.3.IgA-nefropatia
IgA-nefropatia (IgAN) on glomerulonefriitin aiheuttaman munuaisten vajaatoiminnan tärkein syy maailmassa. Myös synnynnäisen immuniteetin komponentit ovat mukana tässä nefropatiassa. IgA-aggregaattien tai IgA-immuunikompleksien kerrostumista ja sitä seuraavaa tulehdusta aiheuttavien T-solujen aktivaatiota pidetään taudin pääsyynä. Keräskeräkseen kerääntynyt lgA-alaluokka on IgA1, jolla on keskeinen rooli taudin patofysiologiassa. Mesangiaalisolujen lisääntyminen on tyypillinen IgAN:n histologinen löydös. Mesangiaalisolut lisääntyvät muiden sytokiinien ohella IL-1:n vaikutuksesta. Tulehduskaskadissa mukana olevien sytokiinien osuus viittaa tämän tulehduskomponentin rooliin IgAN:ssa.
Vaihtoehtoinen komplementtireitti ja lektiinireitit ovat myös osallisena taudin kehittymisessä, koska C3, C4, C4d, propidiini, C5b-C9 ja mannoosia sitova lektiini havaitaan yleensä munuaisbiopsiassa.
7.3.1. Eläinmalli
Tutkijat ovat osoittaneet IL-1:n ilmentymisen munuaiskudoksessa, johon IgAN vaikuttaa [110,111]. Chen et ai., käyttämällä IgAN-eläinmallia ddY-hiirillä, havaitsivat vähentyneen mesangiaalisen proliferaation hiirissä, joita hoidettiin IL-1-reseptorin antagonistilla (IL-1ra). Nämä tulokset viittaavat siihen, että IL-1 on mukana IgAN-kehityksessä, mikä osoittaa tulehduksellisen kaskadin mahdollisen roolin IgAN:ssa.
7.3.2.Ihmis-/in vitro -malli
NLRP3:n rooli lgAN:ssa on vielä selvittämättä. Kanadalainen Chun et al. oli ensimmäinen, joka arvioi in vivo ja in vitro NLRP3:n ilmentymistä IgAN-potilaiden munuaisissa ja taudin etenemistä. He havaitsivat, että NLRP3 ilmentyi pääasiassa tubuluksissa ilman värjäytymistä normaalissa glomeruluksessa. Kuitenkin potilailla, joilla oli IgAN, NLRP3:n ilmentyminen havaittiin glomeruluksessa, vaikka se olikin lisääntynyt tubuluksissa. Sekä ihmisen munuaisbiopsioissa että vähän kulkeutuvissa ihmissoluissa ne havaitsivat NLRP3:n laskun tubulusvaurion aikana. Samoin immunovärjäystulokset ja NLRP3-mRNA:n ilmentyminen vahvistivat NLRP3:n läsnäolon ja sen myöhemmän menetyksen munuaisvaurion jälkeen. Nämä löydöt viittaavat siihen, että NLRP3 voi olla putkimaisen eheyden biomarkkeri. Lisäksi NLRP3:lla on roolinsa munuaissairauden varhaisissa vaiheissa, jotka liittyvät krooniseen munuaissairauteen. Tutkimusrajoitusten vuoksi tutkijat eivät kuitenkaan pystyneet raportoimaan tulehduksen toiminnallisesta roolista.
Muut tutkijat pystyivät havainnoimaan NLRP3:n roolia lgAN:n patofysiologiassa. IgA-immuunikompleksit saivat aikaan NLRP3-tulehduksen aktivoitumisen makrofageissa. Tämä puolestaan stimuloi mitokondrioiden ROS-tuotantoa. He suorittivat hiirimallin, jossa oli IgAN-poisto NLRP3:lle. Knockout-hiiret estivät IgA-immuunikompleksien muodostumista. Munuaisten toiminnan palautuminen kuvattiin NLRP3-poistossa ja NLRP3:n shRNA:n munuaisiin kohdistetussa toimituksessa. Lopuksi tutkijat selventävät, etteivät he voi sulkea pois muiden inflammasomien roolia lgAN:ssa ja että shNLRP3:n käyttö voisi olla hoitoa sairauden parantamiseksi tai ehkäisemiseksi.

7.4 Anti-Glomerulaarinen Basement Membrane Glomerulonefriitti
Anti-glomerulaarinen tyvikalvo (anti-GBM) on harvinainen autoimmuunisairaus, joka vaikuttaa munuaisten ja keuhkojen pieniin verisuoniin. Potilaat kehittävät vasta-aineita kyseisten elinten tyvikalvossa olevan tyypin IV kollageenin 3-ketjun ei-kollageenista domeenia vastaan[115]. Vaikka humoraalisella immuniteetilla on keskeinen rooli, myös soluimmuniteetin osallistumista on raportoitu. Siten lgG1- ja IgG3-alaluokat ovat olleet selvästi yhteydessä taudin vakavuuteen. Vasta-aineiden kerääntyminen munuaissuoniin voi aiheuttaa tulehduksen aktivoimalla komplementtia ja Fc-reseptoria. Toisaalta CD4 plus T-solujen lisääntyminen on korreloinut taudin vaikeusasteen kanssa. Perifeerinen CD4 plus etenee c3 (IV) NC1:n läsnä ollessa. Lisäksi CD4 plus:n on osoitettu eläinmalleissa laukaisevan anti-GBM-vasta-aineiden kehittymisen.
Eläin malli
Tulehduskaskadista peräisin olevilla tärkeimmillä sytokiineilla, IL-1 ja IL-18, on osoitettu olevan patofysiologinen rooli potilailla, joilla on anti-GBM-sairaus. Anti-GBM-, Il-1 -/- ja IL1-tyypin 1 reseptorien (IL-1R)-/-hiirten hiirimallissa IL-1-isoformien, IL{{ 12}} ja IL-1, anti-GMB GN tutkittiin. IL-1ß-hiirillä havaittiin vähemmän puolikuun muotoisten muodostumien kehittymistä ja makrofagien ja T-solujen kerääntymistä, kun taas IL-1R1 -/-hiirillä näytti olevan rooli immuunivasteessa, koska ne oli vähemmän vasta-aineita seerumissa. Lisäksi muut eläinmallit ovat osoittaneet IL-18:n proinflammatorisen roolin munuaistulehduksessa.
Makrofagien aiheuttama glomerulaarinen infiltraatio on luultavasti yksi tärkeimmistä IL{0}}-sytokiinituotannon lähteistä. Useat tutkimukset ovat analysoineet tämän sytokiinin kemoattraktanttiroolia ja ottaneet käyttöön hoidon antagonisteilla IL-1ra rottamallissa, jossa on anti-GBM. Sekä Lan et ai. ja Tang et ai. osoitti, että käyttämällä IL-1ra:ta glomerulusten makrofagien infiltraatio väheni ja proteinuria parani. Lan et ai. paljasti myös munuaisten toiminnan pahenemisen pysähtymisen ja esti histologisen etenemisen, kuten glomeruluskuuppien muodostumisen. Tang et ai. sai ICAM-1:n vähentyneen ilmentymisen IL-1ra-hoidon jälkeen, mikä liittyi myös polymorfonukleaaristen (PMN) solujen ja monosyyttien infiltraation vähenemiseen.
Kuitenkin Timošenko et al. [117] IL-1:n vaikutuksesta anti-GBM:n munuaistulehdukseen, muut kirjoittajat päättelivät hiiren mallia käyttäen, että vain pääasiassa tubulointerstitiumissa sijaitsevat dendriittisolut ilmentävät pro-IL--1-proteiinia ja siksi ne aktivoivat NLRP3:a ja kaspaasia-1 erittävän kypsää IL:tä-1. He osoittivat, että tulehduksellinen akseli ei edistä glomerulustulehdusta, koska glomerulussolut eivät pystyneet tuottamaan IL-1:a steriilin tulehduksen aikana.
8. Loppuhuomautukset
Kuten kattavasti on esitetty, monet tutkimukset ovat osoittaneet tulehduksen roolin glomerulonefriitissä. Tulehduksellisiin ja autoimmuunisairauksiin kohdistuvaan patofysiologisten mekanismien tutkimukseen tarvitaan kuitenkin lisätietoa.
Toisaalta tulehduksen osallistuminen immuniteettiin rohkaisee tarvetta uusille terapeuttisille aseille, jotka tähtäävät sen modulointiin. Äskettäin IL{0}}ra:n antagonistit on jo hyväksytty muiden kuin munuaisten sairauksien, kuten nivelreuman, CAPS:n, familiaalisen Välimeren kuumeen ja Stillin taudin hoitoon. Lisäksi tällä hetkellä kehitetään autoimmuunisairauksien hoitoa potilailla, jotka eivät reagoi tai ovat ajan mittaan resistenttejä hoidolle TNF-antagonisteilla ja/tai T-solujen yhteisstimulaatioantagonisteilla IL-18-antagonistin kanssa. Ottaen huomioon, että IL-1-salpaus tai IL-18-antagonisti on onnistunut tulehduksellista aktivaatiota moduloivissa munuaissairauksien ei-ihmismalleissa. Ehkä olemme valmiita ottamaan nämä kohteet käyttöön nefrologisissa klinikoissa. Yhden sytokiinin salpaus ei kuitenkaan välttämättä riitä vähentämään tulehduksen aktivoitumista, vaan polyterapiaa voitaisiin harkita. Tietojemme mukaan, vaikka autoimmuuni- ja tulehdussairauksista on kehitetty kliinisiä tutkimuksia, ei ole meneillään kliinisiä tutkimuksia, jotka koskevat glomerulonefriittia ja tulehduksia. Siten lisäponnistelut sen selvittämisessä, kuinka hoidot vaikuttavat tulehduksellisen akselin toimintaan, voisivat olla lupaava hoito.
